
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Глава 2. ОПУХОЛИ ПЕЧЕНИ 2 page
|
|
Лечение. При злокачественном поражении печени применяют химио-, лучевую терапию и хирургическое вмешательство.
Химиотерапия не является радикальным методом лечения, но при неоперабельных опухолях печени, множественных метастазах ее применяют и как самостоятельный метод. Консервативное лечение используют также для усиления эффекта оперативных методов в целях профилактики дальнейшего прогрессирования процесса. В настоящее время комбинированный метод лечения получил положительную оценку.
Самым распространенным и широко доступным препаратом является фторурацил. Препарат назначают по 3,5—5—15 мг на 1 кг массы тела в сутки. Срок лечения не менее 3 мес.
Продолжительность жизни больных первичным раком печени, получавших только фторурацил, составляет в среднем 4,7 мес (A. A. Inouye и Т. J. Whelan, 1979).
При использовании химиотерапии как самостоятельного метода лечения улучшение состояния отмечается у 35—40 % больных (Г. А. Клименко, 1973; С. А. Шалимов и соавт., 1988).
Некоторые хирурги для инфузии химиотерапевтических препаратов используют пупочную вену (В. С. Шапкин и соавт., 1976, и др.). В пупочную вену вводят также гепатотропные радионуклиды (лантан, перий, торий, золото, хромфосфат и др.), действие которых окончательно еще не изучено.
При проведении комбинированной химиотерапии 117 больным с метастазами колоректального рака в печень средняя продолжительность жизни составила 11,5 мес (J. G. Fortner и соавт., 1984). При этом у 40 % больных заболевание не прогрессировало, а у 13 °/о появились метастазы в других органах без прогрессирования метастазов в печени.
При сравнении различных схем химиотерапии наиболее эффективным оказалось внутривенное введение фторурацила по 325 мг/м2 в сутки с 1-го по 5-й день и с 36-го по 40-й день в комбинации с цисплатиной по 110 мг/м2 в 1-й день и адриамицином по 40 мг/м2 с 1-го по 36-й день (G. Falkson и соавт., 1984).
В КНИИКЭХ обобщены результаты рентгенохирургического и химиотерапевтического лечения 66 больных с опухолями печени (первичный рак и метастатическое поражение печени при локализации процесса в других органах, чаще метастазы колоректального рака). Диагноз подтвержден пункционной биопсией, данными ультразвукового и радиологического исследований, ангиографией, лапароскопией, лапаротомией. У всех больных диагностирована IV стадия процесса. Больным проводили суперселективную химиотерапию раствором полиплатиллена, который вводили внутриартериально трехкратно по 225 мг с интервалами 2—5 дней в зависимости от состояния больного. Суммарная доза препарата составляла 750—820 мг на курс в пересчете на цис-платину. Эмболизацию собственной печеночной артерии проводили гидрогелем полиметилсилоксана с добавлением 225 мг лиофилизированного полиплатиллена. В крупные опухолевые очаги вводили лиофилизированный полиплатиллен в виде суспензии в дозе 150—225 мг.
В зависимости от метода лечения больные были разделены на 4 группы: 11 больным 1-й группы проводили рентгеноэндоваскулярную окклюзию собственной печеночной артерии или ее ветвей, непосредственно васкуляризирующих опухоль; 15 больным 2-й группы проводили эмболизацию печеночной артерии в сочетании с двумя-тремя курсами инфузионной терапии полиплатилленом; 11 больным 3-й группы с двумя-тремя крупными патологическими очагами в печени полиплатиллен вводили непосредственно в очаги поражения печени под контролем эхолокации, а в дальнейшем, через 2, 4 и 6 мес, проводили регионарную инфузионную терапию полиплатилленом; больным (28 человек) 4-й группы с поражением воротной вены, которым рентгеноэндоваскулярная окклюзия не показана, проводили селективную инфузионную терапию полиплатилленом через чревный ствол.
После проведенного лечения отмечали снижение или полное исчезновение болевого и паранеобластического синдромов, уменьшение явлений интоксикации, улучшение сна и аппетита. Стабилизировались или снижались показатели гуморального и повышались показатели клеточного иммунитета.
Описанные методы лечения позволяют сочетать ишемизацию патологического очага методом рентгенохирургии с суперселективной химиотерапией. Это обеспечивает создание высоких концентраций химиопрепаратов и их депонирование в очагах малигнизации при минимальном общетоксическом действии на организм.
По сравнению с другими паллиативными методами лечения применяемые нами рентгенохирургические методы являются более эффективными и позволяют увеличить продолжительность жизни на 10—17,5 мес. Таким образом, рентгенохирургические методы лечения злокачественных опухолей печени следует более широко внедрять в клиническую практику.
Рентгенотерапию как самостоятельный метод применяют при неоперабельных опухолях в виде короткофокусного облучения в течение 3—5 нед в дозе 25—30 Гр. Эффект очень незначительный. Поэтому чаще используют комбинированную терапию — лучевую и химиотерапию (фторурацил, винкристин, эндоксан и др.).
Все же, несмотря на некоторый положительный эффект консервативной терапии при злокачественном поражении печени, он ненамного больше, чем при симптоматической терапии. Поэтому консервативную терапию следует применять лишь как вспомогательный метод.
Основным методом лечения злокачественных поражений печени является хирургический — иссечение опухоли в пределах здоровых тканей.
Показаниями к хирургическому лечению следует считать:
1) единичные крупные опухоли;
2) осложнения опухоли — кровотечение, перитонит, желтуха;
3) гормонально-активные метастазы в печени.
Противопоказания: снижение уровня альбумина в крови менее 35 г/л, асцит, олигурия, повышение содержания остаточного азота и мочевины в крови, повышение уровня билирубина в крови (более 34 мкмоль/л) при ненарушенной проходимости желчных протоков. Цирроз печени, даже не сопровождающийся нарушениями общего состояния больного и биохимических показателей крови, значительно повышает риск резекции печени. По данным Т. I. Lin (1973), после левосторонней гемигепатэктомии на фоне цирроза печени летальность составила 27%, а после правосторонней — 60 %. Поэтому при возникновении опухоли на фоне цирроза печени допустима лишь небольшая резекция органа и только при условии хорошего общего состояния больного и нормального содержания альбумина, билирубина и остаточного азота в крови.
Прорастание опухоли печени в диафрагму не должно служить препятствием к выполнению радикальном операции. Пораженный участок диафрагмы резецируют в пределах здоровых тканей в процессе мобилизации печени, а затем, после резекции печени, удаляют единым блоком с ней.
Для выполнения резекции печени предложено несколько операционных доступов (рис. 5).
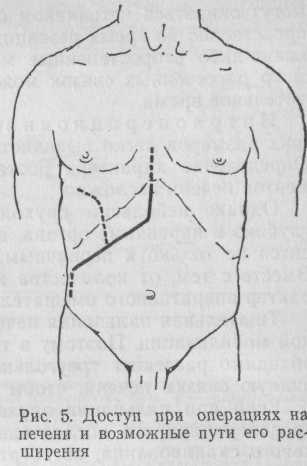
Основным преимуществом правосторонних торакоабдоминальных доступов со вскрытием грудной клетки по шестому или седьмому межреберью является создание широкого операционного поля, особенно при необходимости манипуляций на правой доле печени и нижней полой вене. Подобные доступы применяют Э. И. Гальперин и соавторы (1990), X. Рамеш (1990). Однако они очень травматичны, так как связаны со вскрытием двух полостей. Поэтому в условиях специализированного отделения при высокой хирургической технике и овладении методикой временного выключения печени из кровообращения мы считаем возможным производить все операции на печени из лапаротомного доступа. Если планируется удаление I— IV сегментов печени, прибегаем к верхнесрединной лапаротомии. При удалении IV—VIII сегментов выполняем клюшкообразный разрез, верхняя часть которого проходит по средней линии от мечевидного отростка до пупка, а затем линия разреза направляется вправо и полностью пересекает прямую мышцу живота. При необходимости разрез может быть продлен. Важно, чтобы вверху он доходил до мечевидного отростка, а при больших размерах последнего — огибал его справа до грудины.
Тщательную ревизию печени выполняем за счет широкой мобилизации органа. Во всех случаях пересекаем правую и левую треугольные связки, серповидную связку печени. Последнюю пересекаем близко от диафрагмы, чтобы при необходимости ее можно было использовать для укрытия культи печени. Во время пересечения связок необходимо внимательно осмотреть края разрезов. Небольшие артерии, проходящие в толще связок к диафрагме могут оказаться источником обильной кровопотери. Обычно непосредственно во время резекции печени нет возможности выполнять какие-либо второстепенные манипуляции, поэтому повторный осмотр рассеченных связок может быть проведен только через значительное время.
Интраоперационная диагностика. Опухоль больших размеров легко выявляется при осмотре и пальпации печени. Определение характера роста и расположения относительно сегментов печени несложно.
Однако небольшие опухоли диаметром 2—4 см, находящиеся глубоко в паренхиме органа, выявить удается не всегда. Это относится не только к первичным, но и к метастатическим опухолям. Вместе с тем, от количества и локализации опухолей зависит характер оперативного вмешательства.
Тщательная пальпация печени возможна только после ее широкой мобилизации. Поэтому в трудных диагностических случаях необходимо рассекать треугольные, печеночно-желудочную и серповидную связки печени, чтобы пальпировать орган двумя руками. Если при пальпации опухоль не обнаруживается, а данные предоперационного обследования (радионуклидного и ультразвукового сканирования, ангиографии) указывают на ее существование, производим интраоперационное ультразвуковое исследование. Для этого применяем специальные миниатюрные ультразвуковые датчики типа 10В-502 с частотой 5 МГц аппарата SAL-32B фирмы «Toschiba». Это позволяет производить акустическое сканирование различных участков печени и выявлять очаговые новообразования, а также разветвления сосудисто-протоковых магистралей. По данным А. В. Гаврилина и соавторов (1990), в отдельных наблюдениях при гепатоцеллюлярном раке в просвете воротной вены определяются ультразвуковые признаки опухолевого тромбоза. По данным тех же авторов, у 90,7 % больных с помощью интраоперационного обследования удалось выявить очаги поражения, в то время как эффективность дооперационных диагностических методик составляет 68,9 %. По нашим данным, информативность интраоперационного ультразвукового исследования составляет 97,6 %. Поскольку данные гистологического строения опухолей, особенно при расположении их глубоко в паренхиме печени, важны для выбора рационального объема операции, у 22 больных произведены повторные пункции в нескольких местах иглой диаметром 0,9 мм на всю толщину печени.
Попадание иглы в опухоль распознается по характерному уплотнению тканей и затрудненному продвижению иглы. Выполняем биопсию с последующим цитологическим исследованием пунктата для уточнения характера роста опухоли. Данные гистологического исследования биоптатов совпали с результатами гистологического исследования удаленных опухолей у 80 % больных.
При опухолях печени используют следующие методы оперативных вмешательств:
1) анатомическую резекцию печени с удалением опухоли;
2) атипичную резекцию печени с удалением опухоли;
3) деартериализацию печени;
4) установление катетера для интраартериальной инфузии;
5) другие паллиативные вмешательства.
Анатомическая резекция печени с удалением опухоли. Операция показана при: 1) первичном раке печени; 2) метастатическом раке, поражающем сегмент или долю печени; 3) небольших метастатических опухолях, которые трудно отделить от сегментарных или долевых сосудов.
Под анатомической резекцией печени понимают такой вид вмешательства, при котором линии рассечения паренхимы совпадают с межсекторальными и межсегментарными границами.
Теоретически возможно изолированное удаление каждого сегмента печени. Ниже приведено соотношение резекций печени, предлагаемых европейскими и американскими авторами. Однако на практике из-за особенностей анатомо-топографических взаимоотношений сегментов печени и других органов, а также локализации и распространенности опухоли применяют несколько видов анатомической резекции печени (рис.6):
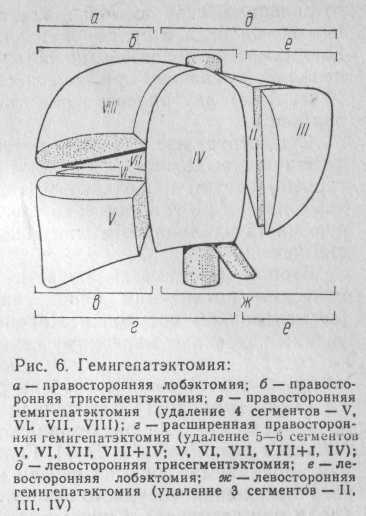
1) левостороннюю лобэктомию (удаление II и III сегментов); 2) левостороннюю гемигепатэктомию (удаление I—IV сегментов); 3) правостороннюю гемигепатэктомию (удаление V—VII сегментов); 4) расширенную правостороннюю гемигепатэктомию (удаление IV—VIII сегментов); 5) удаление IV, V и VIII сегментов.
При резекции печени могут быть использованы: а) техника с первичной лигатурой сосудов (Лортат — Джакоба); б) техника первичного рассечения паренхимы — комиссуральный способ (Т. Т. Тунга); в) сочетание обоих методов, когда накладывают зажимы на элементы ворот печени, не лигируя их, а после рассечения паренхимы лигируют видимые сосуды; г) полное прекращение поступления крови, когда после рассечения венечной связки, малого сальника, серповидной и круглой связок передавливается нижняя полая вена в супра- и инфрапеченочной части (сосуды передавливают не более чем на 60 мин); д) пережатие печеночно-дуоденальной связки при опасности кровотечения (временно, на 10 мин); е) внутрипеченочная окклюзия воротной вены надувным баллоном.
Существует две методики резекции печени. При первой методике вначале выделяют, пересекают и перевязывают долевые (сегментарные) сосуды и желчные протоки, после чего рассекают паренхиму печени по границе сохраненного кровообращения и пораженную часть удаляют. Эта методика носит название воротной резекции печени.
Вторая методика заключается в том, что по наружным анатомическим ориентирам определяют места прохождения долевых (сегментарных) сосудов и желчных протоков. По установленным линиям рассекают паренхиму печени, в толще ее поэтапно выделяют сосуды и желчные протоки, а затем поочередно пересекают и лигируют их. Паренхиму печени разделяют скальпелем и пальцами (Т. Т. Тунг, 1967). Описанная методика резекции печени носит название фиссуральной. Вариантом фиссуральной резекции печени является предложенная Э. И. Гальпериным (1988, 1990) селективная управляемая ишемия печени методом пальцевого чреспеченочного выделения сосудисто-секреторной ножки удаляемого отдела (доли или сегмента). Сущность метода заключается в том, что под контролем турникета, наложенного на печеночно-дуоденальную связку в месте наиболее вероятной проекции сосудисто-секреторной ножки удаляемого участка на висцеральную поверхность печени, определяемой относительно трех наименее вариабельных ориентиров (ложа желчного пузыря, поперечной борозды и круглой связки печени), производят надрез фиброзной оболочки печени длиной 3— 3,5 см, указательным пальцем хирург внутрипаренхиматозно входит, тоннелизируя паренхиму до обнаружения кончиком пальца на глубине 1,5—2 см плотноэластической структуры, которая, как правило, оказывается сосудисто-секреторной ножкой, захватывают ее изгибом пальца и вытягивают в надрез фиброзной оболочки печени. После этого на выделенную ножку накидывают турникет, печеночно-дуоденальную связку освобождают.
Преимущество этой методики, по мнению авторов, состоит в отсутствии необходимости длительной и травматической препаровки для выделения элементов сосудисто-секреторной ножки.
Перечисленные технические приемы резекции печени не исключают, а дополняют друг друга. Если удается быстро выделить и пересечь долевые (сегментарные) сосуды и желчные протоки, операцию выполняют по воротному типу. Однако в тех случаях, когда деление сосудов происходит в толще паренхимы печени, а опухоль резко изменяет взаиморасположение сосудистых стволов, целесообразнее произвести фиссуральную резекцию. Нередко в ходе одной операции используют обе методики резекции. Такая необходимость возникает при расположении опухоли у ворот печени или вблизи печеночных вен.
Левосторонняя лобэктомия — удаление II и III сегментов (рис. 7).
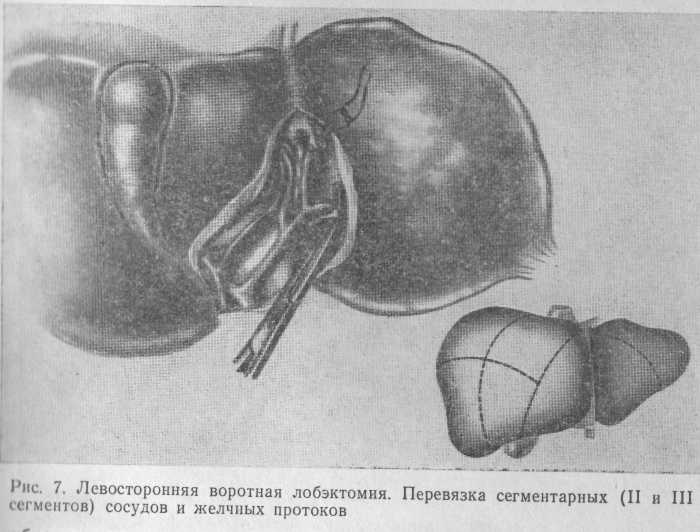
Выполняют верхнюю срединную лапаротомию. Рассекают треугольные и серповидную связки печени. Печеночно-желудочную связку рассекают на всем протяжении от желудочно-дуоденальной связки до диафрагмы. Находящиеся в связке лимфатические узлы смещают в сторону печени. Иногда в толще печеночно-желудочной связки проходит артерия к левой доле печени, которую следует отдельно перевязать и пересечь. Со стороны ворот печени выделяют собственную печеночную артерию, а также общий печеночный проток и воротную вену до места их деления на правую и левую ветви.
По ходу левых долевых сосудов и левого печеночного протока поэтапно рассекают паренхиму печени до места отхождения сосудов и желчного протока к IV сегменту печени. Выше этого уров-ня пересекают и перевязывают сосуды и желчный проток, идущие ко II и III сегментам. Затем первый ассистент движением руки сверху вниз отделяет печень от диафрагмы. Одновременно второй ассистент смещает диафрагму вверх. В поддиафрагмальном пространстве выделяют надпеченочный сегмент нижней полой вены и левую печеночную вену (рис. 8).
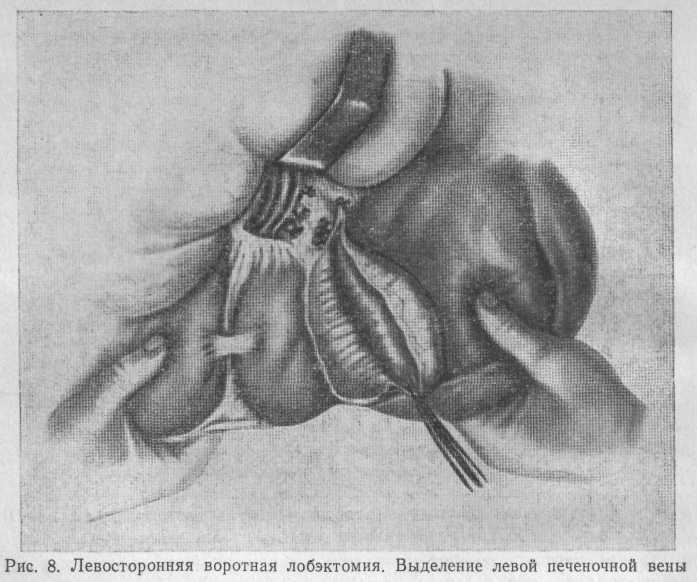
Последнюю перевязывают и пересекают (рис. 9).

По левому краю серповидной связки печени рассекают паренхиму печени по всей толщине ее. Плоскость разреза проходит по левому краю серповидной связки печени вверху и по левому краю нижней полой вены — внизу. Постоянный контроль местонахождения надпеченочного сегмента нижней полой вены дает возможность оценить толщину печени, направление ее рассечения. По мере рассечения паренхимы печени кровоточащие сосуды в плоскости разреза захватывают зажимами. Отсеченную долю печени удаляют вместе с опухолью. Отдельные сосуды и желчные протоки в плоскости разреза лигируют.
Если крово- и желчеистечения с раневой поверхности печени нет, мы не считаем необходимым дополнительное прошивание ее. кетгутовыми П-образными швами прошиваем паренхиму печени в тех случаях, когда имеется крово- и желчеистечение из мелких сосудов и желчных протоков, которые не удается лигировать или коагулировать.
Предложено несколько методов наложения швов на паренхиму печени. Наш опыт свидетельствует о том, что в большинстве случаев удается достичь достаточной компрессии путем наложения П-образных швов из двойной толстой кетгутовой нити. Только при дряблой паренхиме печени необходимо применять прокладки из серповидной связки печени или большого сальника. Существенным недостатком прошивания печени на всю толщину ее является нарушение кровотока и возможность некроза «отжатой» части паренхимы. Поэтому считаем необходимым накладывать швы не далее чем на 1 см от раневой поверхности, а при завязывании нити избегать прорезывания капсулы печени. Необходимо еще раз подчеркнуть, что при выполнении резекции строго по межсегментарным промежуткам крово- и желчеистечение с раневой поверхности бывает незначительным и его можно полностью устранить путем перевязки отдельных сосудов и желчных протоков, без прошивания всей паренхимы печени.
Тщательность гемостаза оценивают при нормальном артериальном давлении. Нередко большая резекция печени сопровождается снижением артериального давления. В этих условиях не следует спешить с окончанием операции, надо дождаться нормализации объема циркулирующей крови и артериального давления и лишь затем приступить к установлению дренажей и зашиванию брюшной полости. Несоблюдение этого правила явилось причиной массивного кровотечения у 1 наблюдаемого нами больного.
Для отграничения подпеченочного и поддиафрагмального пространства от остальной брюшной полости к передне-задней поверхности подшивают большой сальник. К раневой поверхности печени через контрапертуры подводят перчаточно-трубчатые дренажи. Количество дренажей зависит от величины раневой поверхности и особенностей расположения других органов. Обычно после левосторонней лобэктомии один дренаж подводят к левому краю печеночно-дуоденальной связки, а второй — под купол диафрагмы к устью левой печеночной вены.
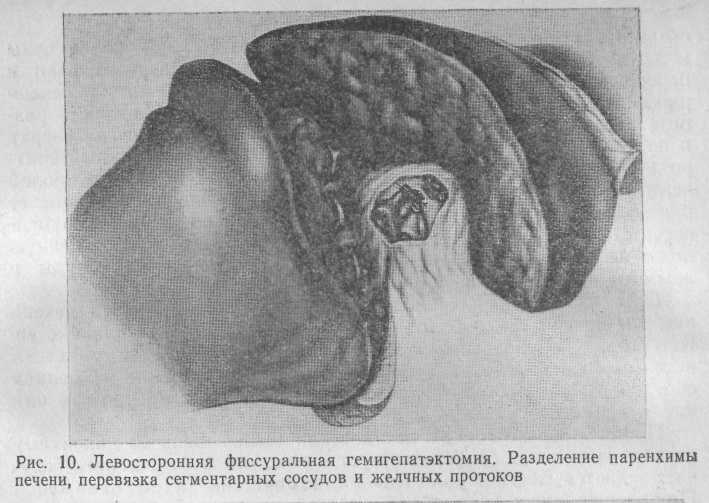
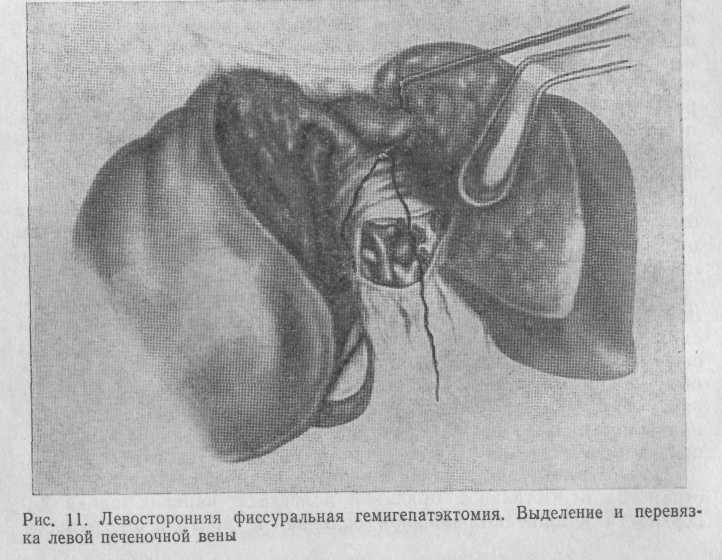
На рис. 10 и 11 показаны отдельные этапы левосторонней фиссуральной гемигепатэктомии, сущность которой описана выше.
Левосторонняя гемигепатэктомия (удаление I — IV сегментов). Оперативный доступ — верхняя срединная лапаротомия. Пересекают треугольные, серповидную и печеночно-желудочную связки печени, как при левосторонней лобэктомии. И в воротах печени отыскивают место деления общего печеночного протока (рис. 12, а), собственной печеночной артерии и воротной вены и перевязывают ветви, идущие к левой доле печени. Если общий печеночный проток или сосуды делятся по типу трифуркации, то центральную ветвь обычно берут на турникет с тем, чтобы при необходимости после окончательной идентификации ее можно было легко перевязать (рис. 12, б).
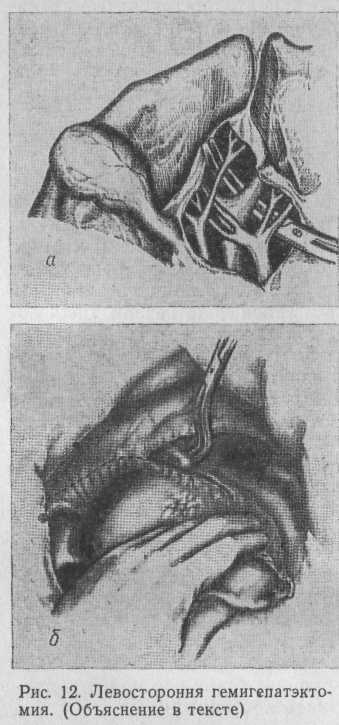
Выделяют подпеченочный сегмент нижней полой вены и перевязывают венозные ветви, идущие от I сегмента. Затем выделяют надпеченочный сегмент нижней полой вены, левую и среднюю печеночные вены. Левую вену перевязывают и пересекают, а среднюю используют как ориентир при резекции. Плоскость рассечения паренхимы печени проходит сверху от дна желчного пузыря до средней печеночной вены, снизу—по середине нижней полой вены.
В ходе рассечения паренхимы печени в толще ее иногда обнаруживают среднюю печеночную вену в виде крупного сосуда, идущего вдоль линии разреза. Сместив разрез несколько влево, вену сохраняют, левые ветви ее захватывают зажимами и после удаления резецированного участка перевязывают.
Обработку культи печени, дренирование брюшной полости производят так же, как после левосторонней лобэктомии.
Правостороннюю гемигепатэктомию (удаление V—VIII сегментов) выполняют из клюшкообразного разреза с пересечением правой прямой мышцы живота на уровне пупка (рис. 13).
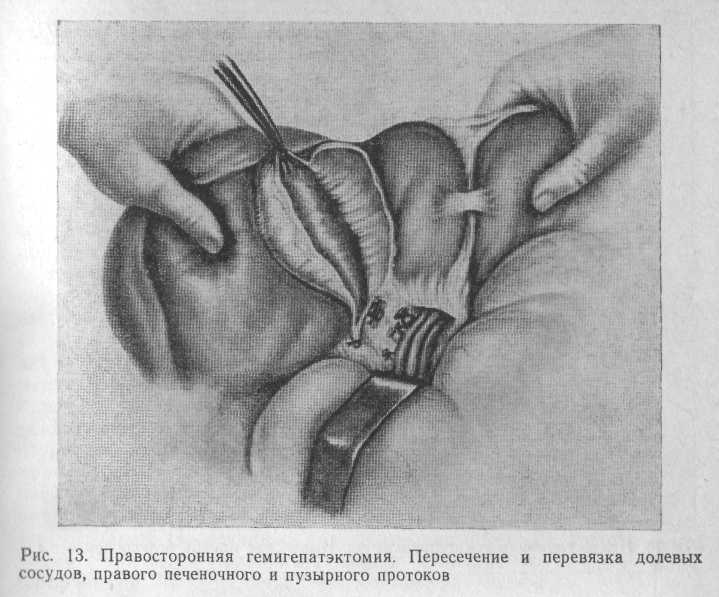
Пересекают треугольные и серповидную связку печени. Выделяют элементы печеночно-дуоденальной связки на уровне пузырного протока. Так как линия отсечения печени проходит через ложе желчного пузыря, обычно одновременно с резекцией печени выполняют холецистэктомию. Поэтому пузырный проток и пузырную артерию пересекают и перевязывают. В воротах печени выделяют, пересекают и перевязывают правые ветви собственной печеночной артерии и воротной вены, желчный проток правой доли печени (рис. 14, 15).
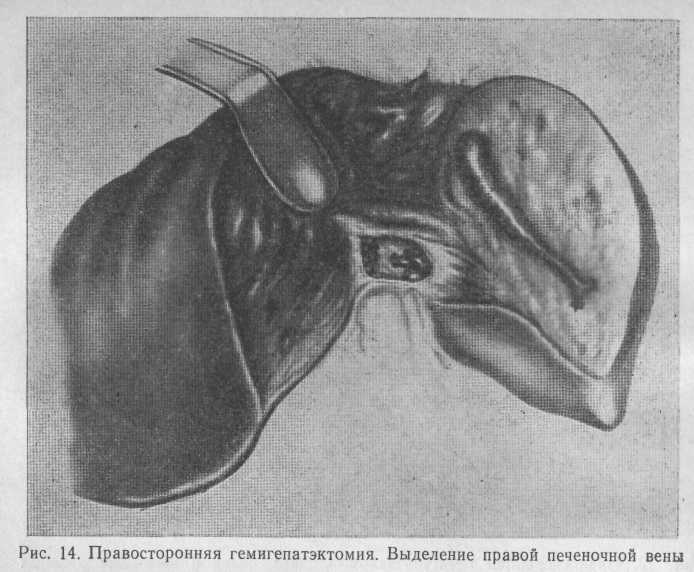
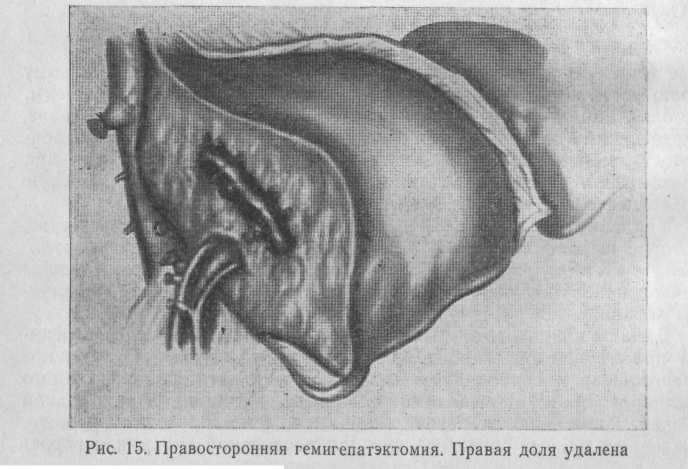
В поддиафрагмальном пространстве выделяют, пересекают и перевязывают правую печеночную вену. Плоскость рассечения печени проходит вверху от дна желчного пузыря к правой печеночной вене, внизу — по ходу нижней полой вены. Желчный пузырь смещают в сторону правой Доли печени и удаляют единым блоком с ней. В области VI и VII сегментов по задней поверхности печень фиксирована рыхлыми сращениями к забрюшинной клетчатке и листком брюшины, переходящим на брюшную стенку. Листок брюшины пересекают, а клетчатку тупо расслаивают. В результате правая доля печени оказывается фиксированной только в области внутрипеченочного сегмента нижней полой вены. Этот этап операции надо выполнять очень осторожно, так как грубые манипуляции могут привести к повреждению правого надпочечника, находящегося на уровне V сегмента печени (в забрюшинной клетчатке). Поэтапно расслаивая паренхиму печени по ходу нижней полой вены, выделяют, пересекают и перевязывают мелкие венозные ветви от V и VII сегментов. Обычно их 2—3. После этого извлекают из поддиафрагмального пространства V—VIII сегменты печени и удаляют их.
Раневую поверхность печени обрабатывают так же, как после левосторонней лобэктомии. Остаточную полость обычно дренируют тремя перчаточно-трубчатыми дренажами: два из них через контрапертуру в правом подреберье проводят к воротам печени и вдоль нижнего края раневой поверхности, а третий — через контрапертуру в девятом или десятом межреберье — к культе правой печеночной вены.
Расширенная правосторонняя гемигепатэктомия —удаление IV—VIII сегментов (рис. 16).

Разрез брюшной стенки, мобилизацию печени, выделение элементов печеночно-дуоденальной связки выполняют так же, как при правосторонней гемигепатэктомии. В поддиафрагмальном пространстве выделяют, пересекают и перевязывают правую и среднюю печеночные вены. Линии рассечения печени проходят вверху по правому краю серповидной связки, внизу — по ходу нижней полой вены. Мобилизацию задней поверхности VI и VII сегментов, выделение, пересечение и перевязку мелких ветвей от печени к внутрипеченочному сегменту нижней полой вены осуществляют так же, как при правосторонней гемигепатэктомии. Так же обрабатывают раневую поверхность и дренируют остаточную полость.
Удаление IV, V и VIII сегментов— сложное вмешательство, которое выполняют только в тех случаях, когда опухоль расположена в области указанных сегментов, а функциональные резервы печени небольшие и требуется максимальное сохранение паренхимы органа.
Делают клюшкообразный разрез брюшной стенки с пересечением правой прямой мышцы живота на уровне пупка. Пересекают треугольные и серповидную связки печени. На уровне общего желчного протока выделяют элементы печеночно-дуоденальной связки. Пересекают и перевязывают пузырные проток и артерию. Выделяют правые ветви собственной печеночной артерии и воротной вены, правый печеночный проток. По ходу указанных сосудов и протока поэтапно рассекают паренхиму печени до тех пор, пока не станет видимым место деления их на сосуды и желчные протоки, идущие к V—VIII и к VI, VII сегментам. Пересекают и лигируют сосуды и желчный проток, идущие к V и VIII сегментам.
Затем поэтапно рассекают паренхиму печени по ходу левых долевых сосудов и желчного протока до места отхождения сосудов и протока IV сегмента. Последние пересекают и перевязывают.
В поддиафрагмальном пространстве выделяют надпеченочный сегмент нижней полой вены и среднюю печеночную вену. Последнюю пересекают и
перевязывают. Пораженный участок печени иссекают. Вверху левая линия рассечения паренхимы печени проходит по правому краю серповидной связки, правая — от правого угла печени у средней печеночной вены. Плоскости разрезов сходятся в направлении к нижней полой вене. Ориентиром служит изменение окраски паренхимы печени в участках, не снабжаемых кровью после перевязки сосудов. Большую осторожность необходимо соблюдать при иссечении печени вблизи устья средней печеночной и нижней полой вен. В этом месте на небольшом протяжении находятся также устья правых и левой печеночных вен. Чтобы избежать их повреждения, обычно оставляют небольшую полоску паренхимы печени непосредственно над нижней полой веной. Культи сосудов и желчных протоков по раневой поверхности перевязывают, а затем сшивают между собой оставшиеся культи паренхимы. В подпеченочное и поддиафрагмальное пространства подводят 2—3 перчаточно-трубчатых дренажа через контрапертуру в правом подреберье.
Аномалии деления сосудов и желчных протоков в области ворот печени могут создавать затруднения при определении принадлежности их к определенному сегменту. Запомнить все возможные варианты строения ворот печени трудно. Поэтому мы считаем необходимым при определении сосуда или желчного протока выделять их до уровня развилки. В тех случаях, когда развилка имеет вид бифуркации, сомнений в анатомо-топографических взаимоотношениях не возникает. Если развилка имеет вид трифуркации или даже квадрифуркации, следует предполагать аномалию деления. В таком случае мы раздельно выделяем и берем на турникеты те сосуды или желчные протоки, которые могут быть связаны с удаляемым сегментом печени. Иногда временное пережатие турникета вызывает изменение кровоснабжения; соответственно изменяется окраска сегмента печени. Если окраска различных участков паренхимы одинаковая, мы используем фиссуральную методику резекции печени. После разделения паренхимы по проекционным линиям облегчается идентификация сегментарных сосудов и желчных протоков.
Резекция печени у детей требует тщательного гемостаза, поскольку потеря 500—1000 мл крови (в зависимости от массы тела) может вызвать необратимый шок (J. G. Randolph и соавт., 1978). В то же время большие регенераторные возможности печени позволяют выполнить у детей значительно большую резекцию органа.
Злокачественные новообразования печени у детей сравнительно поздно метастазируют, вследствие чего частота резекций у них больше, чем у взрослых,— 19—50 % (Л. А. Дурнов, Ю. В. Пашков, 1978).
Временное пережатие печеночно-дуоденальной связки используют для уменьшения кровопотери во время резекции печени. Для кратковременного пережатия связки вводят 4 пальца в сальниковое отверстие, а сверху сдавливают связку большим пальцем. Однако длительное пальцевое пережатие связки трудно выполнимо и, кроме того, ограничивает возможность манипуляций хирурга и ассистента. Поэтому непосредственно после пальцевого пережатия на печеночно-дуоденальную связку накладывают турникет. Обычно используют катетер диаметром 4—6 мм, который дважды проводят вокруг связки, а концы захватывают зажимом. Даже при незначительном подтягивании зажима происходит тугое пережатие связки.
Date: 2015-09-18; view: 856; Нарушение авторских прав