
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Кислоти
|
|
Кислоти – з позиції теорії електролітичної дисоціації це складні речовини, які у водних розчинах дисоціюють тільки на катіони гідрогену і аніони кислотного залишку.
HCl → H+ + Cl-
H2SO4→ H++HSO 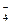
HSO 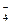 → H++ SO
→ H++ SO 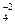
Кислоти бувають кисневовмісні (HNO3, H2SO4, H3PO4) і безкисневі (HCl, HBr, H2S).
По кількості атомів гідрогену в кислоті вони бувають одно-, двох-, трьох- і багатоосновні. Наприклад: HCl – одноосновна, H2SO4 – двохосновна, H3PO4 – трьохосновна.
Назва кисневовмісних кислот залежить від елементу, який утворює цю кислоту з додатком закінчення – на, коли ступінь окислення елемента відповідає номеру групи в періодичній системі H2SO4 – сірчана кислота, HNO3 - нітратна.
По мірі зниження ступеня окислення суфікси змінюються у слідуючому порядку: - вата, - иста, - ватиста. Наприклад: HClO4 – хлорна кислота, HClO3 – хлорновата кислота, HClO2 – хлориста кислота, HСlO – хлорноватиста кислота.
Коли елемент в одній і тій же ступені окислення утворює декілька кисневовмісних кислот, то до назви кислоти з меншим числом кисневих атомів добавляють приставку мета, з більшим – орто. HPO3 – метафосфорна кислота, H3PO4 - ортофосфорна кислота.
Назва безкисневмісних кислот залежить від назви елемента, який утворює цю кислоту з додаванням закінчення “о” і додаванням слова “воднева”. HCl – хлорводнева, або соляна кислота, HBr - бромводнева.
Добування:
1. Взаємодією ангідридів з водою:
SO3 + H2O = H2SO4
2. Дією на неметали сильних окисників:
3P + 5HNO3 + 2H2O = 3H3PO4 + 5NO
3. Прямим синтезом з простих речовин:
H2 + Cl2 = 2HCl
4. Реакцією обміну між сіллю і менш леткою кислотою:
NaCl + H2SO4 = NaHSO4 + HCl
Хімічні властивості
1. З основами:
H2SO4 + 2NaOH = Na2SO4 + 2H2O
2. З металами:
Zn + 2HCl = ZnCl2 + H2
3. З солями:
H2SO4 + BaCl2 = BaSO4 + 2HCl
Date: 2015-09-02; view: 487; Нарушение авторских прав