
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Основные свойства сил Ван-дер-Ваальса
|
|
1) Силы Ван-дер-Ваальса не связаны с переносом заряда и поэтому не относятся к химическим связям. Они обусловлены, в основном, диполь-дипольным взаимодействием нейтральных атомов и молекул и убывают с расстоянием как - 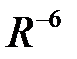 .
.
2) Ориентационное взаимодействие возникает между полярными молекулами, а индукционное - между полярными и неполярными. Эти типы взаимодействия хорошо описываются в рамках классической электростатики.
3) Дисперсионные силы или силы Лондона имеют квантовую природу и обусловлены понижением энергии нулевых колебаний электронных оболочек атомов и имеют универсальный характер.
4) Потенциал парного взаимодействия для сил Ван-дер-Ваальса аппроксимируется потенциалом Леннарда-Джонса: 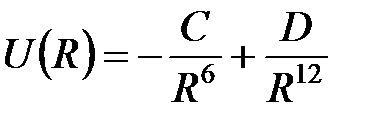 .
.
5) Силы Казимира-Польдера действуют на расстоянии между молекулами 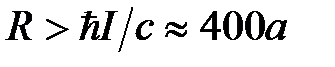 и обусловлены диполь-диподьным взаимодействием молекул с учетом волнового характера излучаемых ими электромагнитных полей.
и обусловлены диполь-диподьным взаимодействием молекул с учетом волнового характера излучаемых ими электромагнитных полей.
6) Силы Ван-дер-Ваальса ответственны за дисперсию света в прозрачных телах, за конденсацию газов, вязкость жидкостей, сухое трение поверхностей твердых тел и пр.
Date: 2015-05-19; view: 879; Нарушение авторских прав