
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Комплекс ионының зарядын анықтау
|
|
Молекулалардың электробейтараптығын ескере отырып, комплекс ионының зарядын екі әдіспен анықтайды:
а) сыртқы сфера бойынша.
ә) ішкі сфера бойынша
а) сыртқы сфера бойынша анықтағанда, комплекс ионының заряды
қарама-қарсы таңбамен алынған сыртқы сфера зарядына тең
[Co(NH3)6]+3Cl3¯
ә) ішкі сфера бойынша, комплекс ионының заряды құрамындағы
бөлшектердің зарядтарының алгебралық қосындысына тең
[Co+3(NH3)60]+3 +3·1 + 0·6= +3
Комплексті қосылыстардың изомериясы.
Комплексті қосылыстардың көп түрлілігі әр түрлі изомерлерінің болуымен түсіндіріледі.
1. Гидратты изомерия, су лигандаларының ішкі сферадан сыртқы сфераға өтуімен түзіледі.
[Cr(H2O)6]Cl3 изомері: [Cr(H2O)5Cl]Cl2·H2O
ашық жасыл түсті
[Cr(OH)4Cl2]Cl·2H2O
қара жасыл түсті
2. Координациялық изомерия, комплекс ішіндегі екі комплекс түзушілердегі
лигандалардың әр түрлі орналасуына байланысты
[Co+3(NH3)6]3+·[Cr+3(C2O4)32]3 және [Cr+3(NH3)6]3+·[Cо+3(C2O4)32]3
гексааминкобальт (ІІІ) триоксалатхроматы (ІІІ)
гексааминхром (ІІІ) триоксалатокобальты (ІІІ).
3. Цис- транс- изомерия, бірдей лигандалардың орталық атомның бір жағына және қарама-қарсы жағына орналасуына байланысты, егер лигандалар орталық атомның бір жағына орналасса цис- изомер деп аталады.
Егер бірдей лигандалар орталық атомның екі жағына орналасса, бір-бірінен диагональ бойында алыс жатса транс - изомер болады. Изомерлердің цис, транс- түрлері жазық квадрат және октаэдр құрылысты комплекске тән.
4. Ионизациялық изомерия, ішкі және сыртқы сфераларда иондардың әр түрлі орналасуына байланысты;
[Pt(NH3)3Br]·NO2 [Pt(NH3)3NO2]Br
5. Оптикалық молекулаға кіретін атомдардың немесе атомдар топтарының кеңістікте әр түрлі орналасуына байланысты.
Мұндай изомерлі заттардың оптикалық активтігі ішкі симметрия жазықтығының болмауымен түсіндіріледі. Комплексті қосылыстардың түзілуін және қасиеттерін валенттілік байланыстар әдісі, кристалдық өріс теориясы және молекулалық орбиталь әдісі түсіндіреді.
Комплексті қосылыстардың номенклатурасы
Комплексті қосылыстардың атаулары ұзақ уақыт бойы Вернердің номенклатурасы бойынша аталып келді. Тек 1962 жылдан бастап Химиктердің Халықаралық одағы (IUPAC) ұсынған жаңа номенклатура қолданылады.
Осы ережеге сәйкес:
1) қосылыстың катионы, содан соң анионы аталады;
2) комплекс ионын, яғни ішкі сфераны тұтас жазады;
3) электробейтарап комплекс бір сөзбен аталады;
4) комплекс ионды атағанда ең алдымен координациялық саны көрсетіліп, лигандалар аталады, ал содан кейін орталық атом аталып, дөңгелек жақша ішіне рим сандарымен тотығу дәрежесі көрсетіледі;
5) комплекс ион-анион болса, орталық атом атауына “ат” жұрнағы қосылады;
6) бейтарап лигандалар молекула атауымен аталады, тек келесі қосылыстардың атаулары өзгешелеу болады:
NH3 -аммин
H2O -аква
Сонымен қатар, металл атомымен тікелей байланысқан NO, CO
топтары нитрозил, карбонил деп аталады.
Тотығу дәрежелерін есептегенде бұл лигандалар бейтарап
молекулалар деп қарастырылады.
7) анион – лигандаларына “о” жұрнағы қосылып аталады. Мысалы: CN- -циано, Cl- -хлоро, NO2- -нитро, NO3 --нитрато, OH¯-гидроксо, F¯ -фторо, Br- -бромо, СО32¯ -карбонато, РО43- -фосфато, SO42 -сульфато,SO32 -сульфито, C2O42 -оксалато.
8) ең алдымен анион лигандалар, содан кейін бейтарап лигандалар аталады.
9) координациялық сан грек сандарымен лигандалар атының алдына қойылады (бір- моно, оны жазбаса да болады, екі-ди, үш-три, төрт-тетра, бес- пента, алты- гекса, жеті- гепта, сегіз- окта т.б.)
Мысалы: [Co(NH3)6]Cl3 -гексаамминкобальт (III) хлориді
[Co(NH3)5H2O]Cl2 -аквапентаамминкобальт (III) хлориді
Na2[PtCl2(CN)4] натрийдің дихлоротетрациано платинаты(IV)
[Co(H2O)(NH3)3Cl2] Cl акватриамминдихлорокобальт(III)хлориді.
Комплексті қосылыстардың тұрақтылығы.
Ішкі сферамен сыртқы сфераның тұрақтылығы бойынша бір-бірінен көп айырмашылығы бар. Сыртқы сферадағы бөлшектер комплекс ионымен электростатикалық күшпен байланысады және ерітіндіде тез үзіледі де, күшті электролиттер сияқты диссоциацияланады.
І саты Ag(NH3)2]Cl→[Ag(NH3)2]++Cl¯. Бұл І-ші ретті диссоциация деп аталады.
Ішкі сферадағы лигандалар орталық атоммен берігірек байланысқан, сондықтан аздап ыдырайды. Комплексті қосылыстар ішкі сферасының диссоциациялануы қайтымды және сатылап жүреді. Оны ІІ-ші ретті диссоциация деп атайды.
ІІ-ші саты [Ag(NH3)2]+↔Ag++2NH3.
ІІ-ші ретті диссоциация комплексті бөлшек, орталық атом және лиганда арасындағы орнайтын тепе-теңдік бойынша сипатталады. Мұны келесі реакция бойынша түсіндіруге болады. Егер ертіндіге Cl¯ ионы бар ерітіндісімен әрекеттестірсек, онда тұнба түзілмейді, яғни AgCl↓ тұнбасы түзілмейді. Аммиак ертіндісіндегі Ag+ ионының концентрациясы аз, ал ЕКAgCl = 1,8· 1010 тең болады.
Ал егер комплекс ертіндісіне KI қоссақ, AgI↓ тұнбасы түзіледі. Бұл ерітіндіде Ag+ ионының бар екендігін көрсетеді. Ag+ ионының концентрациясы аз болғанмен, AgI↓ тұнбасын түзуге жеткілікті, ЕКAgI =1·1016, AgCl ерігіштік көбейтіндісінен біршама аз. Одан басқа H2S қоссақ Ag2S тұнбасы түзіледі, себебі ЕКAg2S = 1051 яғни
[Ag(NH3)2]+ + I¯↔AgI↓ + 2NH3
2[Ag(NH3)2]+ + H2S ↔Ag2S↓+ 2NH3 + 2NH4+
[Ag(NH3)2]+ ионының диссоциациясы әлсіз электролит диссоциациясы сияқты, массалар әсер заңына бағынады да тұрақсыздық константасы деп аталатын тепе- теңдік константасымен сипатталады.
Ктұрақсыздық = [Ag+] [NH3]2/ [Ag(NH3)2]+ = 6,8·108
Комплекс иондардың тұрақсыздық константасы әр түрлі, ол комплекстің тұрақтылығын көрсететін өлшемі. Егер ыдырау өнімінің концентрациясы аз болса, комплекс тұрақты болады да, тұрақсыздық константасының мәні кіші болып келеді.
[Ag(NО2)2] [Ag(NH3)2]+ [Ag(S2O3)2]3 [Ag(СN)2]
Ктұрақсыздық 1,3·103 6,8·108 1·1013 1·1021
тұрақтылығы солдан оңға қарай артады.
Соңғы кезде комплексті қосылыстардың тұрақтылығын сипаттайтын шама ретінде тұрақсыздық константасына қарама- қарсы шама Ктұр= 1/Ктұрақсыздық тұрақтылық константасы қолданылады. [Ag(NH3)2]+ ионының Ктұр = 1/Ктұрақсыз = [Ag(NH3)2]+ / [Ag+][NH3]2
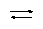 Осы уақытқа дейін комплекстің соңғы өнімдерінің ыдырауы бойынша жалпы тұрақсыздық және тұрақты константалары қарастырылды. Ал шын мәнінде комплекстің диссоциациясы сатылы әлсіз электролиттер диссоциациясы сияқты өтеді. Мысалы, көп негізді қышқылдарға ұқсас.
Осы уақытқа дейін комплекстің соңғы өнімдерінің ыдырауы бойынша жалпы тұрақсыздық және тұрақты константалары қарастырылды. Ал шын мәнінде комплекстің диссоциациясы сатылы әлсіз электролиттер диссоциациясы сияқты өтеді. Мысалы, көп негізді қышқылдарға ұқсас.
K2[PtCl4] 2K+ + [PtCl4]2
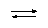 К4
К4
[PtCl4]2+H2O [PtCl3·H2O]¯ + Cl¯
Яғни, комплекс ионының бос координациялық орнын су молекуласы басады. Сондықтан комплекс ионының диссоциациясын орын басу реакциясы деп қарастырады.
К3
 [PtCl3·H2O]+H2O [PtCl2·(H2O)2] + Cl¯
[PtCl3·H2O]+H2O [PtCl2·(H2O)2] + Cl¯
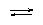 К2
К2
[PtCl2·(H2O)2] +H2O [Pt·(H2O)3Cl]+ + Cl¯
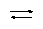 К1
К1
[Pt·(H2O)3Cl]+ [Pt·(H2O)4]+2 + Cl¯
Cl¯ ионының бөлінуіне байланысты комплекс заряды оң зарядтала береді, ал Cl¯ионы саны комплексте азаяды. Бірақ әрі қарай Cl¯ ионының үзіліп шығуы қиындайды. Сондықтан тұрақсыздық константасы мәні мынадай қатынаспен беріледі:
К 4 >K3 >K2 >K1
Ктұрақсыздық =K1·K2·K3·K4 көбейтіндісіне тең.
Ктұрақтылық және Ктұрақсыздық мәндері бойынша комплексті қосылыстар арасындағы реакцияларының өту жағдайын айтып беруге болады.
Мысалы:[Ag(NH3)2]++2H+ ↔ Ag++2NH4+
Тұрақтылық константасының мәндерінің айырмашылығы көп болса, реакция бағыты тұрақтылық константасының мәні көп жағына, яғни комплекс түзілу жағына жүреді, ал егер тұрақсыздық константасы мәнінің аса көп айырмашылық жоқ болса, онда реакция бағыты мәні аз жағына жүреді.
Ктұрақсыздық[Ag(NH3)2]+=6,8·108
Ктұрақсыздық [NH4+]=5,4·1010
қышқыл әсерінен күміс аммиакты иондарға ыдырау бағытында жүреді.
Date: 2015-11-13; view: 2620; Нарушение авторских прав