
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Задача 449
|
|
Исходя из величин стандартных электродных потенциалов рассчитать константу равновесия реакции, протекающей в гальваническом элементе:
Cu + 2AgNO3 ® Cu(NO3)2 + 2Ag.
Решение:
По ряду напряжений находим, 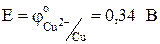 ,а
,а 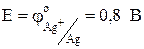 . Отсюда следует, что медный электрод будет отрицательным, т.е. анодом:
. Отсюда следует, что медный электрод будет отрицательным, т.е. анодом:
(-) Cu½Cu2+ ½½Ag+½Ag (+).

Между константой равновесия реакции, протекающей в гальваническом элементе, и э.д.с. элемента существует зависимость
 , откуда
, откуда 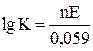 .
.
Вычислим константу равновесия реакции:
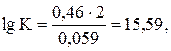 K = 3,8∙1015.
K = 3,8∙1015.
Сопоставляя электродные потенциалы, можно заранее определить направление, в котором будет протекать окислительно-восстановительная реакция. Поскольку
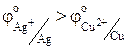 ,
,
то окислителем будет служить ион серебра, а восстановителем – медь: рассматриваемая реакция будет протекать слева направо. По величине константы равновесия (К=3,8 ×1015) судим о сдвиге равновесия реакции в сторону продуктов реакции. Число 1015 означает, что равновесие в данной системе наступит тогда, когда произведение концентрации ионов исходных продуктов будет в 1015 раз меньше произведения концентраций ионов конечных продуктов.
Date: 2015-09-24; view: 436; Нарушение авторских прав