
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Задача 399
|
|
Составить схему, написать уравнения электродных процессов и рассчитать э.д.с. элемента, состоящего из цинковой и никелевой пластин, опущенных в растворы сернокислых солей с концентрацией 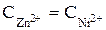 = 0,01 моль/л.
= 0,01 моль/л.
Решение:
В ряду напряжений Zn стоит левее Ni, поэтому в гальваническом элементе отрицательным (анодом) будет цинковый электрод, а положительным (катодом) - никелевый.
Схема гальванического элемента
(-) Zn½ZnSO4½½NiSO4½Ni (+).
При работе элемента протекают реакции:
на аноде Zn ® Zn2+ + 2e,
на катоде Ni2+ + 2e ® Ni.
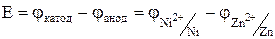
Электродные потенциалы необходимо вычислить по уравнению Нернста:
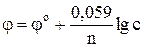 .
.
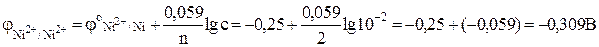
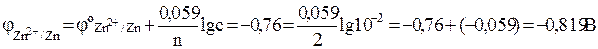 Отсюда Е = -0,309 - (-0,819) = 0,51 В.
Отсюда Е = -0,309 - (-0,819) = 0,51 В.
С учетом того, что число электронов, переносимых во время электрохимической реакции металлами, одинаково и концентрации растворов равны, уравнение упрощается и принимает вид
 ;
; 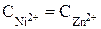 ;
;
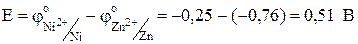 .
.
Гальванический элемент может быть составлен не только из различных, но и из одинаковых электродов, погруженных в растворы одного и того же электролита, различающиеся только концентрацией (концентрационные гальванические элементы). Э.д.с. такого элемента также равна разности потенциалов составляющих его электродов.
Электрод, погруженный в более концентрированный раствор, положителен по отношению к другому, который погружен в более разбавленный раствор.
Задача 406
Вычислить электродвижущую силу концентрационного элемента:
Cu½CuCrO4 (C1=0,01 моль/л) ½½ CuCrO4 (C2=0,1 моль/л)½Cu.
Решение:
Рассчитаем э.д.с. по уравнению:
 .
.
Элемент будет действовать до тех пор, пока не выравнится концентрация ионов у обоих электродов.
Date: 2015-09-24; view: 550; Нарушение авторских прав