
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Характеристика окислительно-восстановительных ферментов. Их роль при переработке и хранении растительного сырья.
|
|
При переработке пищевого растительного сырья заслуживают внимания некоторые представители окислительно-восстановительных ферментов - полифенолоксидаза и липоксигеназа.
Полифенолоксидаза (1.10.3.1) относится к аэробным дегидрогеназам. для которых акцептором водорола может служить лишь кислород воздуха. Отнимая водород, от окисляемого субстрата и передавая его затем кислород} возлуха. полифенолоксидаза может образовать при этом воду.
Полифенолоксидаза содержится в грибах и высших растениях. Этот фермент представляет собой белок, содержащий медь (0.2 - 0.3 %). Примером катализируемой им реакции окисления полифенола может служить окисление пирокатехина в соответствующий хинон:

Полифенолоксидаза окисляет также трифенолы, например пирогаллол. Действием этого фермента объясняется потемнение поверхности разрезанного яблока или картофельного клубня, а также потемнение плодов и овощей при сушке. Полифенолоксидаза участвует в окислении полифенолов и дубильных веществ, происходящем при скручивании и завяливании чайного листа. Полифенолоксидаза (тирозиназа 1.14.18.1) может также окислять тирозин с образованием темноокрашенных соединений меланинов (фенольные полимеры, строение которых до конца не выяснено).

Липоксигеназя (липоксидаза) (1.13.11.12) также относится к оксндазам. Широко распространена в растениях. Катализирует окисление кислородом воздуха некоторых ненасыщенных высокомолекулярных жирных кислот и образуемых ими сложных эфиров.
Наиболее активна липоксигеназа в семенах сои. Оптимум действия липоксигеназы злаков находится при рН 7.0.
Из всех ненасыщенных жирных кислот липоксигеназа окисляет с достаточной скоростью лишь линолевую и линоленовую кислоты.
Окисление ненасыщенных жирных кислот под действием липоксигеназы приводит к образованию гидроперекисей:

Образующиеся таким образом гидроперекиси имеют высокую окислительную способность и могут окислять далее ншые порции ненасыщенных жирных кислот, а также каротиноиды, витамин А, аминокислоты, хлорофилл, аскорбиновую кислоту. Липоксигеназа играет важную роль при разрушении каротина во время сушки и хранения различных растительных продуктов. Перекиси жирных кислот могут легко подвергаться дальнейшему распаду, по этой причине липоксигеназа играет, по-видимому, существенную роль в процессе прогоркания таких продуктов, как мука и различные крупы.
Важной оке и дазой является глюкозооксидаза (1.1.3.4.), содержащаяся в различных плесневых грибах и окисляющая глюкозу с образованием а конечном счете глюконовой кислоты. Фермент действует на СНОН - группу глюкозы. При отщеплении водорода его акцептором служит газообразный кислород.
Каталаза (1. 11.1.6) относится к классу окендоредуктаз, под действием которого происходит разложение перокеща водорода на воду и молекулярный кислород: 2Н1О2 -* 2Н2О + О2.
Каталаза - двухкомпонентный фермент, состоящий из белка и соединенной с ним простетической группой содержащей гематин.
Класс гидролиз весьма обширен, и его подразделяют на ряд подгрупп.
Эстеразы - ферменты, катализирующие реакции расщепления и синтеза сложных эфиров в соответствии с уравнением
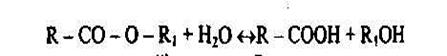
гле К - остаток органической (или неорганической) кислоты. К, - остаток спирта или фенола. Карбогидразы - ферменты, катализирующие реакции типа

где R - остаток моно-, ди- или полисахарида, R  может быть также моно-, ди- или полисахаридом или же веществом неуглеводной природы, содержащим спиртовую или фенольную группу (например, агликоны в гликозидах). Кислородная связь в веществах, расщепляемых карбогидразами, имеет характер ацетильной или эфирной связи.
может быть также моно-, ди- или полисахаридом или же веществом неуглеводной природы, содержащим спиртовую или фенольную группу (например, агликоны в гликозидах). Кислородная связь в веществах, расщепляемых карбогидразами, имеет характер ацетильной или эфирной связи.
Протеазы - ферменты катализирующие растепление белка и полипептидов:
 RСОNНR’ + Н2О RСООН + Н3NR’
RСОNНR’ + Н2О RСООН + Н3NR’
где R и R' - остатки аминокислот, ди- или полипептидов.
Date: 2016-07-25; view: 538; Нарушение авторских прав