
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Патогенез инфекций мочевых 3 page
|
|
Глава 14. Бактериальные инфекции мочевых путей и половых органов
 которая встречается преимущественно у женщин среднего и пожилого возраста. Заболевание опасно из-за обширности повреждения почечной паренхимы. Ксан-тогранулематозный пиелонефрит развивается, как правило, на фоне гидронефроза, чаще всего при мочекаменной болезни. Этиология не известна, но, вероятно, обструкция мочевых путей, осложненная вторичной инфекцией, вызывает скопление ксантомных клеток — макрофагов, нагруженных липидами, — вокруг почечных чашечек и абсцессов в почечной паренхиме. Развивается гранулематозное воспаление, которое в итоге захватывает всю почечную паренхиму, может распространяться на околопочечную и забрюшинную клетчатку. При посеве гранулематозной ткани чаще всего выделяют Proteus mirabilis и Escherichia coli. При гистологическом исследовании в почечной паренхиме находят абсцессы, перемежающиеся с участками гранулема-тозного воспаления. Нужно отметить, что ксантомные клетки похожи на клетки светлоклеточногорака почки.
которая встречается преимущественно у женщин среднего и пожилого возраста. Заболевание опасно из-за обширности повреждения почечной паренхимы. Ксан-тогранулематозный пиелонефрит развивается, как правило, на фоне гидронефроза, чаще всего при мочекаменной болезни. Этиология не известна, но, вероятно, обструкция мочевых путей, осложненная вторичной инфекцией, вызывает скопление ксантомных клеток — макрофагов, нагруженных липидами, — вокруг почечных чашечек и абсцессов в почечной паренхиме. Развивается гранулематозное воспаление, которое в итоге захватывает всю почечную паренхиму, может распространяться на околопочечную и забрюшинную клетчатку. При посеве гранулематозной ткани чаще всего выделяют Proteus mirabilis и Escherichia coli. При гистологическом исследовании в почечной паренхиме находят абсцессы, перемежающиеся с участками гранулема-тозного воспаления. Нужно отметить, что ксантомные клетки похожи на клетки светлоклеточногорака почки.
Клиническая картина
Клиническая картина ксантогранулематозного пиелонефрита разнообразна. Чаще всего встречаются преходящая боль в пояснице (у 70—90% больных) и лихорадка с ознобами (у 45—70% больных). В 11—48% случаев пальпируется объемное образование в боковых отделах живота. При вовлечении в воспалительный процесс соседних структур появляются соответствующие симптомы. Описаны наружные свищи с обильным отделяемым и свищи, сообщающиеся с кишечником и суставными полостями.
Диагностика
Посев мочи выявляет бактериурию примерно у 70% больных. В общем анализе мочи обнаруживают протеи-нурию и лейкоцитурию. Самый надежный метод идентификации возбудителя — посев ткани, полученной при пункции почки. В общем анализе крови выявляют, как правило, анемию и лейкоцитоз. У 50—80% больных при биохимическом исследовании крови отмечаются признаки нарушений функции печени.
Наиболее информативный метод диагностики — КТ. Ее чувствительность достигает 90%. В почке визуализируются очаги пониженной плотности, представляющие собой участки инфильтрации ксантомными клетками, расширенные почечные чашечки и абсцессы (рис. 14.5). Нередко виден камень, окруженный сморщенной почечной лоханкой. Почечная паренхима вокруг очагов контрастируется слабо. КТ позволяет выявить также распространение воспалительного инфильтрата на соседние структуры — мышцы, селезенку, толстую кишку, крупные сосуды.
Другие методы уступают КТ по чувствительности. При экскреторной урографии можно выявить увеличение и камни почки, замедленное выведение рентгено-контрастного средства, объемное образование в проекции почки и деформацию почечных чашечек. При УЗИ
визуализируются увеличение и камни почки. Расширенная чашечно-лоханочная система часто заполнена неоднородным содержимым, что заставляет думать о пионефрозе.
Лечение
Лечение хирургическое. Выполняют нефрэктомию с резекцией или удалением пораженных соседних органов. При ограниченном поражении почки достаточно ее резекции. Однако сообщения о сочетании ксантогранулематозного пиелонефрита и различных злокачественных опухолей почки и почечной лоханки заставляют некоторых авторов рекомендовать нефрэктомию всем больным с этой патологией. Дренирование не излечивает больных и может способствовать развитию наружного свища, осложняющего последующую нефрэктомию.
МАЛАКОПЛАКИЯ
Малакоплакия — редкая гранулематозная болезнь, для которой характерно образование узлов различного размера преимущественно на слизистой мочевых путей. Узлы представляют собой скопления макрофагов и плазматических клеток. В макрофагах имеются пластинчатые включения — тельца Михаэлиса—Гутманна — патогно-моничный признак заболевания. Вероятно, эти тельца представляют собой фаголизосомы, содержащие частично переваренные бактерии, на которых осаждаются гидроксиапатит и соли железа. Причина гранулематоз-ного процесса при малакоплакии, по-видимому, — незавершенный фагоцитоз, как предполагается, из-за дефицита внутриклеточного цГМФ. Очевидна связь между малакоплакией и хронической инфекцией мочевых путей: у 90% больных при посеве мочи выделяют грамот -рицательных представителей кишечной микрофлоры, чаще всего Escherichia coli.
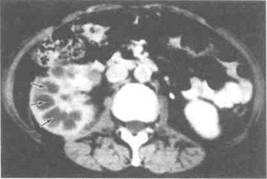
Рисунок 14.5. КТ с контрастированием при ксантогранулема-тозном пиелонефрите. В центре правой почки видны множественные участки пониженной плотности (показаны стрелками), представляющие собой скопления ксантомных клеток.
Глава 14. Бактериальные инфекции мочевых путей и половых органов

 Малакоплакия, как и инфекции мочевых путей, чаще наблюдается у женщин. Большинство больных старше 50 лет. Нередко одновременно наблюдаются другие тяжелые хронические заболевания. Хотя узлы могут появляться в разных органах, у 75% больных поражаются мочевые пути: из них у 70% — мочевой пузырь, у 15% — верхние мочевые пути, еще у 15% — и верхние, и нижние мочевые пути. Клиническая картина определяется локализацией узлов. Поражение мочевого пузыря проявляется гематурией, учащенным, болезненным мочеиспусканием и императивными позывами. При поражении почки возникает схваткообразная боль в пояснице и лихорадка, а в боковых отделах живота может пальпироваться объемное образование. Примерно у 50% больных наблюдается двустороннее поражение почек, при этом развивается ХПН. Вообще малакоплакия часто напоминает другие, более распространенные инфекции мочевых путей, а также злокачественные опухоли мочевых путей и половых органов.
Малакоплакия, как и инфекции мочевых путей, чаще наблюдается у женщин. Большинство больных старше 50 лет. Нередко одновременно наблюдаются другие тяжелые хронические заболевания. Хотя узлы могут появляться в разных органах, у 75% больных поражаются мочевые пути: из них у 70% — мочевой пузырь, у 15% — верхние мочевые пути, еще у 15% — и верхние, и нижние мочевые пути. Клиническая картина определяется локализацией узлов. Поражение мочевого пузыря проявляется гематурией, учащенным, болезненным мочеиспусканием и императивными позывами. При поражении почки возникает схваткообразная боль в пояснице и лихорадка, а в боковых отделах живота может пальпироваться объемное образование. Примерно у 50% больных наблюдается двустороннее поражение почек, при этом развивается ХПН. Вообще малакоплакия часто напоминает другие, более распространенные инфекции мочевых путей, а также злокачественные опухоли мочевых путей и половых органов.
У больных с симптомами раздражения мочевого пузыря при цистоскопии на слизистой обычно обнаруживают бляшки и узлы разного размера. По мере прогрес-сирования они разрастаются и становятся похожими на цветную капусту. На этой стадии при экскреторной урографии определяются дефекты наполнения. Узлы могут вызывать обструкцию мочеточника и гидронефроз. Многоочаговое поражение почки при УЗИ визуализируется как общая гиперэхогенность почечной паренхимы на фоне увеличения органа, при КТ — как множественные очаги пониженной плотности или диффузные изменения. При КТ может определяться также поражение соседних органов. При ангиографии визуализируются скудно васкуляризованные объемные образования с большим числом сосудов по периферии.
Эффективность антимикробных средств при малако-плакии зависит от их способности создавать высокую внутриклеточную концентрацию. Таким свойством обладают ТМП/СМК и фторхинолоны. В макрофаги хорошо проникает ципрофлоксацин, при этом его внутриклеточная концентрация в 2—3 раза выше внеклеточной, что делает его препаратом выбора при малакоплакии. Для стимуляции фагоцитоза применяют бетанехол и аскорбиновую кислоту, хотя их эффективность не доказана. При поражении только нижних мочевых путей достаточно медикаментозного лечения, при поражении почки и мочеточника помимо антимикробной терапии проводят нефроуретерэктомию. При двустороннем поражении почек прогноз неблагоприятный, продолжительность жизни, как правило, не превышает 6 мес.
ОСТРЫЙ ЦИСТИТ Этиология и патогенез
Первичным острым циститом чаще болеют женщины. По определению, это заболевание возникает в отсутствие органических или функциональных изменений мо-
чевых путей. Возбудитель чаще всего проникает в мочевой пузырь восходящим путем из прямой кишки на промежность, а затем в мочеиспускательный канал. У мужчин риск восходящей инфекции мочевого пузыря ниже благодаря бактерицидным свойствам секрета предстательной железы. По данным разных авторов, почти в 80% случаев возбудитель острого цистита у женщин -Escherichia coli. Из грамположительных бактерий острый цистит вызывают только Staphylococcus saprophy-ticus и энтерококки. В редких случаях из мочи выделяют Klebsiella spp. и Proteus spp.
Клиническая картина
Характерны симптомы раздражения мочевого пузыря — учащенное болезненное мочеиспускание и императивные позывы. Нередко наблюдается боль в области крестца и надлобковой области. В отдельных случаях возможны гематурия, а также мутная и зловонная моча. Лихорадка и другие общие симптомы у взрослых, как правило, отсутствуют. При физикальном исследовании специфичных симптомов нет. Возможна только болезненность при пальпации надлобковой области.
Диагностика
В общем анализе мочи обнаруживают лейкоцитурию, бактериурию и реже гематурию. Бактериурию и лейкоцитурию можно выявить с помощью тест-полосок для определения нитритов и лейкоцитарной эстеразы соответственно, однако для подтверждения диагноза и определения вида возбудителя в большинстве случаев необходим посев мочи. Он необязателен у взрослых, если нет сомнений в первичном характере инфекции. По данным некоторых авторов, в очевидных случаях посев мочи лишь увеличивает стоимость обследования, не давая какой-либо дополнительной информации, поскольку возбудители острого цистита хорошо известны. У детей, при атипичном течении, недавней антимикробной терапии и инфекции мочевых путей в анамнезе посев мочи проводят обязательно, поскольку необходимо определить чувствительность возбудителя к антимикробным средствам. Другие исследования при первичном остром цистите у женщин обычно не требуются.
Лечение
Для лечения первичного острого цистита подходит любое антимикробное средство, создающее высокую концентрацию в моче. В отношении большинства возбудителей активен ТМП/СМК. При аллергии к сульфаниламидам применяют триметоприм. Он не менее эффективен, чем комбинированный препарат. Нит-рофурантоин тоже эффективен и безопасен, однако он дороже ТМП/СМК. Устойчивость к нитрофуран-тоину вырабатывается редко, поэтому он особенно показан больным, неоднократно получавшим антимик-
Глава 14. Бактериальные инфекции мочевых путей и половых органов
 робную терапию, у которых высок риск устойчивости возбудителя к антимикробным средствам. Однако обычно нитрофурантоин оставляют на тот случай, когда необходима длительная антимикробная профилактика. Устойчивость к ампициллину и амоксициллину встречается чаще, чем к ТМ П/СМК. Против уропатогенных бактерий очень эффективны фторхинолоны, но это дорогие препараты.
робную терапию, у которых высок риск устойчивости возбудителя к антимикробным средствам. Однако обычно нитрофурантоин оставляют на тот случай, когда необходима длительная антимикробная профилактика. Устойчивость к ампициллину и амоксициллину встречается чаще, чем к ТМ П/СМК. Против уропатогенных бактерий очень эффективны фторхинолоны, но это дорогие препараты.
Были проанализированы результаты 28 клинических испытаний разных схем антимикробной терапии первичного острого цистита у женщин. Показано, что лечение длительностью 3—5 сут и более эффективнее однократного приема антимикробных средств. Эти различия особенно заметны при применении р-лактамных антибиотиков и менее заметны при использовании ТМП/СМК. Однократный прием р-лактамных антибиотиков характеризуется очень низкой эффективностью. По-видимому, оптимальной следует считать антимикробную терапию длительностью 3 сут, поскольку при более длительном лечении значительно возрастает риск побочных действий.
РЕЦИДИВИРУЮЩИЕ ИНФЕКЦИИ МОЧЕВЫХ ПУТЕЙ
Этиология и патогенез
Рецидивирующие инфекции мочевых путей бывают возвратными и повторными. Их нужно различать, потому что от типа рецидивирующей инфекции мочевых путей зависит тактика лечения. Так, возвратная инфекция излечивается, как правило, после удаления источника, а при повторной основное внимание уделяют антимикробной профилактике. Хотя большинство повторных инфекций возникает в результате восходящего проникновения возбудителя из мочеиспускательного канала, их причиной могут быть и органические изменения мочевых путей, в частности пузырно-влагалищные и пу-зырно-кишечные свищи. Об этой причине рецидивирующих инфекций мочевых путей следует думать в первую очередь при наличии пневматурии или примеси кала в моче, при дивертикулите, операциях на органах малого таза и лучевой терапии на эту область в анамнезе. В таких случаях от повторных инфекций мочевых путей избавляет только хирургическое лечение.
Диагностика
При подозрении на возвратную инфекцию показано тщательное обследование. Предварительный диагноз позволяет поставить УЗИ мочевых путей и половых органов. При необходимости проводят цистоскопию и экскреторную урографию. В отдельных случаях требуются ретроградные рентгеноконтрастные исследования, например, чтобы выявить дивертикул мочевого пузыря или рефлюкс в культе мочеточника после нефрэктомии. Катетеризация мочеточников позволяет уточнить локализацию инфекции. При подозрении на простатит ис-
следуют секрет предстательной железы. Объем обследования при повторной инфекции мочевых путей зависит от предполагаемой причины. При подозрении на пузыр-но-влагалищный или пузырно-кишечный свищ проводят КГ, цистоскопию и рентгеноконтрастные исследования ЖКТ. Если предполагается восходящая инфекция и нет признаков пиелонефрита, бывает достаточно цистоскопии.
Лечение
Цель лечения возвратной инфекции мочевых путей — устранение ее источника. Основная причина — инфицированные мочевые камни, которые дробят с помощью дистанционной литотрипсии или удаляют эндоскопическим путем. При врожденных и приобретенных органических изменениях мочевых путей показано хирургическое лечение. Однако устранить источник инфекции можно не всегда, например при хроническом простатите. В таких случаях проводят поддерживающую антимикробную терапию, чтобы предотвратить рецидив инфекции мочевых путей. Для этого назначают антимикробные средства в низких дозах длительно. Чаще всего применяют ТМП/СМК, нитрофурантоин и фторхинолоны.
При повторной инфекции в отсутствие мочевых свищей прибегают к длительной антимикробной профилактике, которую начинают сразу после основного курса лечения и исчезновения бактериурии. Принципиальное различие между антимикробной профилактикой и поддерживающей антимикробной терапией заключается в следующем. Антимикробная профилактика направлена на поддержание стерильности мочи, а поддерживающая антимикробная терапия — на предупреждение попадания возбудителя из имеющегося очага инфекции. Быстрое исчезновение бактериурии после основного курса лечения повторной инфекции не устраняет необходимость в антимикробной профилактике. Ее схемы представлены в табл. 14.6. Антимикробную профилактику проводят, как правило, в течение 6 мес, регулярно выполняя посев мочи. Еще один вид антимикробной профилактики повторных инфекций мочевых путей — пост-коитальная профилактика. Она показана больным, у которых повторные инфекции возникают после половых сношений. Им рекомендуют однократно принимать одно из антимикробных средств, применяемых для
Таблица 14.6. Схемы антимикробной профилактики при рецидивирующих инфекциях мочевых путей
Нитрофурантоин, 50—100 мг/сут внутрь Макрокристаллический нитрофурантоин, 100 мг/сут внутрь ТМП/СМК, 40/200 мг/сут внутрь Цефалексин, 250 мг/сут внутрь Ципрофлоксацин, 250 мг/сут внутрь Триметоприм, 100 мг/сут внутрь
Глава 14. Бактериальные инфекции мочевых путей и половых органов
лечения инфекций мочевых путей, в стандартной дозе после каждого полового акта.
Существенный недостаток антимикробной профилактики — частое возникновение устойчивости микроорганизмов к антимикробным средствам. Чтобы избежать этого, некоторые авторы вместо антимикробной профилактики рекомендуют больным пить клюквенный сок, применять влагалищные свечи или крем с эс-триолом либо влагалищные свечи с Lactobacillus spp. Продолжается разработка вакцин для профилактики инфекций мочевых путей, так как in vitro антитела к Escherichia coli ингибируют прикрепление бактерий к клеткам эпителия мочевых путей, полученным из мочевого осадка. Клиническое испытание влагалищных свечей, содержащих 10 самых распространенных уропато-генных штаммов Escherichia coli, инактивированных нагреванием, показало, что они увеличивают безрецидивный период с 8,7 до 13нед. Вероятно, эти свечи снижают восприимчивость влагалищного эпителия к бактериальному обсеменению. Разрабатываются и субъединичные вакцины на основе фимбрий бактерий. Теоретически, эти вакцины должны стимулировать выработку антител к фимбриям, предотвращая обсеменение слизистой и последующую инфекцию мочевых путей. Такой эффект наблюдали в экспериментах после иммунизации животных адгезином FimH — основным компонентом фимбрий типа 1.
БАКТЕРИУРИЯ ВО ВРЕМЯ БЕРЕМЕННОСТИ
Во время беременности замедляется перистальтика мочеточников, у большинства женщин во второй половине беременности мочеточники расширяются, особенно правый. Это обусловлено, с одной стороны, сдавлением увеличенной маткой, с другой, снижением тонуса гладких мышц мочеточников под действием прогестерона. Во время беременности меняется и функция почек: значительно возрастают почечный плазмоток и СКФ (последняя на 30—50%). По этой причине уровни креати-нина сыворотки и АМК во время беременности ниже, чем вне ее. Кроме того, у беременных повышается экскреция белка с мочой. Органические и функциональные изменения мочевых путей повышают опасность бактериурии во время беременности. И хотя ее частота во время беременности не повышается, составляя, как и вне беременности, 3—9%, значительно возрастает риск острого пиелонефрита. Так, у небеременных бессимптомная бактериурия в отсутствие изменений мочевых путей приводит к острому пиелонефриту редко, а у беременных он развивается в 13,5—65% случаев. Лечение бессимптомной бактериурии во время беременности снижает риск острого пиелонефрита до 0—5,3%.
Профилактика острого пиелонефрита у беременных основана на регулярном обследовании. Посев мочи выполняют при первом обращении к врачу и на 16-й неделе беременности. Такая тактика позволяет выявить боль-
шинство женщин с высоким риском инфекции моче- I вых путей. Если диагностирована бактериурия, приме- I няют антимикробные средства. Во время беременности I можно применять далеко не все препараты. Безопасны- I ми считают пенициллины и цефалоспорины. При бес-симптомной бактериурии назначают трехдневный курс I лечения препаратом для приема внутрь, затем повторя- I ют посев мочи. Если бактериурия сохраняется или во- I зобновляется позже, антимикробные средства назнача-ют в низких дозах до конца беременности. При остром I пиелонефрите показана госпитализация. Антимикробные средства вводят парентерально. После излечения ввиду высокого риска рецидива пиелонефрита до конца беременности регулярно проводят посев мочи.
Без лечения острый пиелонефрит повышает риск преждевременных родов и гибели плода. Как влияет на плод своевременно выявленный и излеченный острый пиелонефрит, не установлено. По некоторым данным, лечение бессимптомной бактериурии и острого пиелонефрита во время беременности не влияет на ее исход. Другие авторы утверждают, что инфекции мочевых путей во время беременности повышает риск гибе- I ли плода и новорожденного более чем вдвое. Независи-мо от действия на плод острый пиелонефрит опасен I для беременной, поэтому антимикробная терапия обя- I зательна даже при бессимптомной бактериурии.
ПРОСТАТИТ
Простатит — очень распространенное заболевание. Согласно отчету Национального института здоровья США за 1990 г., мужчины обращаются к врачу по поводу простатита чаще, чем по поводу аденомы или рака предстательной железы. В более позднем отчете сказано, что простатит — самое распространенное урологическое заболевание среди мужчин моложе 50 лет и третье по распространенности среди мужчин старше 50 лет. В США I это заболевание является причиной 2 млн амбулатор- I ных посещений врача в год. К 79 годам простатит пере- I носят 10—30% мужчин.
Несмотря на высокую распространенность и боль- I шое социально-экономическое значение, наши знания I в области этиологии, диагностики и лечения простатита I недостаточны. Единодушия в отношении классифика- I ции простатита удалось достичь относительно недавно.И в 1995 г., на симпозиуме по хроническому простатиту, I проведенному Институтом диабета, болезней почек и I органов пищеварения (табл. 14.7). Согласно этой клас- I сификации выделяют четыре типа простатита. Типы 1 и I II соответствуют острому и хроническому простатиту. 1 Их диагностируют при наличии воспаления предста- I тельной железы и уропатогенных бактерий в ее секрете. I Тип III обозначает синдром хронической тазовой боли. I Клиническая картина при этом синдроме напоминает I простатит, но возбудитель в секрете предстательной же-1 лезы отсутствует. По содержанию лейкоцитов в секрете I предстательной железы и моче после массажа предста-1
Глава 14. Бактериальные инфекции мочевых путей и половых органов
 тельной железы выделяют две формы этого синдрома — воспалительную и невоспалительную. К простатиту IV типа относится бессимптомный простатит, то есть бессимптомное воспаление предстательной железы, выявленное случайно при биопсии предстательной железы по поводу других заболеваний.
тельной железы выделяют две формы этого синдрома — воспалительную и невоспалительную. К простатиту IV типа относится бессимптомный простатит, то есть бессимптомное воспаление предстательной железы, выявленное случайно при биопсии предстательной железы по поводу других заболеваний.
Диагностика
Четырехстаканная проба, предложенная И. Миаресом и Т. Стейми еще в 1968 г., до сих пор остается основным методом диагностики простатита. Эта проба позволяет уточнить локализацию инфекции. Исследуют три образца мочи и секрет предстательной железы. В первую емкость собирают первые 10 мл мочи (материал из мочеиспускательного канала), во вторую — среднюю порцию мочи (материал из мочевого пузыря), в третью — секрет предстательной железы, в четвертую — 10 мл мочи после массажа предстательной железы. Емкости помечают ПМ1, ПМ2, СПЖ и ПМЗ соответственно (ПМ— порция мочи, СПЖ — секрет предстательной железы). Проводят посев всех образцов. Если в ПМ2 бактерии отсутствуют или выявляются в минимальной концентрации, а в ПМ1 бактерий содержится больше, чем в СПЖ и ПМЗ, диагностируют передний уретрит или обсеменение мочеиспускательного канала. При простатите концентрация бактерий в СПЖ и ПМЗ по крайней мере в 10 раз больше, чем в ПМ1. Информативна и микроскопия осадка образцов. В норме секрет предстательной железы содержит менее 10 лейкоцитов в поле зрения при большом увеличении микроскопа. Наличие более 10 лейкоцитов в поле зрения, особенно вместе с ксан-томными клетками, свидетельствует о воспалении. Однако при хроническом простатите на фоне антимикробной терапии содержание лейкоцитов в секрете может быть не увеличено или увеличено незначительно. Более того, у 5—10% здоровых мужчин содержание лейкоцитов в секрете предстательной железы превышает 10 в поле зрения при большом увеличении микроскопа. Все это объясняет, почему микроскопия осадка дополняет, но не заменяет посев.
Предложен более простой, но столь же информативный, как четырехстаканная проба, метод диагностики
простатита — исследование мочи до и после массажа предстательной железы. Исследование лучше проводить до начала антимикробной терапии, в отсутствие уретрита. В полученных образцах мочи сравнивают число бактерий и лейкоцитов. Однако несмотря на информативность перечисленных исследований,стандартом диагностики простатита остается микроскопия и посев секрета предстательной железы.
Острый простатит
Этиология и патогенез
Спектр возбудителей острого простатита и их чувствительность к антимикробным средствам те же, что и при инфекциях мочевых путей. Самые частые возбудители — аэробные грамотрицательные бактерии. В 80% случаев это Escherichia coli, в 10—15% — Pseudomonas aeruginosa, Serratia spp., Klebsiella spp. и Proteus spp., в 5— 10% — энтерококки. Другие грамположительные бактерии, помимо энтерококков, вызывают острый простатит только в особых условиях. Так, Staphylococcus aureus может быть возбудителем острого простатита при постоянной катетеризации мочевого пузыря. Анаэробы вызывают простатит очень редко. Иногда возбудителей бывает несколько.
Полагают, что возбудители проникают в предстательную железу восходящим путем и в результате рефлюкса инфицированной мочи в предстательные проточки. Не исключено, что из-за особенностей строения предстательной железы в патогенезе простатита основную роль играет именно второй механизм. Инфекция в большинстве случаев локализуется в периферической зоне, проточки которой расположены горизонтально. Это способствует рефлюксу мочи и застою секрета. Проточки центральной зоны проходят косо сверху вниз, поэтому опорожняются более полноценно. Кроме того, бактерии могут проникать в предстательную железу из прямой кишки контактным или лимфогенным путем.
Клиническая картина
Для острого простатита характерны лихорадка, ознобы, боль в прямой кишке, крестце и промежности, императивные позывы, учащенное и болезненное мочеиспус-
Таблица 14.7. Классификация простатита (Институт диабета, болезней почек и органов пищеварения)
Класс ификация
Тип 1 — острый простатит Тип 11 — хронический простатит Тип III — синдром хронической тазовой боли Тип ША — воспалительная форма
Тип П1Б — невоспалительная форма
Тип IV — бессимптомный простатит
Диагност ические критерии
Острая инфекция предстательной железы с клиническими проявлениями
Рецидивирующая инфекция предстательной железы
Возбудитель в секрете предстательной железы не обнаруживается
В секрете предстательной железы более 10 лейкоцитов в поле зрения при
большом увеличении микроскопа
В секрете предстательной железы менее 10 лейкоцитов в поле зрения при
большом увеличении микроскопа
Бессимптомное течение, диагноз устанавливают случайно при биопсии
или исследовании секрета предстательной железы
Глава 14. Бактериальные инфекции мочевых путей и половых органов
 кание. Из-за отека предстательной железы возможна острая задержка мочи. Часто отмечаются недомогание, артралгия и миалгия. При пальцевом ректальном исследовании предстательная железа крайне болезненна, увеличена, с неровной поверхностью. Отмечается местное повышение температуры. При присоединении инфекции мочевых путей моча становится мутной и зловонной. Возможна макрогематурия.
кание. Из-за отека предстательной железы возможна острая задержка мочи. Часто отмечаются недомогание, артралгия и миалгия. При пальцевом ректальном исследовании предстательная железа крайне болезненна, увеличена, с неровной поверхностью. Отмечается местное повышение температуры. При присоединении инфекции мочевых путей моча становится мутной и зловонной. Возможна макрогематурия.
Диагностика
Диагноз нередко удается поставить на основании данных анамнеза и физикального исследования. В общем анализе крови обнаруживают лейкоцитоз со сдвигом лейкоцитарной формулы влево, в общем анализе мочи — лейкоцитурию, гематурию и бактериурию. Возбудителя выделяют при посеве мочи. Массаж предстательной железы и четырехстаканная проба противопоказаны. Во-первых, массаж предстательной железы при остром простатите вызывает сильную боль, во-вторых, он может спровоцировать бактериемию. По тем же соображениям не рекомендуется катетеризация мочевого пузыря. При острой задержке мочи выполняют эпицис-тостомию.
Лечение
При остром простатите антимикробные средства особенно хорошо проникают в предстательную железу, поэтому лечение очень эффективно (даже при использовании препаратов, которые плохо проникают в неизмененную предстательную железу). Эмпирическое лечение начинают сразу, не дожидаясь результатов посева. Применяют препараты, активные в отношении основных возбудителей острого простатита — грамотрицатель-ных палочек и энтерококков. Эффективны фторхиноло-ны и ТМП/СМК. При необходимости антимикробную терапию меняют после получения результатов посева мочи. Кроме того, показаны жаропонижающие средства, анальгетики, размягчающие слабительные, обильное питье и постельный режим. Чтобы избежать осложнений — абсцесса предстательной железы и хронического простатита, лечение продолжают 4—6 нед. При сепсисе, иммунодефицитах, острой задержке мочи и тяжелых сопутствующих заболеваниях показана госпитализация. В стационаре назначают антимикробные средства для парентерального введения, как правило, комбинацию ампициллина и аминогликозида. Как только состояние больного улучшается и становится известной чувствительность возбудителя к антимикробным средствам, переходят на прием препаратов внутрь.
Критерий излечения — отсутствие бактериурии. Через 1 и 3 мес после окончания лечения выполняют посев средней порции мочи (ПМ2). Сохранение бактериурии свидетельствует о высоком риске абсцесса предстательной железы и хронического простатита. Лечение этих осложнений острого простатита подробно описано ниже.
Как уже упоминалось, катетеризация мочевого пузыря и любые трансуретральные вмешательства при ост-
ром простатите противопоказаны. При острой задержке мочи показана эпицистостомия. После восстановления самостоятельного мочеиспускания эпицистостому из мочевого пузыря удаляют.
Осложнения
Абсцесс предстательной железы после острого проста- 1 тита возникает в основном у больных с иммунодефи-цитами, сахарным диабетом, а также при постоянной катетеризации мочевого пузыря или диализе. Если инфекция не устранена, возможно развитие хронического простатита.
Хронический простатит
Этиология и патогенез
Возбудители хронического простатита те же, что и острого. В основном это грамотрицательные палочки и энтерококки. Другие грамположительные бактерии встречаются редко, а если и встречаются, то не вызывают рецидивирующие инфекции мочевых путей. Роль Mycoplasma spp., Ureaplasma spp. и Chlamydia spp. в этиологии I хронического простатита не подтверждена. Большинст- I во авторов считают, что они играют роль в патогенезе 1 синдрома хронической тазовой боли.
Date: 2016-11-17; view: 435; Нарушение авторских прав