
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Методы исследования
|
|
1.3.1 Определение влажности рефрактометрическим методом. Для приготовления 50%-ного раствора взвесить на технохимических весах 5 г сиропа в бюксе с палочкой и крышкой или стаканчике, добавить 5 г дистиллированной воды, растворить навеску при подогревании на водяной бане (температура не выше 70 °С). После охлаждения раствора бюксу взвесить и добавить необходимое количество воды (пока раствор не будет весить 10 г). После этого каплю раствора, нанести стеклянной палочкой на призму рефрактометра и по шкале определить в процентах содержание сухих веществ в растворе. Призму рефрактометра предварительно выдержать при температуре 20 °С.
Массовую долю сухих веществ в сиропе (без учета поправок на температуру, углеводы патоки и инвертного сиропа) рассчитать по формуле:
| Х = nb/g, | (2) |
где n - показания процентной шкалы рефрактометра при температуре 20 °C;
b - масса раствора навески;
g - навеска карамели, г.
Коэффициент преломления растворов веществ зависит от температуры, поэтому в случае отклонения температуры раствора от 20 °C необходимо ввести температурную поправку, определив ее по таблице 3. При температуре выше 20 °С величину поправки следует прибавить, а при температуре ниже 20 °С вычесть из найденного количества СВ.
Таблица 3 – Температурные поправки, рассчитанные на 20 °С
| Температура, °С | Количество сухих веществ, в процентах | |||||
| От процента сухих веществ отнять | ||||||
| 0,35 | 0,37 | 0,38 | 0,39 | 0,40 | 0,41 | |
| 0,28 | 0,30 | 0,30 | 0,31 | 0,31 | 0,32 | |
| 0,21 | 0,22 | 0,23 | 0,24 | 0,24 | 0,24 | |
| 0,14 | 0,15 | 0,15 | 0,16 | 0,16 | 0,16 | |
| 0,07 | 0,08 | 0,08 | 0,08 | 0,08 | 0,08 | |
| К проценту сухих веществ прибавить | ||||||
| 0,08 | 0,08 | 0,08 | 0,08 | 0,08 | 0,08 | |
| 0,15 | 0,15 | 0,16 | 0,16 | 0,16 | 0,16 | |
| 0,23 | 0,23 | 0,24 | 0,24 | 0,24 | 0,24 | |
| 0,31 | 0,31 | 0,31 | 0,32 | 0,32 | 0,32 | |
| 0,39 | 0,40 | 0,40 | 0,40 | 0,40 | 0,40 | |
| 0,47 | 0,48 | 0,48 | 0,48 | 0,48 | 0,48 | |
| 0,55 | 0,56 | 0,56 | 0,56 | 0,56 | 0,56 | |
| 0,63 | 0,64 | 0,64 | 0,64 | 0,64 | 0,64 | |
| 0,72 | 0,73 | 0,73 | 0,73 | 0,73 | 0,73 | |
| 0,80 | 0,81 | 0,81 | 0,81 | 0,81 | 0,81 |
1.3.2 Определение оптической плотности. Для этого20 г сиропа разводят в 100 см3 дистиллированной воды. Раствор наливают в кювету толщиной 10 мм и определяют оптическую плотность на ФЭК при светофильтре с длинной волны 430 нм. Показатель оптической плотности используют для расчета цветности (К, ед. цветности), рассчитывают по формуле:
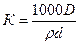 , ,
| (3) |
где D – оптическая плотность раствора;
ρ – концентрация раствора, в процентах (концентрация раствора расчитывается по формуле 1:
ρ = СВсиропа·20/120,
d – толщина кюветы, мм.
1.3.3 Определение редуцирующих веществ. Ряд методов определения редуцирующих сахаров основан на применении щелочного раствора меди, который получается при взаимодействии щелочного раствора сегнетовой соли с сульфатом меди (медным купоросом). Например фелинговый метод (метод горячего титрования).
Раствор сульфата меди носит название Фелинг I, щелочной раствор сегнетовой соли — Фелинг II.
В первый момент при смешивании щелочного раствора сегнетовой соли и медного купороса образуется голубой осадок гидроксида меди.
CuSO4+ 2NaOН =Сu (ОН)2 + Na 2SO4.
При взаимодействии Сu(ОН)2 с сегнетовой солью осадок растворяется, образуется медный комплекс, и раствор окрашивается в густой синий цвет.
Редуцирующие сахара, воздействуя на образовавшийся медный комплекс, восстанавливают медь до закиси.
При количественном определении редуцирующих сахаров пользуются таблицами, составленными на основании экспериментальных данных при определенных условиях опыта, которые необходимо соблюдать. При изменении длительности нагревания или степени щелочности раствора получаются неверные результаты. При определении общего сахара предварительно проводят инверсию сахарозы.
Методов количественного определения редуцирующих веществ и общего сахара с применением щелочных растворов меди довольно много: йодометрический, перманганатный, феррицианидный, фотоколориметрический (с использованием фотоэлектроколориметра ФЭК-56 или ФЭК-М), поляриметрический, фелинговый и биологический. Некоторые из них основаны на определении содержания сахара по количеству выделившейся закиси меди (йодометрический), другие — по количеству израсходованного инвертного сахара на восстановление точно отмеренного объема щелочного раствора меди (методы Соксле, Лейна, Эйнона).
1. Определение содержания редуцирующих веществ методом титрования щелочного раствора меди раствором инвертного сиропа.
Метод предложен Лейном и Эйноном. В качестве индикатора в конце реакции используют метиленовый синий. Редуцирующий сахар придает темно-синюю окраску фелинговой жидкости. При нагревании инвертный сахар вступает в реакцию с фелинговой жидкостью, постепенно обесцвечивает ее с выделением закиси меди ярко-красного цвета. Окраска закиси меди затрудняет установление конца реакции, поэтому используют метиленовый синий. Инвертный сахар после восстановления фелинговой жидкости восстанавливает метиленовый синий до образования бесцветного лейкосоединения и обесцвечивания раствора.
Для приготовления стандартного раствора инвертного сахара навеску химически чистой сахарозы или сахара-рафинада, выдержанных в эксикаторе в течение трех суток, в количестве 1,9 г растворяют в воде, переносят в мерную колбу на 200 мл. Количество воды, затраченное на растворение и перенесение навески, должно быть около 100 мл.
К раствору прибавляют 7-8 мл концентрированной соляной кислоты (плотн. 1,19). Погрузив термометр в колбу, ставят ее на водяную баню, нагретую приблизительно до 80 °С. В течение двух или трех мин температуру жидкости доводят до 67 – 70 °С и при этой температуре выдерживают раствор ровно пять мин, после чего содержимое колбы немедленно охлаждают под струей холодной воды до комнатной температуры и нейтрализуют раствором щелочи (25—30%-ной концентрации), прибавив от одной до двух каплей метилового оранжевого (зона перехода окраски рН – 3,1-4,4). После этого раствор в колбе разбавляют водой до метки и взбалтывают. В одном мл приготовленного стандартного раствора содержится 0,01 г инвертного сахара.
При установлении титра фелинговой жидкости (контрольное титрование – количество редуцирующих веществ в стандартном растворе) в коническую колбу на 100–200 см3 отмеривают пипетками по 10 см3 жидкости Фелинг I и Фелинг II, прибавляют пипеткой 10 см3 воды, нагревают до кипения, кипятят ровно одну мин. Не прерывая кипячения, вносят три капли метиленового синего и титруют тем же раствором инвертного сахара до исчезновения синей окраски и появления красного осадка. Величину навески сиропа g определить по формуле:
| g=aV*100/p, | (4) |
где а —допустимое содержание определяемого сахара в 100 мл приготовленного раствора (0,032), г;
V — объем мерной колбы, взятой для приготовления раствора навески, мл (если навеску необходимо растворить);
р — предполагаемое содержание редуцирующих веществ в исследуемом продукте, в процентах (в карамельном сиропе 12 – 14 %).
В коническую колбу на 100 ─ 150 мл пипетками отмеривают по 10 см3 жидкости Фелинг I, Фелинг II, дистиллированной воды и расчетное количество сиропа (взвешенного на фильтровальной бумаге).
Если сироп имеет водонерастворимые вещества (белки и жиры), то перед проведением опыта навеску подвергают растворению дистиллированной водой в мерной колбе на 100 см3: колбу заполняют наполовину водой, вводят навеску и помещают на водяную баню, температура которой не выше 60 оС. При этой температуре, периодически взбалтывая, выдерживают в течение 15 мин. Охладив раствор до комнатной температуры, осаждают несахара раствором ZnSO4·7H2О, взятого в количестве 10 см3, тщательно взбалтывают и вводят 10 см3 гидроксида натрия или калия. Осветлив жидкость, объем мерной колбы доводят до метки, взбалтывают и через две мин отфильтровывают. Для определения редуцирующих веществ берут 10 см3 приготовленного раствора, но из метода, описанного выше, исключают 10 см3 воды.
Коническую колбу с исследуемым раствором нагревают при взбалтывании до кипения, кипятят одну мин (время отмечают по песочным часам). Не прерывая кипячения, прибавляют три капли метиленового синего и дотитровывают из бюретки стандартным раствором инвертного сахара до исчезновения синего окрашивания и выпадения красного осадка..
Количество редуцирующих веществ X (в %) определить по формуле:
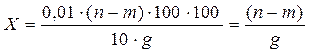 , ,
| (5) |
где n - объем стандартного раствора инвертного сахара, затраченный на 20 мл щелочного раствора меди, см3;
m - количество стандартного раствора инвертного сахара, затраченного при дотитровывании, см3;
g - навеска продукта, г.
1.3.4 Определение активной кислотности потенциометрическим методом. Метод основан на измерении концентрации водородных ионов в испытуемом растворе.
5 г исследуемого продукта смешивают в стакане с 50 см3 дистиллированной воды, ускоряя, если требуется, растворение нагреванием до температуры не выше 70 оС, охлаждают до температуры (20 ± 2) 0С.
Электроды потенциометра погружают в исследуемый раствор и, не обращая внимания на осадок, после того, как показания прибора примут установившиеся значение, отсчитывают величину рН по шкале прибора. Результаты исследований представляют в виде таблицы 4 и строят графические зависимости изменения массовой доли сухих веществ, редуцирующих веществ, активной кислотности и цветности сиропов от продолжительности температурного воздействия; по ним делают вывод по изменению этих показателей во времени в зависимости от состава и соотношения компонентов в рецептурной смеси и температуры уваривания. Полученные результаты исследований сводят в таблицу 4.
Таблица 4 ─ Результаты исследований
| Показатели | Вариант | Продолжительность нагревания, мин. | |||
| Массовая доля, в процентах сухих веществ | |||||
| Массовая доля, %в процентах редуцирующих веществ | |||||
| Активная кислотность, ед. прибора | |||||
| Цветность раствора |
Вопросы для самопроверки
1. Что представляют собой сиропы? Дайте обоснование концентрации кондитерских сиропов.
2. Что такое инвертный сироп? Опишите технологию его получения.
3. Какие изменения происходят с сахарозой при термическом воздействии?
4. На чем основан метод определения цветности сахаропаточных и сахароинвертных сиропов?
5. Что лежит в основе фотоэлектроколориметрических методов анализа?
6. Какими методами можно определить изменения, происходящие в сахаропаточных и сахароинвертных сиропах при нагревании?
7. Назовите технологические параметры, при которых происходит
уваривание сахаропаточных и сахароинвертных сиропов?
8. Какими методами можно определить массовую долю сухих и редуцирующих веществ в объектах кондитерского производства?
Date: 2015-04-23; view: 1136; Нарушение авторских прав