
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Переносчики электронов
|
|
Многие переносчики электронов представлены белками цитохромами, содержащие в качестве простетической группы гем, который придает им красное окрашивание. Цитохромы (сь с, а и а3) расположены в различных участках дыхательной цепи и различаются структурой полипептидных цепей, строением боковых групп и способом прикрепления к апобелку. Присоединение электрона к гему влечет за собой изменение степени окисления железа в активном центре.
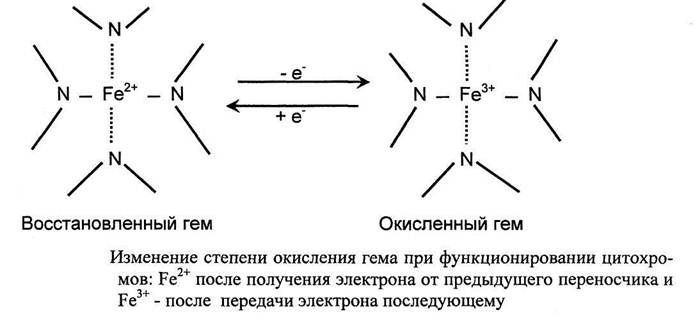
К другому типу негемовых белков - переносчиков электронов относят железо-серные белки (FeS). В них атомы железа связаны с сульфгидрильными группами остатков цистеина белка, а также сульфгидрильными анионами, образуя железо-серные комплексы или центры.
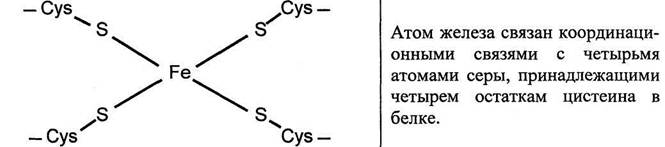
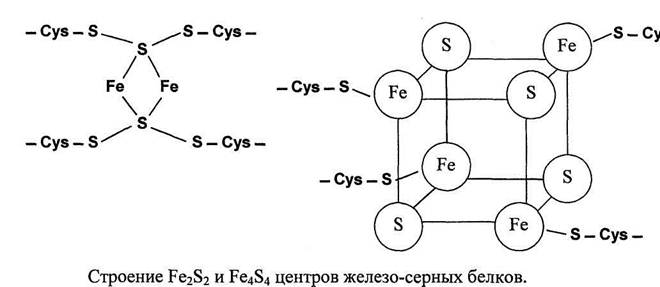
В Fe2S2 центре каждый из двух атомов железа связан координационными связями с двумя атомами неорганической серы и двумя остатками цистеи-на в белке.
В Fe4S4 четыре атома железа связаны с четырьмя атомами серы и четырьмя остатками цистеина в белке.
Атомы железа в FexSx-4eHTpax могут находиться в окисленном (Fe3+) или восстановленном (Fe2+) состоянии.
Атомы железа в FexSx-4eHTpax могут принимать или отдавать электроны переходя в 4>eppo(Fe2+)- или ферри(Ре3+)- состояния. Железо-серные центры функционируют совместно с флавиновыми ферментами, принимая электроны от сукцинатде-гидрогеназы (комплекс II) и дегидрогеназ, участвующих в окислении липидов.
Еще одним типом переносчиков электронов является ФМН-содержащий белок. ФМН (флавин-мононуклеотид) переносит электроны от НАДН на железо-серные центры (включен в состав комплекса I).
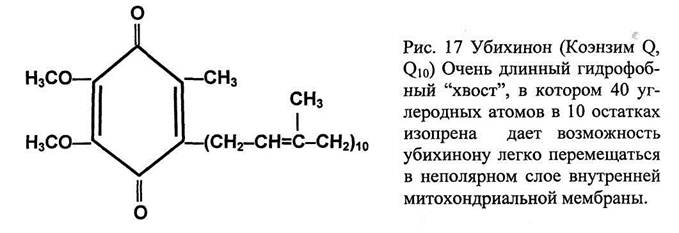
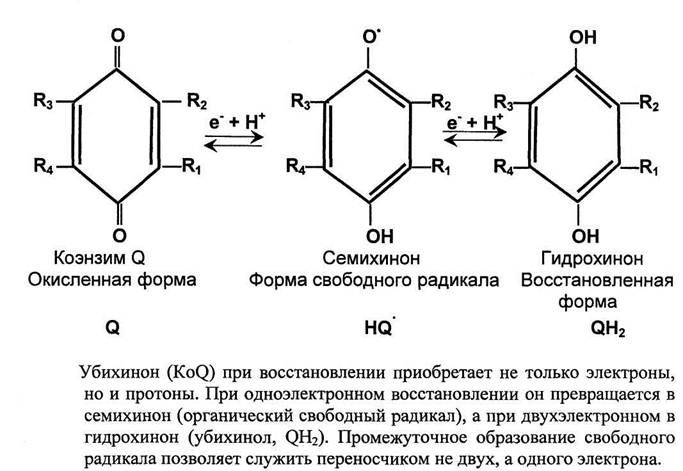
Единственный небелковый переносчик электронов - убихинон (коэнзим Q), названный так, потому, что с одной стороны он хинон, а с другой встречается повсюду (ubiquitous - вездесущий). Железо-серные центры отдают электроны уби-хинону, который включен в состав комплекса III.
Один из цитохромов - цитохром С не закреплен жестко в митохондриальной мембране, а свободно перемещается между III и IV комплексами по внешней стороне мембраны и переносит электрон. Цитохром С гемсодержащий водорастворимый белок, массой 12,5 кДа, содержит 104 аминокислотных остатка.
Коэнзим Q и цитохром С - мобильные переносчики электронов дыхательной цепи. Все другие белковые переносчики - интегральные белки, занимают в мембране строго фиксированное положение и ориентированы определенным образом.
Date: 2015-05-22; view: 1231; Нарушение авторских прав