
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Изменение энтропии в неравновесных процессах
|
|
Выше говорилось, что в классической термодинамике рассматриваются только равновесные процессы. Реальные процессы в различной степени отличаются от равновесных: иногда незначительно (тогда можно без поправок применять все законы классической термодинамики), иногда – существенно. В последнем случае неравновесность приходится учитывать в расчётах. Этим занимается «неравновесная термодинамика», основателем которой является И. Пригожин.
Уже Р. Клазиус, а затем и И. Пригожин установили, что энтропия является специфической функцией. Она выступает в двух ипостасях. При рассмотрении равновесных систем она качественно не отличается от других известных нам функций состояния – u и h и используется в расчетах наряду с ними. Но она выступает в другом качестве при изучении неравновесных процессов, поскольку только она дает возможность характеризовать степень неравновесности процесса.
Возьмем термодинамическую систему (рабочее тело) в равновесном состоянии 1. Это значит, что его параметры (T 1, v 1, h 1, s 1 и т.д.) во всех точках одинаковы. Пусть эта система, совершив какой-то термодинамический процесс, перейдет в состояние 2. Мы не знаем, равновесным был этот процесс или нет, но мы можем выждать достаточно времени, чтобы состояние 2 стало равновесным (т. е. T 2, s 2 и т.д. стали одинаковыми по всему объему тела). В результате мы можем посчитать изменение любого параметра в этом процессе, в том числе и 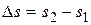 .
.
Рассмотрим принципиальные отличия неравновесных процессов от равновесных на примере расширения газа в цилиндре под поршнем (рис. 3.2), получающего теплоту d q от источника с температурой Т 1 и совершающего работу против внешней силы Р, действующей на поршень.
| Рис. 3.2. Расширение газа под поршнем, совершающего работу против внешних сил |

Расширение будет равновесным только в случае, если температура газа Т равна температуре источника (Т = Т 1), внешняя сила Р равна давлению газа на поршень (Р = pF), а при расширении газа нет ни внешнего, ни внутреннего трения. Работа расширения газа в этом случае равна 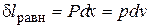 , а изменение энтропии рабочего тела в таком процессе
, а изменение энтропии рабочего тела в таком процессе 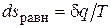 .
.
Невыполнение хотя бы одного из указанных условий делает расширение газа неравновесным. Если неравновесность вызвана трением поршня о стенки цилиндра, то работа d l, совершаемая против внешней силы Р, оказывается меньше, чем pdv, так как часть ее затрачивается на преодоление трения и переходит в теплоту d q тр. Она воспринимается газом вместе с подведенной теплотой d q, в результате чего возрастание энтропии газа в неравновесном процессе 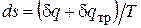 оказывается больше, чем в равновесном при том же количестве подведенной от источника теплоты d q.
оказывается больше, чем в равновесном при том же количестве подведенной от источника теплоты d q.
Если неравновесность вызвана отсутствием механического равновесия (P < pF), поршень будет двигаться ускоренно. Быстрое движение поршня вызывает появление вихрей в газе, затухающих под действием внутреннего трения, в результате чего часть работы расширения опять превращается в теплоту d q тр. Работа против внешней силы снова получается меньше, а возрастание энтропии – больше, чем в равновесном процессе с тем же количеством теплоты d q.
Если неравновесность вызвана теплообменом при конечной разности температур (температура газа Т меньше температуры источника Т 1), то возрастание энтропии рабочего тела  оказывается больше, чем
оказывается больше, чем 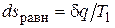 в равновесном процессе из-за снижения температуры газа.
в равновесном процессе из-за снижения температуры газа.
Итак, неравновесность всегда приводит к увеличению энтропии рабочего тела при том же количестве подведенной теплоты. Это выражение является одной из формулировок второго закона термодинамики.
Итак, для равновесных процессов справедливо соотношение  . Разобранный пример достаточно наглядно показывает, что в неравновесных процессах
. Разобранный пример достаточно наглядно показывает, что в неравновесных процессах 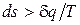 , если d q – количество подведенной к системе или отведенной от нее теплоты, а Т – температура источника теплоты.
, если d q – количество подведенной к системе или отведенной от нее теплоты, а Т – температура источника теплоты.
В общем виде это можно записать следующим образом
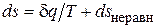 , (3.7)
, (3.7)
причем ds неравн всегда положительно.
Соотношение (3.7) представляет собой математическую запись второго закона термодинамики.
Для адиабатно изолированных систем, которые по определению не обмениваются теплотой с окружающей средой (d q = 0), выражение (3.7) принимает вид
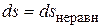 . (3.8)
. (3.8)
Если в адиабатно изолированной системе осуществляются равновесные процессы, то энтропия системы остается постоянной.
Самопроизвольные (а значит, и неравновесные) процессы в изолированной системе всегда приводят к увеличению энтропии.
Следует подчеркнуть, что равенство (3.8) применимо только к адиабатно изолированным системам. Если от системы отводится теплота, то ее энтропия может убывать и при протекании в ней самопроизвольных (неравновесных) процессов, когда 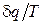 в формуле (3.7) больше по абсолютной величине, чем ds неравн.
в формуле (3.7) больше по абсолютной величине, чем ds неравн.
Date: 2015-05-09; view: 1939; Нарушение авторских прав