
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Второй закон термодинамики
|
|
Первый закон термодинамики, рассмотренный в предыдущей лекции, по сути представляет собой закон сохранения энергии для процессов, происходящих в макроскопических системах, состоящих из большого числа микрочастиц. Он позволяет количественно описать превращение одних видов энергии в другие. Однако, как показывает опыт, далеко не все процессы, разрешенные первым законом термодинамики, являются возможными. Например, наливаем горячую воду в холодный стакан. Очевидно, что вследствие теплопередачи стакан нагреется, а вода немного остынет. Но первому закону термодинамики не противоречил бы и обратный процесс: стакан становится все холоднее и холоднее, а вода нагревается и закипает. Другой пример: положим на пол деревянный брусок и сообщим ему некоторую скорость. Брусок начнет скользить по полу и, поскольку на него будет действовать сила трения, через некоторое время остановится. В процессе скольжения кинетическая энергия бруска превращается в энергию теплового движения молекул самого бруска и покрытия пола. Однако, закон сохранения энергии не был бы нарушен и при протекании данного процесса в обратном направлении: брусок и контактирующая с ним часть пола самопроизвольно охлаждаются, вследствие чего брусок приобретает кинетическую энергию и приходит в движение.
Приведенные выше примеры показывают, что, помимо первого закона термодинамики, позволяющего количественно охарактеризовать процессы, происходящие в макросистемах, необходим еще один закон, определяющий направление, в котором эти процессы протекают. Такой закон был сформулирован в середине XIX века и носит название второго закона термодинамики. Существует несколько эквивалентных формулировок данного закона. Приведем две из них – Клаузиуса[18] и Кельвина.
1. Клаузиус (1850 г.): невозможен самопроизвольный переход теплоты от тела с меньшей температурой к телу с большей температурой, или невозможен такой процесс, единственным результатом которого был бы переход теплоты от тела с меньшей температурой к телу с большей температурой.
Обратите внимание, что формулировка Клаузиуса отнюдь не запрещает переход теплоты от холодного тела к горячему, а запрещает процесс, в котором такой переход происходит самопроизвольно и является единственным результатом. Например, в Вашем домашнем холодильнике теплота переходит от холодной морозильной камеры к теплому воздуху комнаты, но этот процесс не является самопроизвольным и не является единственным результатом работы холодильника (т.к. холодильник при этом потребляет электрическую энергию).
2. Кельвин (1851 г.): невозможен такой процесс, единственным результатом которого было бы полное превращение теплоты, полученной от какого-либо тела, в работу.
Вы можете сказать, что формулировке Кельвина противоречит процесс изотермического расширения идеального газа, в ходе которого не изменяется внутренняя энергия, и вся теплота идет на совершение газом работы против внешних сил: 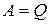 (см. § 3.3). Однако, полное превращение теплоты в работу не является единственным результатом данного процесса, поскольку в его ходе объем газа увеличивается, а значит состояние газа изменяется.
(см. § 3.3). Однако, полное превращение теплоты в работу не является единственным результатом данного процесса, поскольку в его ходе объем газа увеличивается, а значит состояние газа изменяется.
Второй закон термодинамики, также как и первый, является постулатом, т.е. принимаемым на веру обобщением огромного числа экспериментальных фактов.
Значительный объем экспериментальных данных, послуживших обоснованием второго закона термодинамики, был накоплен в результате многовековых неудачных попыток создать так называемый вечный двигатель. Поэтому законы термодинамики часто формулируют как запрет вечного двигателя. Первый закон постулирует невозможность вечного двигателя I рода - устройства, способного бесконечно долго совершать механическую работу без подвода энергии (работа возникает «из ничего»). Второй закон термодинамики утверждает невозможность постройки вечного двигателя II рода – устройства, которое забирало бы теплоту из океана и полностью превращало бы его в работу (такой двигатель практически то же, что и «настоящий вечный», т.к. при современном уровне потребления человечеством энергии температура океанов за 1000 лет понизилась бы всего на 1 К).
Date: 2015-05-08; view: 1119; Нарушение авторских прав