
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Равновесие жидкости и насыщенного пара
|
|
Рассмотрим процесс сжатия вещества при постоянной температуре. Первоначально вещество предполагается газообразным. Вначале, по мере уменьшение объема, давление газа будет расти (рис.1.9). По достижении объема V г давление перестает изменяться, а вещество перестает быть однородным – часть газа конденсируется в жидкость. Происходит расслоение вещества на две фазы: жидкую и газообразную. По мере дальнейшего уменьшения объема всё большая часть вещества переходит в жидкую фазу, причем переход осуществляется при постоянном объеме р н.п (давление насыщенного пара). После того как процесс конденсации заканчивается (это происходит при достижении объема V ж), дальнейшее уменьшение объема начинает сопровождаться быстрым ростом давления.
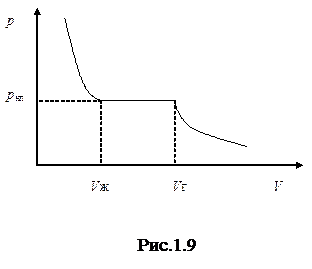 На рис.1.9 V г есть объем, занимаемый веществом в газообразном состоянии при давлении р н.п, V ж – объем вещества в жидком состоянии при том же давлении. При любом промежуточном значении объема часть вещества с массой mж будет находиться в жидком, а mп – в парообразном состоянии. Найдем отношение
На рис.1.9 V г есть объем, занимаемый веществом в газообразном состоянии при давлении р н.п, V ж – объем вещества в жидком состоянии при том же давлении. При любом промежуточном значении объема часть вещества с массой mж будет находиться в жидком, а mп – в парообразном состоянии. Найдем отношение 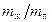 . Назовем удельным объемом
. Назовем удельным объемом 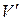 объем единицы массы вещества. Тогда, если масса вещества равна m, удельные объемы насыщенного пара и жидкости при давлении насыщенного пара будут равны:
объем единицы массы вещества. Тогда, если масса вещества равна m, удельные объемы насыщенного пара и жидкости при давлении насыщенного пара будут равны:
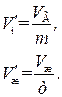 (1.76)
(1.76)
В состоянии, при котором масса жидкой фазы равна m ж, а масса пара m п, на долю жидкости будет приходиться объем V’ ж m ж, а на долю насыщенного пара – объем V’ п m п. В сумме оба эти объема должны быть равны объему V
V=V’ ж m ж +V’ п m п.
Подставив сюда выражение (1.76) для удельных объемов и заменив массу m суммой m ж + m п получим:
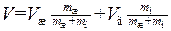 ,
,
отсюда
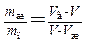 . (1.77)
. (1.77)
Таким образом, отношение масс жидкости и насыщенного пара в двухфазном состоянии равно отношению отрезков, на которые делит горизонтальный участок изотермы точка, изображающая состояние.
Отметим, что при температурах, далеких от критической, различий между объемами жидкости и пара бывает намного больше. Например, удельный объем насыщенного водяного пара при 100˚C в 1600 раз превышает удельный объем жидкой воды при той же температуре.
Итак, на диаграмме состояниям равновесия между жидкостью и насыщенным паром соответствует горизонтальный участок изотермы. Этот результат является общим для всех двухфазных состояний. Соотношение, аналогичное (1.77), имеет вид:
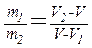
(m1 и m2 – массы вещества в первой и второй фазах).
Date: 2015-05-05; view: 1325; Нарушение авторских прав