
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Эффект Джоуля-Томсона
|
|
Зависимость внутренней энергии идеального газа от температуры и объёма даёт возможность получения низких температур за счёт расширения газа.
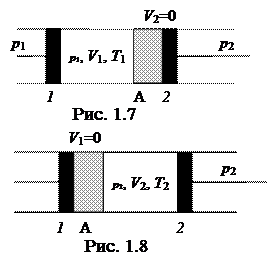 Особый интерес представляет процесс, предложенный Джоулем и осуществлённый позднее Томсоном (Кельвином). В трубе с теплоизолированными стенками, разделённой на две части пористой перегородкой А, могут перемещаться два поршня. В начале эксперимента 1 моль некоторого реального газа занимает объём V 1 между левым поршнем и перегородкой при температуре Т 1 и давлении р 1. Правый поршень занимает положение вплотную к перегородке и находится под давлением р 2 (рис.1.7). В процессе эксперимента левый поршень под давлением р 1 медленно продавливает газ через перегородку. При этом правый поршень перемещается под давлением р 2. В результате этих действий весь газ оказывается справа от перегородки, занимая объём V 2 при температуре Т 2 и давлении р 2 (рис.1.8). Определим соотношение между температурами Т 1 и Т 2.
Особый интерес представляет процесс, предложенный Джоулем и осуществлённый позднее Томсоном (Кельвином). В трубе с теплоизолированными стенками, разделённой на две части пористой перегородкой А, могут перемещаться два поршня. В начале эксперимента 1 моль некоторого реального газа занимает объём V 1 между левым поршнем и перегородкой при температуре Т 1 и давлении р 1. Правый поршень занимает положение вплотную к перегородке и находится под давлением р 2 (рис.1.7). В процессе эксперимента левый поршень под давлением р 1 медленно продавливает газ через перегородку. При этом правый поршень перемещается под давлением р 2. В результате этих действий весь газ оказывается справа от перегородки, занимая объём V 2 при температуре Т 2 и давлении р 2 (рис.1.8). Определим соотношение между температурами Т 1 и Т 2.
В соответствии с первым началом термодинамики при адиабатном процессе продавливания газа, или, как говорят, в процессе дросселирования газа, изменение внутренней энергии равно
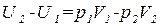 . (1.74)
. (1.74)
Пусть объём V 2 настолько велик, что газ после дросселирования можно считать идеальным. Тогда:
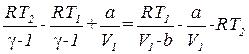 ,
,
учитывая, что 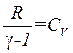 , получим
, получим
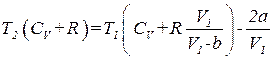 . (1.75)
. (1.75)
Теперь рассмотрим несколько случаев:
1. Пусть в объёме V 1 тоже находится идеальный газ, т.е. a = b = 0. Это значит, что Т 1 = Т 2 и эффект Джоуля-Томпсона не наблюдается.
2. Пусть между молекулами в реальном газе преобладают силы отталкивания, т.е. силы притяжения стремятся к нулю (a = 0). В этом случае
Т 2 > Т 1, наблюдается эффект Джоуля-Томпсона – изменение температуры реального газа при очень малом адиабатическом изменении объёма и давления. В данном случае газ нагревается. Это можно объяснить тем, что при наличии одних только сил отталкивания между молекулами газ представляет собой как бы сжатую пружину. При расширении газа потенциальная энергия переходит в кинетическую энергию хаотического движения молекул.
3. Пусть между молекулами в реальном газе преобладают силы притяжения, т.е. силы отталкивания стремятся к нулю (b = 0). Тогда Т 2 < Т 1, также наблюдается эффект Джоуля-Томпсона. В данном случае газ охлаждается. Объяснение такого эффекта аналогично: охлаждение является следствием того, что для расширения газу необходимо совершить работу против сил притяжения между молекулами. При этом их кинетическая энергия должна уменьшиться.
Третий случай выполняется для многих газов и применяется в технике (для получения низких температур).
Date: 2015-05-05; view: 1124; Нарушение авторских прав