
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Рак поджелудочной железы
|
|
Удельный вес первичного рака поджелудочной железы к числу всех раковых поражений составляет от 1 до 7% (А. И. Абрикосов, 1956; Н. С. Макоха, 1965; А. А. Шелагуров, 1970; Clifton, 1952, и др.). Е. Г. Кудимова и В. С. Григорян (1969) отмечают, что из 2571 больного, умершего от злокачественных опухолей в 4-й городской больнице, рак поджелудочной железы встретился в 4,9%. Показатель смертности на 100000 населения при этом заболевании равен 4—8 (А. П. Демченко, 1965^ Б. И. Гольдберг, Н. Н. Сульдина, 1969). Segi (1960) сообщает, что этот показатель составил в 1957г. в США 7,24, в Англии— 8,05, в Канаде—6,62. А. А. Шалимов, Н. А. Сумцов (1970> подсчитали, что если условно принять смертность от рака под-желудочнй железы по стране 4 на 100000 населения, то при-населении в 240 000 000 от этой причины умирает ежегодно около 10 000 человек. Средний показатель смертности от рака поджелудочнй железы выше, чем от рака пищевода (Н. С. Макоха, 1965; А. А. Шалимов, Н. А. Сумцов, 1970; Segi, 1960).
Большинство больных в возрасте свыше 50—60 лет. Средний возраст 234 больных, наблюдавшихся в МНИОИ им. П. А. Герцена, составил 60 лет. Описаны единичные наблюдения (Н. И. Лепорский, 1951; Becker, 1957) заболевания в возрасте от 6 мес до 4 лет.
Патологическая анатомия. Рак поджелудочной железы, согласно статистическим данным, чаще всего (в 50—80%) локализуется в головке. Bell (1957) приводит данные 609 вскрытий, умерших от этого заболевания; при этом рак головки обнаружен в 59,1%, тела—в 18,2%, хвоста—в 7,4%, диффузный рак—в 15,3%. По данным Berk (1941), на 1149 случаев рака поджелудочной железы головка была поражена в 82%, по. наблюдениям В. В. Виноградова (1959) —в 60%; А. А. Шела-гурова (1970)-в 70%, А. А. Шалимова (1970) - в 64,4%. В ОНЦ АМН СССР наблюдалось 293 больных: поражение головки железы отмечено в 76,1%, тела — в 14,6%, хвоста — в 6,8%, всей железы — в 2,4%.
Рак поджелудочной железы обычно имеет вид плотного бугристого узла различных размеров, белого или светло-желтого цвета, без четких границ переходящего в окружающую ткань. Небольшая опухоль головки может очень рано вызвать сдавле-ние общего желчного и панкреатического протоков, в результате чего развивается механическая желтуха, нарушается внешне-секреторная деятельность железы, приводящая к нарушению пищеварения и быстрому истощению. Опухоли, расположенные в теле и хвосте железы, могут достигать значительных размеров, не вызывая значительных нарушений функции органа.
В 80—90% рак развивается из эпителия выводных протоков значительно реже из островковой ткани железы и в болыпинстве случаев имеет строение аденокарциномы. Описан и плоскоклеточный рак, развивающийся из метаплазированных эпителиальных клеток выводных протоков, трансформировавшихся в -многослойный плоский эпителий.
В поджелудочной железе вокруг опухоли всегда определяется хронический воспалительный склеротический процесс с резко выраженной круглоклеточной инфильтрацией, значительным скоплением лейкоцитов и плазматических клеток. Железистые элементы подвергаются резкой атрофии. Выводные протоки расширены, а окружающая их ткань склерозирована.
Рак поджелудочной железы дает ранние обширные метастазы в регионарные—парапанкреатические лимфатические узлы, затем в мезентериальные, околожелудочные и другие лимфатические узлы брюшной полости и забрюшинного пространства. Отдаленными метастазами чаще всего поражается печень, реже легкие, мозг, кости, почки, кожа, параректальная клетчатка, лимфатические узлы средостения, шейной и надключичной области. По данным Н. И. Лепорского (1951), В. Я. Михайлова <1969), А. А. Шелагурова (1970), Вгачп с соавт. (1952), метастазы при раке поджелудочной железы выявляются в 70—90 Уо случаев. Т. А. Другова (1972) из ОНЦ АМН СССР на 1012 лскрытий обнаружила метастазы в 79,2%.
Опухоль может распространяться на соседние органы и ткани: двенадцатиперстную кишку, желудок, печеночно-двенадца-типерстную связку, а также сдавливать или прорастать близлежащие крупные венозные сосуды: верхнюю брыжеечную, воротную и нижню полую вены.
Клиника. Симптоматология многообразна и зависит от локализации опухоли в поджелудочной железе, а также от взаимоотношений опухоли с окружающими органами и тканями (желчными протоками, двенадцатиперстной кишкой, желудком, сосудами и др.).
Боли — довольно постоянный симптом, который отмечается у 60—90% больных (по данным МНИОИ им. П. А. Герцена— у 69%). Боли вызываются вовлечением в процесс нервных элементов поджелудочной железы и забрюшинного пространства;они могут быть обусловлены растяжением капсулы печени при обтурации общего желчного протока, а также воспалительными изменениями ав поджелудочной железе и застоем секрета в ее протоках. При раке головки чаще всего наблюдаются тупые боли в эпигастрии, преимущественно в верхнем правом квадранте живота. При поражении тела и хвоста железы болевой синдром обычно резко выражен. Боли локализуются в подложечной области и могут иррадиировать в оба подреберья, спину, поясницу, в паховую, крестцовую и бедренную области, вызывая жесточайшие страдания.
Желтуха — наиболее яркий признак рака поджелудочной железы. Частота ее появления определяется местоположением первичного опухолевого узла по отношению к желчным путям. Закономерно, что желтуха возникает значительно чаще (в 80— 90%) при локализации рака в головке, чем в теле и хвосте железы. Появление механической желтухи следует рассматривать не только как симптом, но и как тяжелое патологическое состояние, зачастую определяющее дальнейшую судьбу больного. Клиническим выражением желчной гипертензии является желтушное окрашивание кожи и слизистых оболочек, кожный зуд, нарушение функции печени, сердечно-сосудистой и нервной системы, а также различные нарушения обмена. Характерны брадикардия, головная боль, апатия, повышенная раздражительность. По мере нарастания интенсивности и длительности желтухи возможно развитие таких грозных осложнений, как печеночная или печеночно-почечная недостаточность, холемическое кровотечение.
При раке головки желтуха обычно стойкая, интенсивная; она яе является ранним признаком заболевания. По данным МНИОИ им. П. А. Герцена, у 70% больных желтухе предшествовали различные симптомы, вызванные фоновыми заболева-яиями и осложнениями опухолевого роста. Это позволило выделить несколько клинических форм рака поджелудочной железы в дожелтушном периоде: панкреатитоподобную, диабетоидную, холангитическую, гастритоподобную и др. Продолжительность •безжелтушного периода составила в среднем 4 мес. Аналогичные клинические формы приводят А. В. Смирнов и П. А. Воронцов (1971). В. А. Михайличенко и М. А. Тамаркина (1972) также указывают, что у 69,5% больных появлению желтухи предшествовали другие симптомы (гастрит, диабет, панкреатит и др.) на протяжении 1—6 мес.
Частым симптомом рака поджелудочной железы является значительное похудание (на 10—20 кг в течение нескольких месяцев). Нарушение питания наступает в результате прекращения поступления в кишечник желчи и панкреатического сока, участвующих в расщеплении жира и белка. С испражнениями теряется до 80% жира, принятого с пищей (А. А. Шалимов, 1970). Наблюдаются различные диспепсические расстройства: чувство тяжести после еды, отрыжка, изжога, тошнота, рвота, обильный частый зловонный стул глинисто-серого цвета.
Прорастание рака головки в двенадцатиперстную кишку приводит к развитию гастродуоденальной непроходимости, кишечному кровотечению и холангиту. Симптомы нарушения моторной и эвакуаторной функции двенадцатиперстной кишки выявляются у 13—18% больных (Л. А. Эндер, 1963; Mikal, Campbell, 1950).
Состояние отягощается присоединением симптомов хронического панкреатита и диабета. Воспалительный процесс в поджелудочной железе часто (в 50—60%) сопутствует опухолевому
поражению. Не исключено, что хронический рецидивирую-щий панкреатит может быть патогенетической основой для развития рака железы (А, И. Абрикосов, 1956; Д. Ф. Благовидов, 1973; Г. М. Маждраков, 1961). Однако возможен и обратный вариант: возникновение вторичного воспаления на фоне опухоли (А. В. Смирнов и др., 1972). У 9—32% больных наблюдается нарушение углеводного обмена различной степени: от преходящей гипергликемии и гликозурии до ярко выраженного диабета (Н. И. Лепорский, 1951; И. Н. Марков, 1970, и др.).
Рак поджелудочной железы может сопровождаться тромбозом сосудов. Т. А. Другова (1972), изучив 431 протокол вскрытий умерших от рака поджелудочной железы, установила, что тромбозы и эмболии были непосредственной причиной смерти у 12,2% больных. Strang, Walton (1953) наблюдали это осложнение у 24% больных. Все исследователи считают, что тромбо-образование значительно чаще встречается при поражении тела и хвоста, чем при поражении головки железы.
Диагностика. Поступление больного в хирургическое отделение из поликлиники с диагнозом «рак поджелудочной железы» — редкость. Статистический анализ, проведенный Ю. А. Га-лушко (1969), показал, что из 100 больных, страдающих опухолями или камнями желчевыводящей системы, 90 первоначально попадают в инфекционные стационары, где обследуются чрезвычайно длительно: от 4 до 12—14 лед. Таких больных следует скорее переводить в хирургические отделения, тем более что дифференцировать характер желтухи, как уже указывалось выше, обычно удается в течение нескольких дней.
Этиология желтухи может быть заподозрена уже на основании тщательно собранного анамнеза. В отличие от желчнока-менной болезни желтуха при раке поджелудочной железы возникает обычно без выраженного болевого синдрома, быстро нарастает, носит стойкий характер и наблюдается, как правило^ у лиц пожилого взраста. В возрасте до 40 лет у 2 из 3 больных желтуха имеет гепатогенное происхождение, реже она возникает в результате желчнокаменной болезни и совсем редко вызывается опухолевым процессом в панкреатодуоденальной зоне, Диагноз подтверждается не только симптоматологией заболевания, но и пальпаторными данными: у 70--75% больных раком головки поджелудочной железы определяется симптом Курву-азье. При раке тела и хвоста железы довольно часто удается пальпировать опухоль.
Бесспорную ценность имеет метод гипотонической дуодено-графии, позволяющий поставить правильный топический диагноз у 40—50% больных. Косвенными признаками рака головки поджелудочной железы являются: развернутость подковы двенадцатиперстной кишки; сужение ее просвета (рис. 118);выпрямленность и инфильтрация внутреннего контура кишки;
смещение антрального и препилорического отделов желудка вверх и влево. Для опухоли тела или хвоста железы характерно сдавление просвета желудка и смещение его кпереди или влево.
Уточнению диагноза может помочь чрескожная холангиография (рис. 119), дуоденофиброскопия, скеннирование поджелудочной железы (Ю. Н. Касаткин и др., 1971; Steinhoff et al., 1968), лапароскопия, а также селективная ангиография чрев-ной и верхней брыжеечной артерии (А. А. Шалимов и др., 1968; И. Б. Розанов, Г. И. Сабельников, 1970; Kahn et al., 1969;
Font et al., 1969). По данным А. П. Савченко с соавт. (1974),точность ангиографического заключения при раке поджелудочной железы достигает 89 %.
Во время операции наибольшие трудности встречаются при.дифференциальном диагнозе между раком поджелудочной же-.лезы и хроническим индуративным панкреатитом, так как оба 'процесса при осмотре и пальпации дают сходную картину. В этих случаях может быть произведена пункция измененного.участка железы со срочным цитологическим исследованием пунктата или биопсия ткани железы. Следует, однако, помнить, что раку поджелудочной железы, как правило, сопутствует хронический панкреатит и при получении отрицательных данных
•срочного морфологического исследования опухолевый процесс не может быть отвергнут.
Для уточнения диагноза применяется также холангиография;на операционном столе. Необходимо подчеркнуть, что некоторые методы исследования (чрескожная холангиография, пункция и биопсия поджелудочной железы, ангиография) небезопасны, в связи с чем должны применяться по строгим показаниям.
Лечение. Факт установления механической желтухи является основанием к операции. По данным А. Фишера (1961), Smith (1969) и др., полная обтурация желчных путей приводит v. смерти максимум через 6—7 мес. П. Н. Напалков, выступая на I Международном конгрессе хирургов-гастроэнтерологов в 1971 г., подчеркнул: «Важно не терять много времени для выяснения точной природы желтухи. Ранняя операция является вместе с тем и важным, а иногда и главным диагностическим приемом».
Радикальное лечение. При раке головки общепризнанной радикальной операцией является панкреатодуоденальная резекция, впервые успешно выполненная W. Kausch в 1909 г. Отечественные и зарубежные хирурги (В. Н. Шамов, 1955; А. Н. Велико-рецкий, 1959; В. В. Виноградов, 1959; А. А. Шалимов, 1970;Н. С. Макоха, 1964; В. И, Ршчиашвили, 1970; А. В. Смирнов, 1969; Child, 1966; Brunschwig, 1942; Cattel, 1953; Salmon, 1966;
•Smith, 1965, и др.) внесли большой вклад в разработку этого вмешательства. Из отечественных хирургов наибольший опыт панкреатодуоденальных резекций в настоящее время имеет А. А. Шалимов, который сообщил на XXIV Конгрессе Международного общества хирургов (1971) о 103 операциях, Н. С. Макоха произвел 85 операций (1969), А. В. Смирнов — 70 (1969), Е. С. Футорян и Б. М. Шубин (1977) —39. По данным зарубежных авторов (Warren et al., 1962), в клинике Лехи за 20 лет произведено 218 панкреатодуоденальных резекций. Monge с соавт. (1964) сообщают о 239 операциях в клинике Мейо за 22 года.
Несмотря на накопленный опыт, панкреатодуоденальная резекция широкого распространения не получила. Это вызвано целым рядом причин. Больные поступают в хирургические отделения в большинстве случаев с распространенным опухолевым процессом, в связи с чем резектабельность при раке поджелудочной железы низка и составляет по данным А. А. Шалимова (1970) 9,4%, В. И. Кочиашвгош (1970) — 10,1%; С. М. Микир-тумова (1963) — 4,9%, по данным клиники Мейо (Monge et al., 1964) резектабельность при раке головки поджелудочной железы составила 10%. У отдельных авторов этот показатель выше: у Salembier (1970) — 13%, Doutre с соавт. (1970) — 25%,yElias (1969)-27%.
Панкреатодуоденальная резекция — тяжелое травматическое вмешательство, сопровождающееся высокой послеоперационной летальностью. Enters с соавт. (1961) приводят материалы различных исследователей. По их данным, летальность составляет от 20 до 80%. На 169 операций, произведенных отечественными хирургами к 1968 г. (исключая наблюдения А. А. Шалимова), послеоперационная летальность составила 50%. Лучшие показатели лишь у единичных авторов: Sinith (1965) —7,7%, а из 35 больных, оперированных Warren с соавт. (1968), умер
1 больной.
Пятилетняя выживаемость после данкреатодуоденальной резекции при раке поджелудочной железы очень низкая: от 0 до 10—12%; средняя продолжительность жизни 9—15 мес (А. Н. Великорецкий, 1959; А. В. Смирнов, 1961; Fayos, Lainpe, 1967; Bowden, Pack, 1969, и др.). По данным ОНЦ АМН СССР, резектабельность при раке поджелудочной железы составила 5,4%. В МНИОИ им. П. А. Герцена резектабельность оказалась равной 7,4%, послеоперационная летальность — 48%; средняя продолжительность жизни составила 13 мес. Это объясняет, почему наряду с пропагандой панкреатодуоденальной резекции ее сторонниками высказывается сдержанное или негативное отношение к этому вмешательству. Радикальная или паллиативная операция при раке поджелудочной железы — вопрос, обсуждение которого не сходит со страниц медицинской прессы.
Успехи анестезиологии, получение антибиотиков широкого спектра действия, антиферментная терапия для профилактики и лечения послеоперационного панкреатита, применение эффективных дезинтоксикационных средств и др. дают основание к дальнейшей разработке панкреатодуоденальной резекции.
Операция состоит из двух этапов:
первый включает мобилизацию и удаление препарата,
второй — заключается в восстановлении проходимости желудочно-кишечного тракта и желчных путей. Методика мобилизации достаточно хорошо разработана, близка к стандартизации и подробно представлена в значительном числе монографий и атласов (В. В. Виноградов, 1959; А. А. Шалимов, 1970; В. И. Кочиашвили, 1970). Производится резекция головки поджелудочной железы, общего желчного протока, дпстального отдела желудка и двенадцатиперстной кишки (рис. 120). А. А. Шалимов (1970) в зависимости от степени распространенности процесса применяет два варианта операции:
I — с резекцией двенадцатиперстной кишки до мезентериальных сосудов;
II — с полным удалением двенадцатиперстной кишки после высвобождения ее дистального отрезка из-под мезентериальных сосудов.
Восстановительный этап операции очень вариабелен. Предлагаемые способы реконструкции (более 70) направлены на предупреждение осложнений (холангита, панкреатита и др.).
Ключевым моментом панкреатодуоденальной резекции является обработка культи железы. Метод глухого ушивания культи, разработанный Whipple в 1935 г., не нашел широкого распространения. Более физиологично создание панкреатодигестив-ного соустья. По мнению Е. С, Футоряна и Б. М. Шубина (1975), при определенных показаниях оправдано применение трех вариантов (рис. 121).
1. Наиболее распространенный метод — наложение панкреатоеюноанастомоза. Реконструктивный этап осуществляется путем последовательного (сверху вниз) создания панкреатоди-гестивного, билиодигестивного и желудочно-кишечного соустий. В МНИОИ им. П. А. Герцена применяется методика разобщения первых двух соустий путем прошивания петли кишки между ними с помощью аппарата УКЛ-60. Такая методика предотвращает забрасывание желчи в протоки поджелудочной железы и панкреатического сока в желчные пути, что служит профилактикой послеоперационного холангита и панкреатита.
2. Глухое ушивание культи показано при выраженном вторичном панкреатите с образованием некротических бляшек, когда наложение соустья с кишкой особенно рискованно. В этих случаях целесообразно произвести субтотальную резекцию железы в надежде на малую внешнесекреторную функцию небольшой культи (это уменьшает опасность развития послеоперационных осложнений).
3. Наложение панкреатогастроанастомоза показано при благоприятных анатомических условиях и широкой культе панкреатического протока. При создании соустья оправдано применение временного наружного отведения панкреатического сока.
При раке тела и хвоста железы производится резекция дистального отдела железы обычно вместе с селезенкой. Эти операции крайне редки, так как больные поступают, как правило, в запущенной стадии заболевания. В МНИОИ им. П. А. Герцена метастазы выявлены при этой локализации рака в 96% случаев.
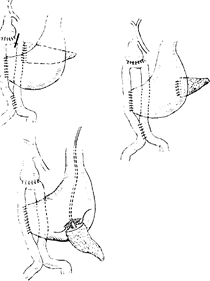

Рис. 120. Границы панкреатодуоденальной резекции.
Рис. 121. Варианты реконструктивного этапа панкреатодуоденальной резекции.
Паллиативное лечение проводится большинству (70—80%) больных раком поджелудочной железы с целью декомпрессии желчных путей или ликвидации гастродуоденальной непроходимости. Применяются различные варианты билиодигестивных соустий (холецистогастроанастомоз, холецистоэнтероанастомоз и др.). В основе решения вопроса о выборе способа декомпрессии желчных путей у онкологических больных в первую очередь должно лежать стремление к созданию наиболее безопасного, мало травматичного и технически легко выполнимого соустья. Этим требованиям, по мнению некоторых авторов, отвечает холецистогастроанастомоз (А. Д. Очкин, 1951; В. В. Шаак^ А. П. Шанин, 1962; В. С. Даценко, 1964, и др.). Другие хирурги (А. Н. Великорецкий, 1959; Я. Д. Витебский, 1971; А. А. Шалимов, 1970; Morgenster et al., 1970) предпочетение отдают желчно-кишечным анастомозам. В МНИОИ им. П. А. Герцена» имеющем опыт более 200 паллиативных операций, накладывают желудочно-пузырное соустье, применяя при этом разработанную Б. М. Шубиным и Е. С. Футоряном (1965) методику временного наружного дренирования желчных путей с помощью управляемого трансназального дренажа (рис. 122). Появились немногочисленные публикации о попытках инфу-зионной внутриартериальной химиотерапии при раке желудоч-но-кишечного тракта через систему чревной артерии (Anstield, 1966; Burrows et al., 1967). В ОНЦ АМН СССР применяется внутриартериальная химиотерапия рака поджелудочной железы через правую желудочно-салышковую артерию. Экспериментальными исследованиями А. Б. Итина (1972) установлено, что при регионарном введении меченого препарата (5-фторурацила) в артерию собак накопление изотопа в ткани головки железы в 18—19 раз и в ткани тела железы в 5—6 раз больше, чем при системном введении препарата. В МНИОИ им. П. А. Герцена разработано два варианта катетеризации.правой желудочно-сальниковой артерии.
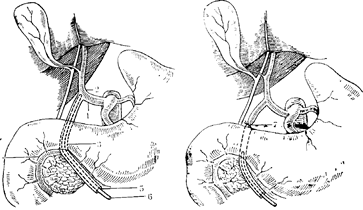
•Рис. 123. Катетеризация правой желудочно-сальниковой артерии для лечебной инфузии печени (а), поджелудочной железы и двенадцатиперстной кишки (б).
1 — общая печеночная артерия; 2 — собственно печеночная артерия-
3 —желудочно-двенадцатиперстная артерия; 4—верхняя поджелудочно-две-надцатиперстная артерия; 5 — правая желудочно-сальниковая артерия; 6 — полиэтиленовая трубка в просвете артерии; 7 — лигатура на желудочно-двенадцатиперстной артерии.
Для создания максимальной концентрации препарата в области головки и двенадцатиперстной кишки целесообразно производить перевязку желудочно-двенадцатиперстной артерии (рис. 123). Для целенаправленной терапии только печени и желчного пузыря катетер продвигают в ствол печеночной артерии. Правильное положение катетера контролируют во время операции введением в артериальное русло 2—3 мл индигокармина, изменяющего окраску органа, а в послеоперационном периоде путем ангиографии (рис. 124). Наблюдения дают основания к продолжению исследований по внутриартериальной химиотерапии рака поджелудочной железы 5-фторурацилом и циклофосфаном. Кроме того, методика катетеризации правой желудочно-сальниковой артерии рекомендуется для проведения внутриартериальных инфузии лекарственных веществ с целью профилактики и борьбы с послеоперационными осложнениями, а также для снятия болевого синдрома при иноперабельном раке.
Летальность после паллиативных операций 15—45% (3. А. Топчиашвили, 1957; А. А. Шалимов, 1970; В. И. Ко-чиашвили, 1970; Helm, 1960; Feduska et al., 1971), продолжительность жизни 8—12 мес (Н. И. Лепорский, 1951; В. А. Ло-бачева, 1969; Реп et al., 1968, и др.).
Date: 2015-10-19; view: 854; Нарушение авторских прав