
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Примеры решения типовых задач. Пример 1. Укажите, с какими из указанных растворов (FeSO4, CuSO4 и Na2SO4) будет взаимодействовать никель при стандартных условиях?
|
|
Пример 1. Укажите, с какими из указанных растворов (FeSO4, CuSO4 и Na2SO4) будет взаимодействовать никель при стандартных условиях? Приведите уравнения возможных реакций.
Решение. Возможность взаимодействия металла с раствором соли и вытеснения из данного раствора металла, входящего в эту соль, можно определить на основании значений стандартных электродных потенциалов металлов (ряд напряжений). Каждый металл этого ряда вытесняет (восстанавливает) из растворов солей только те металлы, ионы которых расположены за ним, т.е. имеют более высокие значения электродных потенциалов. Из табличных данных (Прил., табл. 12) находим значения E o Меn+ / Me для никеля и металлов, ионы которых входят в состав солей: E oNi2+ / Ni=−0,25 B; E o Fe2+ / Fe=−0,44 B; E oCu2+/ Cu=+0,34 В; E oNa+/ Na=−2,71 B.
Следовательно, из предлагаемых растворов солей никель способен вытеснить только медь, так как E oCu2+/ Cu> E oNi2+ / Ni.
Уравнение реакции имеет вид:
Ni + CuSO4 ↔ NiSO4 + Cu,
восстановитель ½Ni  Ni2+ + 2
Ni2+ + 2 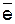 (процесс окисления);
(процесс окисления);
окислитель ½Cu2+ + 2 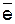
 Cu (процесс восстановления).
Cu (процесс восстановления).
Пример 2. Рассчитайте электродный потенциал меди, находящейся в растворе сульфата меди с концентрацией ионов [Cu2+ ]=0,001 моль/л.
Решение. Электродный потенциал металла вычисляется по уравнению Нернста. В табл. 12 приложения находим значение стандартного электродного потенциала E oCu2+/Cu =+0,34 В.
E Cu2+/ Cu =+0,34 +  =0,25 В.
=0,25 В.
Пример 3. Вычислите электродный потенциал для водородного электрода при температуре 25 оС и парциальном давлении Н2 1 атм, рН которого равен 3.
Решение. Уравнение Нернста для расчета потенциала водородного электрода в разных средах:  =−0,059рН. Вычисляем потенциал водородного электрода при рН=3.
=−0,059рН. Вычисляем потенциал водородного электрода при рН=3.  =−0,059
=−0,059  3=−0,017 В.
3=−0,017 В.
Пример 4. Вычислите потенциал кислородного электрода в растворе с концентрацией ионов [Н+]=10-1 моль/л при температуре 25 оС и парциальном давлении О2 1 атм.
Решение. Уравнение Нернста для расчета потенциала кислородного электрода в разных средах:
Е O2+2H2O / 4OH- = Е оO2+2H2O / 4OH-+0,059рОН.
Учитывая, что рН+рОН=14 и рН=− lg[H+], рассчитываем потенциал кислородного электрода: Е O2+2H2O / 4OH- =0,4+0,059х13=1,167 В.
Пример 5. Рассчитайте ЭДС гальванического элемента Fe/ Fe(NO3)2 IIAgNO3/Ag при концентрации раствора Fe(NO3)2, равной 0,1 моль/л и концентрации раствора [AgNO3]=0,001 моль/л.
Решение.
E Fe2+ / Fe = −0,44+  lg10-1=0,44+(−0,0295)=–0,4695 B;
lg10-1=0,44+(−0,0295)=–0,4695 B;
E Ag+ / Ag = +0,8+0,059 lg10-2 =+0,682 B.
Следовательно, железный (Fe) электрод является анодом, серебряный (Ag) – катодом. ЭДС= Е к– Е а=+0,682–(–0,4695)=1,1515 В.
Date: 2015-10-19; view: 757; Нарушение авторских прав