
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Химические свойства аминокислот
|
|
Поскольку свойства белков во многом определяются химическими свойствами аминокислот, целесообразно более подробно остановиться на их кислотно-основных свойствах. Аминокислоты обладают довольно высокой химической активностью. Как и карбоновые кислоты, производными которых они являются, аминокислоты диссоциируют в водном растворе. Отщепляя один ион водорода (протон), карбоксильная группа образует анион:
R-СН(NH2)-СООН → R— СН(NH2)—СОО- + Н+.
В то же время аминогруппа может присоединять протон собразованием катиона:
R—СН(NH2)—СООН + Н+→ R(NH3+)—СН—СООН.
Однако характер ионизации аминокислот зависит от рН раствора. В щелочной среде усиливается диссоциация карбоксильной группы, а аминогруппа практически не диссоциирует:
NH2-СН2—СООН + ОН- → NH2-СН2—СОО- + Н2О.
В кислой среде, наоборот, происходит ионизация аминогруппы, в то время как карбоксильная группа не диссоциирует;
NH2-CH2COOH +H+ → NH3+-СН2—СООН.
Из приведенных уравнений видно, что в щелочной среде аминокислота существует в виде аниона, в кислой — в виде катиона. В электрическом поле анионы и катионы отдельных аминокислот будут перемещаться соответственно к аноду и катоду. При некотором промежуточном значении рН может происходить одновременная диссоциация карбоксильной и протонизация аминной групп. В результате образуется биполярный ион (цвиттер-ион), суммарный заряд которого равен нулю;
NH2-СН2-СООН → NH3+-CH2COO-.
Такой смешанный ион не перемещается в электрическом поле. Значение рН, при котором молекула аминокислоты не имеет заряда, называется изоэлектрической точкой аминокислоты. Исходя из вышеизложенного, аминокислоты следует рассматривать как амфотерные электролиты. Они взаимодействуют со щелочами:
NH2-RСН-СООН + NaOH → NH2-RСН—COONa + Н2О,
с кислотами:
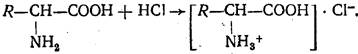
Кроме того, они могут образовывать сложные эфиры:
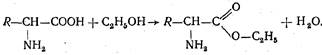
Характерными для аминокислот являются реакции декарбоксилирования и дезаминирования:
NH2-RСН-СООН → R—СН2—NH2 + СО2;
NH2 —RCH— СООН + Н2О →-R—СНОН—СООН + NH3.
Они также взаимодействуют друг с другом с образованием ди-, три-и полипептидов:
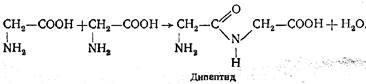
Соединяясь таким образом между собой, аминокислоты образуют полимерные цепи, которые и представляют собой основу строения белковой молекулы.
Date: 2015-09-22; view: 2079; Нарушение авторских прав