
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Химические свойства
|
|
Реакции нуклеофильного замещения
Ацилгалогениды легко реагируют с различными нуклеофильными реагентами, причем эти реакции не требуют катализа. Общая схема этих реакций может быть представлена уравнениями
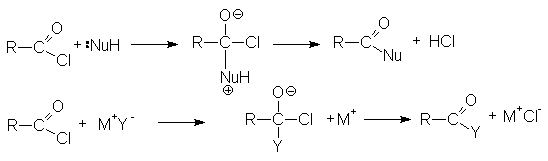 Галогенангидриды — сильные электрофильные реагенты, сильнее карбоновых кислот. Галоген в этих соединениях обладает исключительно большой подвижностью. Электрофильные свойства подобных соединений зависят от величины дробного положительного заряда на углероде карбонильной группы. Со стороны галогена проявляется выраженный который в статическом состоянии больше, поэтому на атоме углерода возникает выраженный что и обуславливает сильные электрофильные свойства галогенангидридов. Они легко вступают в реакции нуклеофильного замещения. В подобных реакциях в молекулу нуклеофила вводится ацильная группа, поэтому такие реакции называют реакциями ацилирования, а галогенангидриды карбоновых кислот — цилирующими агентами.
Галогенангидриды — сильные электрофильные реагенты, сильнее карбоновых кислот. Галоген в этих соединениях обладает исключительно большой подвижностью. Электрофильные свойства подобных соединений зависят от величины дробного положительного заряда на углероде карбонильной группы. Со стороны галогена проявляется выраженный который в статическом состоянии больше, поэтому на атоме углерода возникает выраженный что и обуславливает сильные электрофильные свойства галогенангидридов. Они легко вступают в реакции нуклеофильного замещения. В подобных реакциях в молекулу нуклеофила вводится ацильная группа, поэтому такие реакции называют реакциями ацилирования, а галогенангидриды карбоновых кислот — цилирующими агентами.
Галогенангидриды в силу своей высокой активности нашли чрезвычайно большое применение в органическом синтезе.
Важными реакциями нуклеофильного замещения по ацильному углероду являются:
-
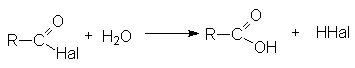 Гидролиз
Гидролиз
-
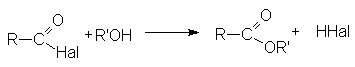 Взаимодействие со спиртами (этерификация)
Взаимодействие со спиртами (этерификация)
-
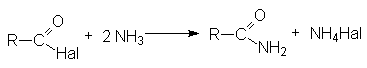 Взаимодействие с аммиаком и аминами (аммонолиз)
Взаимодействие с аммиаком и аминами (аммонолиз)
- Взаимодействие с гидразином и его производными
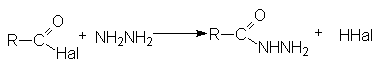
- Взаимодействие с металлоорганическими соединениями
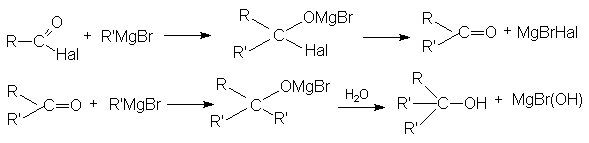
По этому суммарно реакцию можно представить следующей схемой
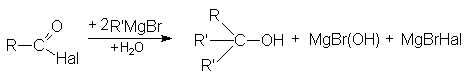
Реакции восстановления
- Восстановление натрийборгидридом или литийалюминий гидридом.
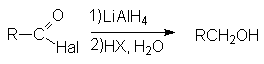
- Восстановление по Розенмунду
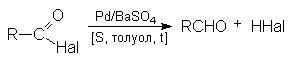
Реакция с диазометаном (реакция Арндта-Эйстерта)
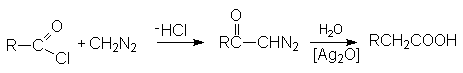
Эта реакция является синтетическим средством увеличения длины углеводородных цепей органических соединений на один атом углерода.
Номенклатура, ізомерія, способи добування галогенозаміщених карбонових кислот. Кислотні властивості та їх залежність від кількості та розміщення галогену у вуглеводневому радикалі.
Галогенкарбоновыми кислотами называют производные карбоновых кислот, которые в углеводородном радикале содержат один или несколько атомов галогена.
По природе углеводородного радикала различают алифатические, алициклические и ароматические галогенкарбоновые кислоты.
Алифатические галогенокарбоновые кислоты по взаимному расположению атома галогена и карбоксильной группы делятся на: а,?, Y, А и т. д. К гетерофункциональным карболовым кислотам относятся производные карбоновых кислот, в углеволоролном радикале которых один или несколько атомов водорода заметены на другие атомы или атомные группы: галоген, гидроксигруппу, альдегидную группу, кетонную группу, аминогруппу. Гетерофункциональные карбоновые кислоты — это бифункциональные соединения, они обладают свойствами карбоновых кислот и свойствами того класса органических соединений, который определяет заместитель в углеводородном радикале.
Название галогенкарбоновые кислоты производят от назв. карбоновых кислот с указанием числа атомов галогена и их положения относительно карбоксильной группы, например С1СН2СООН-хлоруксусная к-та, СН2С1СНС1СООН - 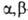 -дихлорпропионовая.
-дихлорпропионовая.
Способы получения галогенокарбоновых кислот.
1. Действие галогенов на органические кислоты.
2. Реакция Геля — Фольгарда — Зелинского. Это г способ имеет большое значение. Он заключается в действии галогена на предельные карбоновые кислоты в присутствии фосфора. Реакция Геля — Фольгарда — Зелинского осуществляется значительно легче, чем в предыдущем случае. На первой стадии образуется бромангирид уксусной кислоты. Бром в значительной степени усиливает смещение электронной плотности oт а-углеродного атома. Водороды при углеродном атоме становятся более подвижны и легко замешаются на галоген. Образовавшийся бромангидрид бромуксусной кислоты при взаимодействии с водой образует бром уксусную кислоту.
Галогенокарбоновые кислоты более сильные кислоты, чем карбоновые. Введение галогенов в молекулу увеличивает силу кислот. Сила кислот зависит от величины дробного положительного заряда на атоме углерода карбоксильной группы. А величина 6+ увеличивается с введением галогенов, которые обладают отрицательным индуктивным эффектом.
Например, трихлоруксусная кислота по силе приравнивается к серной кислоте. Значит, сила кислоты зависит от количества атомов галогена в углеродном радикале. Кроме того, сила кислоты зависит от положения галогена в цепи. Поскольку индуктивное смешение эффективно на протяжении четырех — пяти G-связей,галогенокарбоновые кислоты более сильные, чем?-, a?— сильнее, чем у-галогенокарбоновые кислоты.
Для галогенокарбоновых кислот характерны реакции по карбоксильной группе и реакции с участием атома галогена.
По карбоксильной группе они образуют все функциональные производные карбоновых кислот: соли, сложные эфиры, ангидриды, галогенангидриды, амиды и др. Алифатические галогенокарбоновые кислоты, подобно галогеналканам, вступают в реакции замещения галогена по механизму нуклеофильного замещения. Причем, подвижность галогена зависит от взаимного расположения галогена и карбоксильной группы. Карбоксильная группа, как электроакцепторная группа, увеличивает подвижность атома галогена в молекуле. Галоген в положении менее подвижен, а положении влияние карбоксильной группы практически не сказывается.
Галогенокарбоновые кислоты находят широкое применение для получения окси- и аминокислот, широко используются в органическом синтезе лекарственных препаратов, бромизовалериановой кислоты — бромизовал — это снотворный препарат.
Date: 2015-07-27; view: 1439; Нарушение авторских прав