
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Класифікація, номенклатура та способи добування дикарбонових кислот. Хімічні властивості дикарбонових кислот як біфункціональних сполук
|
|
Дикарбоновыми кислотами называют производные углеводородов, содержащие в своем составе две карбоксильные группы. По заместительной номенклатуре название дикарбоновых кислот строят исходя из соответствующих углеводородов с добавлением множительной приставки ди- и суффикса -овая кислота.
Наряду с заместительной номенклатурой широко применяются тривиальные названия. 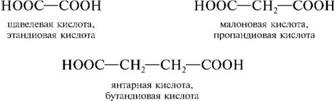
Способы получения дикарбоновых кислот.
Дикарбоновые кислоты получают теми же методами, что и монокарбоновые кислоты, используя в качестве исходных веществ соответствующие бифункциональные соединения.
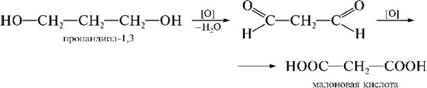
Окисление двуперничных гликилей, диальегидов и гидроксикислот. Одной из важных реакций получения дикарбоновых кислот является реакция омыления дигитридов.
Окисление двухатомных спиртов - гликолей: НО-СН2-СН2-ОН + [О] -> НООС-СООН + Н2O
Имея в своем составе две карбоксильные группы, дикарбоновые кислоты диссоциируют ступенчато, образуя анион (рКд,) и дианион (рКа2).
Высокая кислотность по первой ступени объясняется взаимным влиянием второй карбоксильной группы, которая способствует делокализации образующегося отрицательного заряда карбоксилат-иона и гем самым повышает его устойчивость. По мере удаления карбоксильных групп ослабевает их взаимное влияние и кислотность по первой ступени падает. Отрыв протона от второй карбоксильной группы происходит труднее вследствие низкой стабильности дианиона, поэтому кислотность дикарбоновых кислот по второй ступени значительно ниже, чем по первой.
При максимальном удалении карбоксильных групп последние не оказывают взаимного влияния и через 5-6 связей каждая из них ведет себя независимо.
Date: 2015-07-27; view: 1025; Нарушение авторских прав