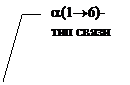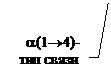Главная
Случайная страница
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?
Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника
|
Метаболизм глюкозы в клетках
В клетки тканей организма глюкоза может поступать как экзогенная из пищи, так образованная эндогенно из депонированного гликогена (в результате гликогенолиза) или из других субстратов, таких как лактат, глицерол, аминокислоты (в результате глюконеогенеза). Всосавшаяся в тонкой кишке глюкоза поступает через воротную вену в печень и попадает в гепатоциты. По своей природе глюкоза является гидрофильным веществом, следовательно она не может свободно поникнуть через фосфолипидную мембрану. Механизм ее транспорта осуществляется с помощью белков-переносчиков. При стимуляции инсулином наблюдается увеличение содержания этих белков в плазматических мембранах в 5-10 раз при одновременном уменьшение их одержания на 50-60% внутри клетки. Для стимуляции передвижения белков-переносчиков к мембране требуется дальнейшее стимулирующие влияние инсулина. На сегодняшний день выделено два класса транспортеров глюкозы:
· Na-глюкозный котранспортер, который экспрессируется специальными эпителильными реснитчатыми клетками тонкой кишки и проксимальным отделом почек. Этот белок осуществляет активный транспорт глюкозы из просвета кишки или нефрона против градиента концентрации путем связывания глюкозы с теми ионами натрия, которые транспортируются ниже градиента концентрации.
· Собственные транспортеры глюкозы. Это мембранные белки, находящиеся на поверхности всех клеток и осуществляющие транспорт глюкозы ниже градиента концентрации. Транспортеры глюкозы осуществляют перенос глюкозы не только в клетку, но и из клетки и также участвуют во внутриклеточном передвижении глюкозы. В настоящее время описано 6 транспортных белков для глюкозы – GluT.
В клетках глюкоза фосфорилируется в гексокиназной реакции, превращаясь в глюкозо-6-фосфат (Гл-6-Ф), Гл-6-Ф является субстратом нескольких путей метаболизма: с этой молекулы начинается синтез гликогена, пентозофосфатный цикл, гликолитический распад до лактата или аэробное полное расщепление до СО2 и Н2О. В клетках, способных к глюконеогенезу (клетки печени, почек, кишечника), Гл-6-Ф может дефосфорилироваться и в виде свободной глюкозы поступать в кровь и переноситься в другие органы и ткани.
Особенно важна глюкоза для клеток мозга. Клетки нервной системы зависят от глюкозы как от основного энергетического субстрата. В то же время в мозге нет запасов глюкозы, она там не синтезируется, нейроны не могут потреблять другие энергетические субстраты, кроме глюкозы и кетоновых тел, глюкоза практически полностью может исчерпываться из внеклеточной жидкости, так как клетки нервной системы потребляют глюкозу инсулин-независимым путем.
Гликоген. Из Гл-6-Ф в результате сочетанного действия гликогенсинтетазы и «ветвящего» фермента синтезируется гликоген - полимер, напоминающий по виду дерево. В молекуле гликогена может содержаться до миллиона моносахаридов. При этом происходит как бы кристаллизация гликогена и он не обладает осмотическим эффектом. Такая форма пригодна для хранения в клетке. Если бы такое количество молекул глюкозы было растворено, то из-за осмотических сил клетку бы разорвало. Гликоген является депонированной формой глюкозы и энергии. Он содержится практически во всех тканях, в клетках нервной системы его минимальное количество, в печени и мышцах его особенно много. Гликоген содержит только 2 типа гликозидных связей: a(1®4)-тип и a(1®6)-тип. Связь a(1®4)-тип формируется через каждые 8-10 остатков D-глюкозы (рис 4).
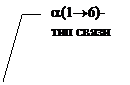  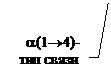 
|
Рис. 4. Структура гликогена.
За счет a(1®4)- и a(1®6)-гликозидных связей формируется ветвистая молекула гликогена, содержащая до 1 млн. остатков D-глюкозы
|
Гликогенолиз. Это путь расщепления гликогена. Гликоген в организме в основном сохраняется в печени и скелетных мышцах. Гликоген мышц используется в качестве источника энергии при интенсивной физической нагрузке. Гликогенолиз в печени активируется в ответ на снижение глюкозы при перерывах в приеме пищи или как стрессовая реакция. Основными гормонами, активирующими гликогенолиз, являются глюкагон, адреналин (эпинефрин) и кортизол (таблица 2).
Таблица 2
| Гормональная регуляция гликогенолиза
| | Гормон
| Место образования
| Инициатор
| Эффект на гликогенолиз
| | Глюкагон
| a-клетки поджелудочной железы
| гипогликемия
| быстрая активация
| | Адреналин
| мозговой слой надпочечника
| стресс,
гипогликемия
| быстрая активация
| | Инсулин
| b-клетки поджелудочной железы
| гипергликемия
| подавление
|
Гликогенолиз начинается с отщепления концевых остатков глюкозы по связям a(1®4), в этом процессе ключевым ферментом является гликогенфосфорилаза (рис 5.). Активация фосфорилазы осуществляется фосфорилированием с участием цАМФ-зависимой протеинкиназы и киназы фосфорилазы. Контролируют активацию фосфорилазы катехоламины (печень, мышцы) и глюкагон (печень). Эти гормоны способствуют расщеплению гликогена в печени и тем самым гипергликемическому ответу. Продуктом фосфорилазной реакции является глюкозо-1-фосфат (Г-1-Ф), который превращается в Г-6-Ф при участии фермента фосфоглюкомутазы. В печени глюкоза образуется из Г-6-Ф и Г-1-Ф при участии соответственно ферментов Г-6-Фтазы и Г-1-Фтазы. Фермент фосфорилаза специфичен только для связей a(1®4). Он расщепляет гликоген до тех пор, пока в конце ветви не останется 3-4 углеводных остатка. Затем действует ферментный комплекс из трансглюкозилазы и глюкозидазы. Первый из этих ферментов переносит (транслоцирует) короткий сегмент углеводных остатков в конец цепи a(1®4), второй отщепляет глюкозу по связи a(1®6). Цикл с участием фосфорилазы и ферментного комплекса, разрушающего ветвления гликогена, повторяется. Около 90 % глюкозы освобождается из гликогена в виде Г-1-Ф при разрушении связи a(1®4), 10 % в виде свободной глюкозы при разрушении связи a(1®6). Глюкоза может образовываться из гликогена при участии амило-1,6-глюкозидазы, расщепляющей боковые цепи гликогена.
     | мышцы V тип,
печень - VI тип
| |        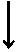 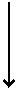 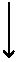  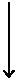 
|
Рис. 5. Дефекты ферментов метаболизма гликогена, приводящих к гликогенозам разного типа.
| Гликогенозы. Это группа наследственных заболеваний, связанных с дефектами ферментов, при которых нарушен распад гликогена (рис. 5) и, несмотря на огромный запас гликогена в органах, у больных детей развивается гипогликемия (таблица 3).
Таблица 3.
| Гликогенозы - болезни накопления гликогена
| | Тип
| Название болезни
| Дефект фермента
| Структурные и клинические проявления дефекта
| | I
| von Gierke’s
(Гирке)
| глюкозо-6-фосфатаза
| тяжелая постабсорбционная гипогликемия, лактоацидоз, гиперлипидемия
| | II
| Pompe’s
(Помпе)
| лизосомальная a-глюкозидаза
| гранулы гликогена в лизосомах
| | III
| Cori’s
(Кори)
| трансглюкозилаза/
глюкозидаза
| измененная структура гликогена, гипогликемия
| | IV
| Andersen’s
(Андерсен)
| «ветвящий» фермент
| измененная структура гликогена
| | V
| McArdle’s
(Мак-Ардль)
| мышечная фосфорилаза
| отложение гликогена в мышцах, судороги при физической нагрузке
| | VI
| Hers’
(Геру)
| фосфорилаза печени
| гипогликемия, но не такая тяжелая, как при I типе
| Наиболее изучена болезнь Гирке (гликогеноз I типа), при этом заболевании блокировано расщепление гликогена из-за отсутствия фермента глюкозо-6-фосфатазы, структура гликогена нормальная. Нарушено образование свободной глюкозы, образуется много лактата. Гипогликемия приводит к активации жирового обмена, окисление липидов сопровождается образованием кетоновых тел. Гипогликемия проявляется ярко при определении глюкозы в крови глюкозоксидазным и гексокиназным методами, в то время как редуктометрическим методом по Хагедорну из-за присутствия в крови восстанавливающих веществ результаты определения глюкозы значительно искажаются. Велика ценность адреналиновой и глюкагоновой пробы, так как адреналин и глюкагон не повышают уровень глюкозы в крови из-за неспособности печени поставлять свободную глюкозу из гликогена.
ИСТОРИЯ БОЛЕЗНИ № 1
БОЛЕЗНЬ ГИРКЕ (ГЛИКОГЕНОЗ ПРИ ДЕФИЦИТЕ Г-6-Фазы)
Девочка 6 месяцев постоянно капризничала, имела болезненный вид, быстро утомлялась, впадала в сонливость, у нее часто возникали расстройства пищеварения, наблюдалось значительное увеличение печени.
Лабораторный анализ:
Глюкоза в крови (через 1 ч после кормления) - 3,5 ммоль/л (референтный диапазон» 5 ммоль/л)
Через 4 ч после кормления на фоне признаков болезненного состояния при пульсе 110 в 1 мин уровень глюкозы составил 2 ммоль/л. Симптомы снимались после еды. Биопсия печени показала массивные отложения гликогена в цитоплазме гепатоцитов.
Поставлен диагноз - болезнь Гирке. Лечение включало частые кормления с уменьшением углеводов в пище и питание через назогастральный зонд по ночам.
ИСТОРИЯ БОЛЕЗНИ № 2
БОЛЕЗНЬ МАК-АРДЛЯ (ГЛИКОГЕНОЗ СО СНИЖЕНИЕМ МЫШЕЧНОЙ СИЛЫ)
30-летний мужчина консультировался у врача по поводу хронических болей в мышцах ног и рук и судорог при физической нагрузке. У него отмечалась слабость в мышцах, поэтому он никогда не занимался спортом. Состояние не менялось до тех пор, пока он не решил укрепить мышцы, занимаясь спортом. При упорных физических упражнениях боли, как правило, проходили через 15-30 мин тренировки, и он мог дальше заниматься упражнениями.
Лабораторный анализ:
При лабораторном исследовании установлено, что при умеренной физической нагрузке уровень глюкозы в крови был нормальным, но повышенным была активность ММ фракции креатинкиназы (ММ-КК), что свидетельствует о повреждении мышц. При интенсивной мышечной работе уровень глюкозы в крови незначительно уменьшался, но при этом снижался и уровень лактата. Биопсия показала необычно высокое содержание гликогена в мышцах, что доказывает болезнь накопления гликогена.
Обсуждение:
В начальный период мышечной нагрузки всегда начинает интенсивно потребляться глюкоза, которая образуется из распадающегося гликогена. Однако при судорогах, возникающих при кислородной задолженности, в результате активации гликолиза должно происходить образование пирувата, который превращается в лактат и поступает в кровь. В этом же случае не было увеличения лактата, что доказывает нарушение мобилизации мышечного гликогена. Прекращение мышечных болей через 0,5 ч после нагрузки объясняется физиологической реакцией, вызванной освобождающимся при нагрузке адреналином, который способствует поступлению в мышцы из крови глюкозы и жирных кислот, компенсирующих недостаточное поступление глюкозы из мышечного гликогена.
Гликолиз. В анаэробных условиях гликлиз - основной метаболический путь расщепления глюкозы. В этом процессе при распаде 1 молекулы глюкозы образуется 2 молекулы АТФ и 2 молекулы пирувата. В тканях, где не обеспечивается полностью синтез АТФ за счет окислительного фосфорилирования, глюкоза является основным источником энергии. При интенсивной мышечной работе в мышцах углеводы расщепляются до лактата, вызывая, так называемую, кислородную задолжность и приводя к внутриклеточному закислению. Ряд лекарственных препаратов, в частности бигуаниды, сульфонилмочевинные препараты первой генерации, активируют гликолиз, поэтому при диабете могут быть дополнительными факторами, способствующими развитию лактоацидоза. В связи с этим, наряду с определением параметров КОС и газов крови, в экспресс-лабораториях при реанимационных отделениях рекомендуется определение лактата у больных с развивающейся гипоксией. Ингибиторами гликолиза являются монойодацетат и NaF - сильнодействующие яды. В эритроцитах гликолиз и пентозофосфатный цикл являются основными путями утилизации глюкозы, интенсивность их высокая, поэтому не рекомендуется при определении глюкозы оставлять сгусток с сывороткой или измерять глюкозу в стабилизированной ЭДТА крови более чем через 1 час. При необходимости хранить кровь рекомендуется использовать в качестве ингибитора гликолиза монойодацетат или NaF.
Аэробное окисление глюкозы. Глюкоза является одним из основных энергетических субстратов в организме. Скорость ее окисления в состоянии покоя натощак составляет около 140 мг/кг массы в течение 1 часа. Некоторые жизненно важные органы, в частности кора головного мозга, используют в качестве энергетического субстрата исключительно глюкозу. В процессе окисления она превращается через гликолитический путь обмена в пируват, который поступает в митохондрии, где декарбоксилируется до ацетил-коА. Дальнейшее окисление происходит в цикле Кребса и процессе окислительного фосфорилирования, в котором синтезируется АТФ и образуется эндогенная вода. Это основной путь образования энергии: 1 молекула глюкозы в процессе аэробного окисления дает возможность синтезироваться в 19 раз больше АТФ, чем при гликолизе, то есть 38 молекул АТФ Окисление глюкозы в аэробных условиях - наиболее эффективный путь использования кислорода для энергетических нужд. Эффективность основного обмена наиболее высока, когда окисляется глюкоза, поэтому она является важным компонентом при парентеральном питании.
Пентозофосфатный шунт. Биологическая роль этого цикла состоит в образовании пентозофосфатов, необходимых для синтеза нуклеиновых кислот, для генерирования восстановленных эквивалентов в виде НАДФН для синтеза жирных кислот и для обеспечения антиоксидантной системы клеток. Среди дефектов пентозофосфатного шунта наиболее распространен дефицит или аномалии фермента глюкозо-6-фосфатдегидрогеназы. При этом не обеспечивается необходимое восстановление глютатиона. В мембране эритроцитов активируется перекисное окисление, накапливаются гидроперекиси, нарушается проницаемость клеточной мембраны, в результате наступает гемолиз.
Взаимосвязь между углеводным, белковым и липидным обменами. Важным общим промежуточным продуктом метаболизма углеводов, аминокислот и липидов является в клетках молекула ацетил-коА. Через ацетил-коА глюкоза и другие углеводы могут превращаться в жирные кислоты и триглицериды, в заменимые аминокислоты и наоборот глюкоза может синтезироваться через эту молекулу. Через пути взаимопревращений при разном питании организм синтезирует необходимые компоненты. Поэтому даже при исключительно углеводном питании может увеличиться масса жировой ткани. После приема пищи, также как после приема углеводов, не рекомендуется исследовать базальный уровень глюкозы в крови. Практически постоянно при гипертриглицеридемии имеется склонность к нарушению углеводного обмена вследствие развития инсулинорезистентности.
Глюконеогенез. Так называется метаболический процесс синтеза глюкозы из аминокислот и продуктов промежуточного обмена веществ. В процессе глюконеогенеза протекают те же реакции, что в гликолизе, но в обратном направлении. Исключение составляют 3 реакции, которые шунтируются. Полный набор ферментов глюконеогенеза содержится в клетках печени, почек, слизистой кишечника. Глюкокортикоиды, в частности кортизол, являются мощными стимуляторами синтеза ферментов глюконеогенеза, вызывая гипергликемию, за счет синтеза глюкозы из аминокислот при катаболизме белков.
РЕГУЛЯЦИЯ УГЛЕВОДНОГО ОБМЕНА.
Уровень глюкозы в крови является важнейшим фактором гомеостаза. Он поддерживается на определенном уровне функцией кишечника, печени, почек, поджелудочной железы, надпочечников, жировой ткани и других органов (рис. 6).
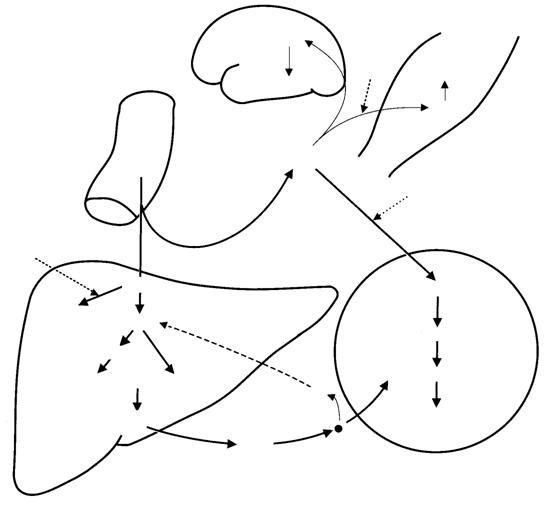
Рис. 6. Метаболизм глюкозы после еды. Всосавшаяся в кишечнике глюкоза поступает в печень. Печень поддерживает постоянную доставку энергетических субстратов для других органов, в первую очередь для мозга. Поступление глюкозы в печень и мозг не зависит от инсулина, в мышцы и жировую ткань - инсулинзависимое. Во всех клетках первый этап метаболизма глюкозы - фосфорилирование. В печени инсулин стимулирует фермент глюкокиназу, инициируя образование гликогена. Избыток глюкозо-6-фосфата используется для синтеза аминокислот и липидов. В мышцах глюкоза запасается в виде гликогена, в жировой ткани переходит в триглицериды, в мозговой ткани глюкоза используется как энергетический субстрат.
Выделяют несколько типов регуляции углеводного обмена: субстратную, нервную, гормональную, почечную.
Date: 2015-07-17; view: 2210; Нарушение авторских прав | Понравилась страница? Лайкни для друзей: |
|
|