
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

III. Идентификация выделенных алкалоидов.
|
|
С этой целью могут быть использованы как хим., так и ф.-х. методы анализа. План судебно-хим. иссл-ния на наличие алкалоидов включает следующие этапы: 1. Анализ начинают с общеалкалоидных осадительных р-ций в кач-ве предварительных групповых проб. 2. Затем проводят ХТС-скрининг - также в кач-ве предварит. теста, но более специфичного благодаря индивидуальным величинам Rf для отдельных алк-дов. 3. Далее выполняют частные р-ции на отдельные алк-ды – р-ции окрашивания и микрокристалличес. р-ции. 4. Снимают спектральные хар-ки алк-дов в УФ и ИК-областях спектра. 5. Для некот. алкалоидов проводят фармакологические пробы.
1) Исследование с общеалкалоидными осадительными реактивами. проводится в качестве предварит. испытаний на наличие алк-дов. Применение этих реактивов основано на св-ве алк-дов давать даже в разбавленных р-рах простые или комплексные соли с некот. к-тами, солями тяж. металлов, комплексными иодидами и рядом др. соед-ний. Общеалкалоидные осадительные реактивы делят на 2 группы: 1. Реактивы, дающие с алкалоидами простые соли: р-р таннина, пикриновая, пикролоновая и некот. др.орг. к-ты. 2. Реактивы, дающие с алк-дами комплексные соед-я, к-е делятся на 2 подгруппы: а) реактивы, содержащие в своем составе металлоиды: I2/KI - реактив Бушарда-Вагнера; H3PO4·12Mo·O3 - фосфорномолибденовая к-та (реактив Зонненшейна); H3PO4 ·12WO3 ·2H2O- фосфорновольфрамовая к-та(реактив Шейблера). б) реактивы, содержащие в своем составе металлы: BiI3/KI - реактив Драгендорфа (K[BiI4]); CdI2/KI - реактив Марме (K2[CdI4]); HgI2/KI – реак. Майера (K2[HgI4]); H2[PtCl6] - платинохлористовод-ная к-та: H[AuCl4] - золотохлористоводородная к-та.
Обычно предварит. испытания на наличие алк-дов проводят с 2-3 общеалк. реактивами, чтобы получить достоверные рез-ты. Р-ции выполняются с солями алк-дов. Для того чтобы перевести алкалоид-основание, в виде к-го он выделяется из био. мат-ла, в алкалоид-соль, остаток после испарения хлороформа раств-ют в 1-2 каплях 0,1Н р-ра НСl. При наличии алк-дов набл-ся выпадение осадков или помутнение капли.
Судебно-хим. оценка р-ций. Р-циям с общеалк. осадительными реактивами придается т-ко отрицат. судебно-хим. значение.Отриц. рез-тат р-ций дает право судебному химику сделать заключение о ненахождении алк-дов и исключить их из дальнейшего иссл-ния.
Положит. рез-тат, свидетельствует о присутствии в исслед. объекте либо алк-дов, либо других азотсодержащих в-в основного хар-ра, и требует проведения подтверждающих испытаний.
2) ХТС-скрининг алкалоидов более специфичен по сравнению с общеалк. осадит. р-циями, хотя ему также придается ориентирующее значение в связи с неспецифичностью реагентов-проявителей алк-дов на хроматограмме. Хроматографирование проводится в тонком закрепленном слое силикагеля. В кач-ве подвиж. фазы исп-ся системы растворителей: 1) диоксан - хлороформ - ацетон - 25% раствор аммиака (47,5: 45: 5: 2,5); 2) толуол - ацетон - этанол - 25% раствор аммиака (45: 45: 7,5: 2,5) (в экспресс-анализе интоксикаций, вариант ВЭТСХ). Детектирование алк-дов проводится реактивом Драгендорфа. В зонах расположения в-в появляются красно-оранж. пятна. Идентиф-цию алк-дов по вел-не Rf (фактор удерживания – отношение расстояний) относительно метчиков. В кач-ве метчиков исп-ют хлороформные р-ры стандартных в-в с опред. конц-цией. ХТС-скринингу придается отриц. судебно-хим. значение. При отсутствии пятен на хроматограмме можно сделать заключ. о ненахождении алк-дов и др. азотсод-щих ЛВ основного хар-ра и исключить их из дальнейшего хода иссл-ния. Совпадение вел-ны Rf испытуемого в-ва с вел-ной Rf метчика дает возможность сделать предварит. заключение об их идентичности. Последующее подтверждение присутствия алк-да проводится более специфичными реакциями и методами.
3) В качестве подтверждающих р-ций после хроматограф. иссл-ния исп-ют р-ции окрашивания и микрокристаллические реакции.
а) Реакции окрашивания. Чаще всего для реакций окрашивания используются: Конц. серная кислота; Конц. азотная к-та; Конц. серная к-та + конц. азотная к-та (реактив Эрдмана); Конц. серная к-та + формальдегид (реактив Марки); Конц. серная к-та + молибденовая к-та (реактив Фреде); Конц. серная к-та + ванадиевая к-та (реактив Манделина). Реакции окрашивания выполняются с основаниями алк-дов. Соответствующий реактив наносится на сухой остаток после испарения хлороформного извлечения. Р-ции окрашивания м. б. специфичными для некот. алк-дов (бруцин, вератрин), или могут давать возможность обнаружения группы алк-дов (н-р, реактив Марки явл-ся групповым на опийные алк-ды).
б) Микрокристаллические р-ции. Они основаны на спос-сти алк-дов образовывать кристаллы характерной формы при взаим-вии с некот. к-тами (пикриновой, пикролоновой, платино- и золотохлористоводородной – H2PtCl6, HAuCl4), солями тяж. металлов и комплексными йодидами. Судебно-хим. оценка метода. Микрокрист. р-ции обладают высокой чувств-стью, надежностью и доказательностью. Рез-ты их наглядны, они м. б. зафиксированы в виде фотографий и представлены судебно-следственным органам в кач-ве приложения к акту судебно-хим. экспертизы. Недостатки: при иссл-нии био. мат-ла присутствие соэкстрактивных в-в приводит к появлению кристаллов нехарактерной формы, нарушаются кристаллооптические константы, отмечается полиморфизм (присутствие одновременно кристаллов различ. форм), поэтому требуется высокая степень чистоты выделенных в-в. Значительное влияние на надежность метода оказывает квалификация химика, навык в выполнении этих реакций.
4. УФ и ИК спектроскопия явл-ся одним из наиб. важных способов идентификации алк-дов. Для доказ-ва алк-дов, выделенных из био. мат-ла, чаще исп-ют УФ-спектроскопию как наиб. чувствительный метод. Гетероциклы, лежащие в основе строения отдельных групп алк-дов, часто имеют характерные максимумы поглощения в УФ-свете. Спектральные методы анализа требуют высокой степени чистоты выделенных в-в и сочетаются с предварительной очисткой.
5. Фармакологические пробы.
В том случае, если алк-ид оказывает характерное д-вие на живой орг-зм, м. б. выполнены фармаколог. пробы на животных, к-е проводятся квалифиц. специалистом-фармакологом. Н-р, при доказательстве атропина капают водный р-р испытуемого в-ва в глаз кошки. При наличии атропина набл-ся характерное стойкое расширение зрачка. Стрихнин и никотин, нанесенные на спинку лягушки, вызывают ее гибель в характерной позе («молящаяся лягушка» - стрихнин, «сидящая» - никотин).
IV. КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ проводится фотометрическим и спектрофотометр. методами (в видимой и УФ-областях спектра).
1. Определение в УФ-области (200-400 нм) проводится по специфическому поглощению (абсорбции) самого алк-да при наличии у него хромофорной системы. Интенсивность поглощения пропорциональна конц-ции. Расчет ведут по уравнению закона Бугера-Ламберта-Бера. Определение проводится на спектрофотометре, т.к. закон Бера справедлив только для монохроматического излучения.
2. Определение в видимой области (400-800 нм) основано на измерении абсорбции окрашенных комплексов алк-дов с кислотными реагентами (пикриновой к-той, тропеолином-00, метиловым оранж., бромфеноловым синим и т.п.). В этом случ. образ-ся ионные ассоциаты, для образования к-х большое значение имеет рН среды, т.к. в момент р-ции и алк-ды, и реагенты д. б. ионизированы. Окрашенные ионные ассоциаты м. б. экстрагированы из водной фазы орг. раств-лем. Такое определение носит название экстракционно-фотометрического.
Окрашенные продукты м. б. получены т/ж в р-циях окисления, восст-ния, конденсации, азотосочетания и некот. др. Измерение абсорбции можно вести как на фотоэлектроколориметрах, так и на спектрофотометрах. Расчет конц-ции проводится по калибровочной кривой. При исп-нии спектрофотометрии можно исп-вать уравнение Бугера-Ламберта-Бера. Фотометрическ. методы ан-а позволяют определять очень малые (несколько микрограммов) кол-ва алк-дов, но требуют высокой степени чистоты выделенного в-ва, поэтому сочетаются с ХТС – очисткой полученных извлечений.
Производные изохинолина: морфин, кодеин и синтетические аналоги - промедол, этилморфин, диацетилморфин. Их особое токсикологическое значение, специфика методов изолирования и определения.
МОРФИН  явл-ся одним из главных алк-дов опия, в к-м сод-ся 3-20 % этого алк-да. В медицине прим-ся гидрохлорид морфина. Этот пр-т явл.ся основным представителем группы нарк. анальгетиков. Морфин оказывает сильное болеутол. д-вие, понижает возбудимость болевых центров, оказывает противошок. д-вие при травмах и т. д. Морфин вызывает эйфорию. При повторном прим. морфина к нему быстро развив. болезненное пристрастие (морфинизм). Постоянное прим-е пр-тов опийной группы приводит к психическ. и физ. деградации и ранней гибели больных. Объектами судебно-хим. ан-за на морфин явл-ся желудок с содержимым, печень, селезенка, почки, легкие, кровь, моча, головной и спинной мозг. Выделение морфина из био. материала. Рекомендованы методы, основанные на изолир-нии этого алк-да спиртом, подкисленным щавелевой к-той, или водой, подкисленной щавелевой или серн. к-той. Большие кол-ва морфина выделяются с помощью метода, основанного на изол-нии его водой, подкисленной серной к-той.
явл-ся одним из главных алк-дов опия, в к-м сод-ся 3-20 % этого алк-да. В медицине прим-ся гидрохлорид морфина. Этот пр-т явл.ся основным представителем группы нарк. анальгетиков. Морфин оказывает сильное болеутол. д-вие, понижает возбудимость болевых центров, оказывает противошок. д-вие при травмах и т. д. Морфин вызывает эйфорию. При повторном прим. морфина к нему быстро развив. болезненное пристрастие (морфинизм). Постоянное прим-е пр-тов опийной группы приводит к психическ. и физ. деградации и ранней гибели больных. Объектами судебно-хим. ан-за на морфин явл-ся желудок с содержимым, печень, селезенка, почки, легкие, кровь, моча, головной и спинной мозг. Выделение морфина из био. материала. Рекомендованы методы, основанные на изолир-нии этого алк-да спиртом, подкисленным щавелевой к-той, или водой, подкисленной щавелевой или серн. к-той. Большие кол-ва морфина выделяются с помощью метода, основанного на изол-нии его водой, подкисленной серной к-той.
Обнаружение морфина. 1) Р-ции с реактивами группового осаждения алк-дов. Морфин дает осадки (реактивы Бушарда, Драгендорфа, Майера, Зонненшейна и др.). 2) Цветные р-ции. Морфин дает окраску с конц. азотной к-той, реактивами Манделина, Марки, Фреде и Эрдмана. 3) Реакция Пеллагри. При нагревании морфина с конц. соляной и серн. к-тами он превращается в апоморфин, к-й дает положит. р-цию При выполнении р-ции Пеллагри на морфин и кодеин их переводят в апоморфин путем нагревания с конц. соляной и серн. к-тами, а затем прибавляют остальные реактивы, необх-е для протекания этой р-ции. 4) Р-ция с хлоридом железа (III) - синяя окраска. 5) Реакция с йодноватой к-той (НIO3). В рез-те выдел-ся свобод. иод, к-ый при взбалт-нии с хлороформом переходит в хлороформный слой, окрашивая его в фиол. цв. 6) Р-ция с гексацианоферратом (III) калия и хлоридом железа (III). Р-ция основана на том, что гексацианоферрат (III) калия окисляет морфин и превращается в гексац-ррат (II) калия, к-й взаим-вует с FeCl3.. При этом образ-ся берлинская лазурь, имеющая синюю окраску. 7) Метод хроматографии.После всех процедур пластинкуопрыскивают реактивом Драгендорфа. При наличии морфина пятна этого алк-да на хроматограф. пластинке приобретают розовато-бурую окраску. 8) Обнаружение морфина по УФ- и ИК-спектрам. 9) Фотоколориметрический метод определения морфина. Применяют метод, основанный на р-ции этого алк-да с кремне-молибденов. к-той, в рез-те к-й возникает синяя окраска.
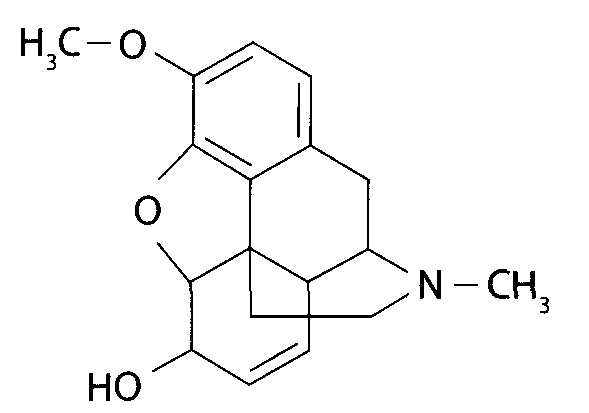 КОДЕИН - монометиловый эфир морфина. Он явл-ся одним из алк-дов опия. В опии, полученном из снотворного мака, сод-ся 0,2-2 % кодеина. В отдельных сортах индийского опия сод-ся около 6 %. Кодеин прим. в медицине в виде основания и фосфата. По д-вию на орг-зм кодеин близок к морфину. Однако болеутоляющее св-во кодеина выражено слабее, чем у морфина. Он в меньшей степени, чем морфин, угнетает дыхание. Он уменьшает возбудимость кашлевого центра, и поэт. назначается для успокоения кашля, в сочетании с анальгином, амидопирином, кофеином, фенобарбиталом и др. пр-тами прим-ся при голов. болях, невралгиях и т. д. Менее токсичен, чем морфин. Но при частом, повторяющемся приеме кодеина возможно привыкание к нему. Объектами анализа при отравлении кодеином явл-ся желудок и толстая кишка с содержимым, почки, моча, мозг, печень с желчным пузырем, кровь. Извлечение. Кодеин экстрагируется орг. раств-лями из подщелоченных водных вытяжек. Максимальные кол-ва кодеина экстрагируются хлороформом при рН=8,0...3,5. Обнаружение кодеина. 1) Предварит. проба на кодеин: Применяют предварит. пробы, основанные на р-циях с реактивом Марки (красноватая окраска, переходящая в сине-фиолет.) и ванадатом аммония (зел. окраска, переходящая в синюю. 2) Р-ция с реактивами группового осаждения алк-дов. При взаим-вии кодеина с реактивами Драгендорфа, Бушарда, Майера и др. образуются осадки. 3) Цветные р-ции. Кодеин с реактивами Манделина, Марки (сине-фиол. окрас.) и Фреде (зеленая, прех. в синюю) дает окрашенные продукты р-ции. 4) Р-ция Пеллагри. При нагревании кодеина с конц. соляной к-той, а затем с конц.серной к-той происх. деметоксилирование этого алк-да и образ-ся апоморфин, к-й дает р-цию со спирт. р-ром иода. 5) Метод хр-графии. 6) Способы ид-кации, позв-щие отличить кодеин от морфина. Кодеин не дает р-ций с хлоридом железа (III), с НIO 3, с гексацианоферратом (III) калия и хлоридом железа (III), к-е дает морфин. Кодеин можно отличить от морфина и по светопоглощению в ИК-области спектра. Кодеин отличается от морфина и тем, что морфин не экстрагируется диэтил. эфиром из щелочных р-ров(образуется морфинат). Это свойство указанных алкалоидов используется для разделения их в ходе анализа. 7) Экстракционно-фотоколориметрическ. метод определения кодеина. Метод основан на рции с тропеолином 00, при кй образся ионный ассоциат, экстрагщийся хлороформом.
КОДЕИН - монометиловый эфир морфина. Он явл-ся одним из алк-дов опия. В опии, полученном из снотворного мака, сод-ся 0,2-2 % кодеина. В отдельных сортах индийского опия сод-ся около 6 %. Кодеин прим. в медицине в виде основания и фосфата. По д-вию на орг-зм кодеин близок к морфину. Однако болеутоляющее св-во кодеина выражено слабее, чем у морфина. Он в меньшей степени, чем морфин, угнетает дыхание. Он уменьшает возбудимость кашлевого центра, и поэт. назначается для успокоения кашля, в сочетании с анальгином, амидопирином, кофеином, фенобарбиталом и др. пр-тами прим-ся при голов. болях, невралгиях и т. д. Менее токсичен, чем морфин. Но при частом, повторяющемся приеме кодеина возможно привыкание к нему. Объектами анализа при отравлении кодеином явл-ся желудок и толстая кишка с содержимым, почки, моча, мозг, печень с желчным пузырем, кровь. Извлечение. Кодеин экстрагируется орг. раств-лями из подщелоченных водных вытяжек. Максимальные кол-ва кодеина экстрагируются хлороформом при рН=8,0...3,5. Обнаружение кодеина. 1) Предварит. проба на кодеин: Применяют предварит. пробы, основанные на р-циях с реактивом Марки (красноватая окраска, переходящая в сине-фиолет.) и ванадатом аммония (зел. окраска, переходящая в синюю. 2) Р-ция с реактивами группового осаждения алк-дов. При взаим-вии кодеина с реактивами Драгендорфа, Бушарда, Майера и др. образуются осадки. 3) Цветные р-ции. Кодеин с реактивами Манделина, Марки (сине-фиол. окрас.) и Фреде (зеленая, прех. в синюю) дает окрашенные продукты р-ции. 4) Р-ция Пеллагри. При нагревании кодеина с конц. соляной к-той, а затем с конц.серной к-той происх. деметоксилирование этого алк-да и образ-ся апоморфин, к-й дает р-цию со спирт. р-ром иода. 5) Метод хр-графии. 6) Способы ид-кации, позв-щие отличить кодеин от морфина. Кодеин не дает р-ций с хлоридом железа (III), с НIO 3, с гексацианоферратом (III) калия и хлоридом железа (III), к-е дает морфин. Кодеин можно отличить от морфина и по светопоглощению в ИК-области спектра. Кодеин отличается от морфина и тем, что морфин не экстрагируется диэтил. эфиром из щелочных р-ров(образуется морфинат). Это свойство указанных алкалоидов используется для разделения их в ходе анализа. 7) Экстракционно-фотоколориметрическ. метод определения кодеина. Метод основан на рции с тропеолином 00, при кй образся ионный ассоциат, экстрагщийся хлороформом.
 ПРОМЕДОЛ (тримеперидин) прим. как болеутол. ср-во при травмах и различ. забол-ях, при подготовке к операции и в послеоперац. периоде. Он прим. при язвенной болезни, стенокардии, инфаркте миокарда, различ. коликах, для обезболивания при родах. Промедол явл-ся одним из противошоковых средств. Он понижает возбудимость больших полушарий голов. мозга. Промедол обладает сильной анальгезирующей акт-стью. По д-вию на ЦНС промедол близок к морфину. Он в меньшей степени угнетает дыхат.центр, чем морфин.
ПРОМЕДОЛ (тримеперидин) прим. как болеутол. ср-во при травмах и различ. забол-ях, при подготовке к операции и в послеоперац. периоде. Он прим. при язвенной болезни, стенокардии, инфаркте миокарда, различ. коликах, для обезболивания при родах. Промедол явл-ся одним из противошоковых средств. Он понижает возбудимость больших полушарий голов. мозга. Промедол обладает сильной анальгезирующей акт-стью. По д-вию на ЦНС промедол близок к морфину. Он в меньшей степени угнетает дыхат.центр, чем морфин.
При частом применении промедола может развиваться привыкание и болезненное пристрастие к нему (наркомания). Поэтому промедол применяется т-ко по назнач. врача. Извлечение. Экстрагируется орг. раст-лями из щелочных водных р-ров. Обнаружение. Для обнаружения промедола в химико-токс. анализе применяется огранич. число р-ций и методов. Однако сочетание этих методов позволяет обнаружить промедол в вытяжке из био. материала. 1) Р-ция с реактивом Марки. От прибавления реактива Марки к промедолу появл. красно-пурпурная окраска. 2) Обнаружение промедола методом хроматографии. При наличии промедола в хлороформной вытяжке на желтом фоне пластинки появл. корич. пятна.
 ЭТИЛМОРФИН (дионин (гидрохлорид этилморфина, т.е. доб. в формулу *HCl*2H2O)) получают синтетическим путем из морфина. По д-вию на организм близок к кодеину. Он прим. как ср-во для успокоения кашля, а также исп-ся в офтальмологии в виде капель и мазей. Извлечение. Экстрагируется орг. раств-лями из щелочных водных р-ров. Обнаружение. Для обнаружения дионина прим. цветные и микрокристаллоскопическ. р-ции, а т/ж метод спектроскопии.
ЭТИЛМОРФИН (дионин (гидрохлорид этилморфина, т.е. доб. в формулу *HCl*2H2O)) получают синтетическим путем из морфина. По д-вию на организм близок к кодеину. Он прим. как ср-во для успокоения кашля, а также исп-ся в офтальмологии в виде капель и мазей. Извлечение. Экстрагируется орг. раств-лями из щелочных водных р-ров. Обнаружение. Для обнаружения дионина прим. цветные и микрокристаллоскопическ. р-ции, а т/ж метод спектроскопии.
1) Реакция с реактивом Марки – зел. окраска, переходящая в синюю, а затем в синефиолет. 2) Реакция с хлоридом ртути (II) – бесцвет. тонкие призматическ. кристаллы. 3) Обнаружение этилморфина по УФ-спектру. Этилморфин в 0,2 н. р-ре серной к-ты имеет максимум поглощения при 285 нм и изгиб при 277 нм. 4) Отличие этилморфина от морфина. Этилморфин не дает р-ции с хлоридом железа (III), иодноватой к-той (НIО3) и гексацианоферратом (III) калия, к-е дает морфин.
 ДИАЦЕТИЛМОРФИН (героин) - Это быстродействующий наркотический анальгетик с малым периодом полувыведения. Он относится к числу наиб. опасных нарк. средств. Героин явл-ся синтетическим в-вом, изготовляемым в подпольных лаб-риях. Его получают по р-ции ацетилирования из морфина и морфинсодержащего сырья. Последствием д-вия героина на организм явл-ся привыкание, к-е наступает быстро, иногда с первого раза. Героин вызывает расстройство пищеварения, деятельности внутренних органов. Наблюдается нарушение эндокринного баланса, снижение иммунитета, импотенция, опасное подавление многих реакций организма. Развивается безразличие, депрессия, раздражительность, истерия, психопатические реакции, склонность к гневу, агрессии, суициду. Ухудшается работа мозга, наблюдаются отек мозга, судорожные припадки, необратимые изменения личности, умственная, психическая и физическая деградация, остановка дыхания, потеря сознания, перебои в работе сердца и смерть. После прекращения приема наркотика характерно эмоциональное напряжение, раздражительность, зрачки расширяются, глаза слезятся, наблюдается слюнотечение, потливость, «гусиная кожа», мышцы спины, рук и ног напрягаются, возникает физическая слабость, аритмия, тахикардия, тошнота, рвота, тремор, появляются выламывающие боли мышц рук, ног, сведение жевательных мышц, икр, нестерпимые боли в животе, пояснице, в области сердца, зуд, жжение. Извлечение. Подкисленной водой или подкис. спиртом.
ДИАЦЕТИЛМОРФИН (героин) - Это быстродействующий наркотический анальгетик с малым периодом полувыведения. Он относится к числу наиб. опасных нарк. средств. Героин явл-ся синтетическим в-вом, изготовляемым в подпольных лаб-риях. Его получают по р-ции ацетилирования из морфина и морфинсодержащего сырья. Последствием д-вия героина на организм явл-ся привыкание, к-е наступает быстро, иногда с первого раза. Героин вызывает расстройство пищеварения, деятельности внутренних органов. Наблюдается нарушение эндокринного баланса, снижение иммунитета, импотенция, опасное подавление многих реакций организма. Развивается безразличие, депрессия, раздражительность, истерия, психопатические реакции, склонность к гневу, агрессии, суициду. Ухудшается работа мозга, наблюдаются отек мозга, судорожные припадки, необратимые изменения личности, умственная, психическая и физическая деградация, остановка дыхания, потеря сознания, перебои в работе сердца и смерть. После прекращения приема наркотика характерно эмоциональное напряжение, раздражительность, зрачки расширяются, глаза слезятся, наблюдается слюнотечение, потливость, «гусиная кожа», мышцы спины, рук и ног напрягаются, возникает физическая слабость, аритмия, тахикардия, тошнота, рвота, тремор, появляются выламывающие боли мышц рук, ног, сведение жевательных мышц, икр, нестерпимые боли в животе, пояснице, в области сердца, зуд, жжение. Извлечение. Подкисленной водой или подкис. спиртом.
Производные барбитуровой кислоты (барбитал, фенобарбитал, бутобарбигал, этаминал натрия). Химическое строение и свойства. Токсичность. Методы изолирования, обнаружения, количественного определения.
Слева-направо: барбитал, фенобарбитал, бутобарбитал, этаминал-натрий.

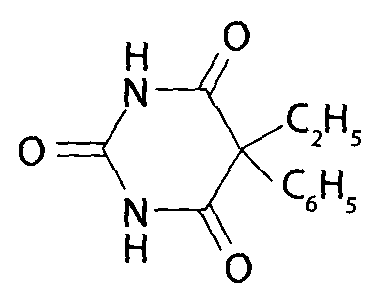


Свойства. Барбитураты - белые крист. в-ва без запаха. Они практически нераств. или малораств. в воде, раств. в этил. спирте, диэтил. эфире, этилацетате, в р-рах щелочей, мало раств. в хлороформе. Барбитураты обладают слабыми кислот. св-вами. Характерным св-вом барб-тов явл-ся их способность возгоняться без разложения, что часто исп-ся с целью очистки извлечений из био.объектов.
Токсиколог. значение. Важным д-вием барб-тов на орг-зм явл-ся угнетение ЦНС. С лечеб. целью производные барбитуровой к-ты находят применение в мед. практике в кач-ве снотв. и успокаивающих ср-тв. По продолж-сти сна, вызываемого барб-тами, их делят на 3 гр.: длит-го д-вия (барбитал, фенобарбитал); средней продолж-сти д-вия (бутобарбитал, барбамил, этаминал-натрий); короткого д-вия (гексенал). В наст. время в мед. практике находят применение барбитал и фенобарбитал. Фенобарбитал входит в сост. некот. готовых ЛФ «Пенталгин», «Андипал», «Беллатаминал», «Теофедрин», «Корвалол», «Валокордин», «Барбовал» и др. Этаминал-натрий и барбамил включены в список нарк. и псих. ср-тв, оборот к-х ограничен. Бутобарбитал исп-ся как вспом. ср-во при общей анестезии и при судорожных сост-ях. Злоупотребление барб-тами приводит к наркомании. Картина опьянения напоминает по внеш. признакам алког.е опьянение: приятное ощущение состояния эйфории, общего благополучия. Позже наступает оглушенность, сонливость, вплоть до комы. Отравления барб-тами встречаются относит-но редко. Чаще эти пр-ты исп-ся с целью самоубийства. Токсические дозы барб-тов выз-ют первоначально наркотическ. опьянение, затем коматозное состояние, к-е осложняется сердечно-сосудистой или дыхат. недост-стью. Тяжелые отравления хар-ся глубокой комой, редким поверхностным дыханием, слабым пульсом, цианозом. В заключит. стадии отравления, вследствие поражения дыхат. цетра, дыхание становится неравномерным, после чего наступает его остановка. Токсическое д-вие барб-тов усиливают наркотики, алкоголь, транквилизаторы. Объекты анализа: трупный материал (внутр. органы), био. ж-сти (кровь, моча), лек. преп-та. Для анализа исп-ют хлороформный (эфирный) экстракт, полученный из водной вытяжки из объекта при рН=2. Анализ на производные барбит. к-ты проводят, если при ТСХ-скрининге на пластинке получены пятна сине-фиолет. цвета при детектировании солями ртути (II) и р-ром дифенилкарбазона в хлороформе. Методы определения. Для обнаружения индивид. в-в исп-ют ТСХ в частной системе раств-лей, хим. метод, ВЭЖХ, УФ-спектрофотометр., ИК-спектроскопию, газовую хрграфию и сочетание газовой хрграфии с масс-спектрометрией.
Хим. метод основан на применении р-ций комплексообразования и микрокристаллоскопических р-ций. 1) Реакция с аммиачным р-ром нитрата кобальта -красно-фиол. окраш. Реакция чувствительна. Имеет судебно-хим. значение при отрицат. рез-те. 2) Реакция обнаружения кислотной формы барбитуратов. На предметное стекло наслаивают экстракт. Полученный сухой остаток растворяют в капле конц. серной к-ты. Рядом наносят 1 каплю воды очищ., после чего обе капли соединяют.Ч/з 10-20 мин при хранении стекла во влажной камере наблюдают образование кристалличю осадка (под микроскопом) с характерной для каждого барбитурата формой кристаллов. Эта р-ция хар-ся высокой специф-стью, но низкой чувст-стью. Р-ция приемлема при относительно больших кол-вах барб-тов. 3) Р-ция с хлорцинкйодом. Наблюдают характерную форму кристаллов. Р-ция чувствительна, явл-ся подтверждающей. 4) Реакция с подкисленным спиртовым раствором йодида калия. Наблюдают образование характерного кристаллического осадка. Реакция чувствительна, позволяет обнаружить в пробе до 0,5 мкг барбитуратов, является подтверждающей. Фенобарбитал и барбамил с подкисленным спиртовым р-ром йодида калия кристаллического осадка не образуют. 5) Реакция со смесью р-ров хлорида железа(Ш) и йодида калия (железойодидной комплексной солью). Кристаллы характерной формы образуют барбамил, этаминал, фенобарбитал и бутобарбитал. Барбитал с железойодидным реактивом характерных кристаллов не образует. Реакция чувствительна, является подтверждающей. 6) Реакция с меднопиридиновым реактивом (реакция Цвиккера). Набл. кристаллы. Фенобарбитал, барбамил, этаминал характерных кристаллов с меднопиридиновым реактивом не образуют. Реакция чувствительна, является подтверждающей.
Хроматография в тонком слое сорбента в частной системе растворителей. Проводится в присутствии «стандартов», в качестве ко-х исп-ют спиртовые р-ры барбитала, фенобарбитала, барбамила, этаминал-натрия и бутобарбитала. Идентифицируют барбитураты на хроматографическ. пластинке по месторасположению, окраске и значению Rf анализируемого в-ва и «стандарта».
УФ-спектрофотометрия. Для регистрации УФ-спектра поглощения остаток после испарения экстракта из водной вытяжки со значением рН=2 растворяют в 5 мл воды очищенной, к которой была добавлена 1 капля 2 М раствора аммиака (рН=10), и измеряют величину светопоглощения полученного р-ра в интервале длин волн 210-320 нм.
ИК-спектрометрия. Для регистрации ИК-спектра остаток после испарения хлороформа (диэтилового эфира) растирают с бромидом калия и после прессования помещают в прибор для снятия спектра. Производные барбитуровой кты имеют основные характерные для каждого барбитурата волновые числа в ИК спектре.
ГЖХ-анализ. Для обнаружения барбитуратов используют индексы удерживания для каждого барбитурата.
Газовая хроматография в сочетании с масс-спектрометрией исп-ся для обнаружения нанограммовых кол-ств барб-тов и позволяет вести анализ на фоне эндогенных соед-ний, выделенных из исследуемого объекта. Для выделения барб-тов из объекта после гидролиза исп-ют жидкость-жидкостную или твердофазную экстракцию. Концентрирование извлечений проводят упариванием при т-ре 40-60°С. Идентиф-ют барб-ты по времени удерживания (для барбитала - 5,18 мин) и по отношению массы ионов к заряду (204 для фенобарбитала).
ВЭЖХ. Барбитураты извлекают из био. объектов при рН=1-2 хлороформом, смесью хлороформ - изопропанол 9:1 или диэтиловым эфиром. Предварительно рек-дуется при анализе мочи провести кислотный гидролиз для разрушения метаболитов - глюкуронидов. Для обнаружения барб-тов в исследуемой пробе сравнивают время (объем) удерживания и коэффициент емкости определяемого в-ва с образцом сравнения в тех же условиях; сравнивают УФ-спектры поглощения с образцом сравнения, а также сопоставляют УФ-спектры исследуемого компонента и образца сравнения при 2 и более длинах волн и оценивают их спектральные отношения.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ проводится прямым фотометрическим методом, с помощью дифференциальной спектрофотометрии и высокоэффективной жидкостной хроматографии.
Фотометрический метод основан на взаим-вии барбитуратов с раствором ацетата кобальта в присутствии изопропиламина и метанола (В.И.Попова). Барбитураты из био. материала извлекают водой, подкисленной серной кислотой. После очистки с помощью гель-хроматографии проводят концентрирование путем экстракции хлороформом. Хлороформный экстракт выпаривают до сухого остатка. Сухой остаток, в зависимости от обнаруженного барбитурата, растворяют в хлороформе (барбитал, фенобарбитал) или метиловом спирте (барбамил, этаминал), К полученным растворам добавляют по 5 мл 0,125% раствора ацетата кобальта в метиловом спирте и по 1 мл 50% изопропиламина в метиловом спирте. Оптическую плотность растворов, окрашенных в фиолетовый цвет, измеряют с помощью фотоэлектроколори-метра ФЭК-М при зеленом светофильтре в кювете 20 мм. В качестве раствора сравнения применяют смесь реактивов.
Дифференциальная спектрофотометрия. Количественное определение проводят в этом случае по разности величины оптической плотности исследуемого и контрольного опытов.
Химическая дифференциальная спектрофотометрия. Этот метод приемлем в том случае, когда при различных значениях рН среды изменяется спектр поглощения исследуемого вещества, а спектр поглощения примесей (посторонних экстрактивных веществ) остается без изменений. Такая методика предложена для определения производных барбитуровой кислоты. Барбитураты изолируют из биологических объектов общими (Стаса-Отто, Васильевой) или частными (Валова, Поповой) методами. Для экстракции барбитуратов из водной фазы при рН=2-2,5 применяют диэтиловый эфир или хлороформ. В основу метода дифференциальной спектрофотометрии положена способность барбитуратов к лактим-лактамной (имидо-имидольной) таутомерии. В органическом растворителе после экстракции барбитураты находятся в лактамной форме. Использование дифференциального варианта спектрофотометрического определения барбитуратов позволяет получить достаточно надежные результаты и исключить влияние посторонних веществ, экстрагируемых в процессе анализа вместе с барбитуратами из раствора при рН=2-2,5.
Метод ВЭЖХ в трех вариантах: метод добавок, метод внешнего стандарта и метод внутреннего стандарта.
1) Метод добавок. Для выделения токсических в-в из мочи исп-т жидкость-жидкостную экстракцию. Анализ ведут с двумя пробами мочи. С помощью ВЭЖХ проводят анализ экстракта из одной пробы мочи и экстракта из второй пробы мочи с добавлением в нее опред. кол-ва в-ва (эталонного р-ра), обнаруженного при качественном анализе. Расчет количества найденного в-ва в экстракте из мочи.
2) Метод внешнего стандарта. Он основан на линейной завис-сти выходного сигнала от массы в-ва. В этом случае параллельно с анализом экстракта из мочи в тех же условиях проводят анализ эталонного р-ра найденного в-ва приблизительно той же конц-ции. Расчет ведется по фор-ле.
3) Метод внутреннего стандарта. К пробе мочи до операции пробоподготовки добавляют опред. кол-во в-ва, к-е явл-ся стандартом. Стандарт и определяемое в-во должны хорошо разделяться в процессе ан-за. При ан-зе барб-тов в кач-ве внутренних стандартов рек-ется исп-вать одно из след. в-в: апробарбитал, метилфенобарбитал, фенилгидантоин, к-е при хр-графировании полностью отделяются от комп-тов образца. Конце-цию определяемого в-ва рассчитывают по формуле.
Производные 1.4-бензодиазепина (хлордиазепоксид, диазепам, оксазепам, нитразепам). Химическое строение и свойства. Токсичность. Методы изолирования, обнаружения, количественного определения.
Слева-направо: хлордиазепоксид (хлозепид), диазепам (сибазон), оксазепам (нозепам), нитразепам.
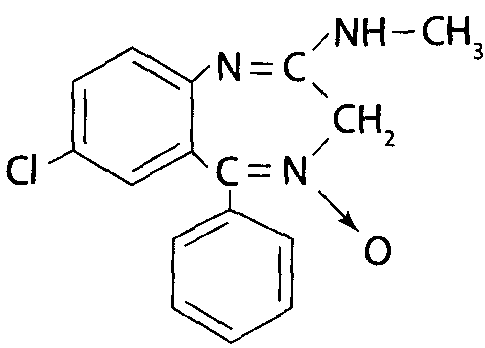



Свойства. Оксазепам, диазепам, хлордиазепоксид - белые крист. в-ва. Допускается желтоват., зеленовато-желт. или кремовый оттенок. Нитразепам имеет светло-желтую с зел. оттенком окраску за счет наличия в мол-ле нитрогруппы. Производные бензодиазепина практически нераств. в воде, малораств. в этаноле и эфире, но хор. раств. в хлороформе. Они облад.т слабоосновными св-вами за счет гетероатома азота в положении 4 и слабокислот. св-вами за счет имидо-имидольной таутомерии в полож. 1-2.
Токсикологическ. значение. Введены в мед. практику как транквилизаторы. Находят применение в психиатрическ. практике как нейролептики, но отлич-ся отсутствием антипсихотической акт-сти. В связи с распространяющимися фактами злоупотр-ния соед-ями данной группы, Комиссия ООН по наркотикам включила их в список соед-ний, находящихся под м/ународным контролем. При злоупотреблении однократ. доза достигает 10 табл. и более на прием. Больные испытывают чувство умиротворения, расслабленности. Внешне такие больные выглядят, как находящиеся в легкой стадии опьянения: неувер походка, беззаботность, блаженная улыбка. При длит. злоупотр. развивается абстинентный синдром, выражающийся в тревоге, беспокойстве, страхе, бессоннице, повыш. потливости, тахикардии. Бензодиазепины обладают выраженными токсическими св-вами. Описаны случаи отравлений в рез-те несчастных случаев (чаще всего с маленькими детьми) или с целью самоубийства. Пр-ты хор. всас.ся из пищевар. тракта. При легкой степени отравления хлозепидом проявл-ся вялость, сонливость, заторможенность, расш. зрачков, снижение мышечного тонуса. При отравлениях средней тяжести признаки отравления, указанные выше, выражены более четко. Добавляется гиперемия лица, сухость кожных покровов, тахикардия, тремор конечностей, отсутствие многих рефлексов. При тяжелой форме отравления сознание спутано, наблюдается психомоторное возбуждение, клонические судороги или галлюцинаторный синдром, развивается дыхательная и сердечная недост-сть. Диазепам по действию на организм сходен с хлозепидом, но его токсическое д-вие проявляется в меньших дозах. Оксазепам (тазепам) менее токсичен, чем хлозепид. Нитразепам оказывает более выраженное успокаивающее и снотв. д-вие. Картина отравления сходна с хлозепидом.
Объекты анализа: желудок с содержимым, тонкий кишечник с содерж., голов. мозг, печень, почки, кровь, моча, лек. пр-ты.
Изолирование. При ненаправленном анализе иссл-ние проводится после изол-ния из био. мат-ла подкисленным спиртом или подкисл. водой с хлороформным экстрактом из водной фазы с рН=2 и рН=10.
При исследовании извлечений из био. объектов исп-ют 2 направления в анализе.
1 направление основано на гидролизе бензодиазепинов до 2-аминобензофенонов. Данный способ позволяет обнаружить и определить в извлечении нативные соед-ния и их метаболиты. Этому направлению придают судебно-хим. значение при отриц. рез-те.
2 направление исп-ся, если в процессе иссл-ния обнаружены бензофеноны по 1 направлению анализа. Этот способ позволяет точно установить природу 1,4-бен-зодиазепина по нативным соед-ям и их метаболитам.
Date: 2016-08-31; view: 1608; Нарушение авторских прав