
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Угольная кислота и ее соли
|
|
Оксиду CO2 соответствует слабая, нестойкая угольная кислота H2CO3
Соли этой кислоты:
§ средние соли карбонаты (K2CO3)
§ кислые соли гидрокарбонаты (KHCO3)
Особенности карбонатов и гидрокарбонатов:
карбонат любого металла (кроме I A) → оксид металла + CO2
CuCO3 → CuO + CO2 ↑
K2CO3 → реакция не идет (ибо K – I А)
гидрокарбонат любого металла при to → карбонат + СО2 + Н2О
2NaHCO3 → Na2CO3 + H2O+ CO2
Кроме того, гидрокарбонат переходит в карбонат под действием ЩЕЛОЧИ!
2NaHCO3 + NaOH → Na2CO3 + H2O
а карбонат в гидрокарбонат – под действием CO2 + H2O
Na2CO3 + H2O+ CO2 →2NaHCO3
Оксид кремния SiO2 – кристаллическое вещество с атомной решеткой. Не растворим в воде. Имеет свойства кислотного оксида. Он – основа стекла.
Получение – путем разложения кремневой кислоты при нагревании:
H2SiO3 → H2O + SiO2
Особенности химических свойств:
1. Реагирует с HF. Поэтому HF разъедает стекло
SiO2 + HF → SiF4 + H2O
2. Вытесняет СО2 из карбонатов и сульфитов
K2CO3 + SiO2 → K2SiO3 + CO2
K2SO3 + SiO2 → K2SiO3 + SO2
3. НЕ реагирует с Н2О: SiO2 + H2O → ۞
SiO2 соответствует кремневая кислота H2SiO3 (твердая, нерастворимая в воде, имеет полимерное строение и атомную кристаллическую решетку).
Её соли кремневой кислоты – силикаты.
Качественная реакция на силикаты: K2SiO3 + H2O + CO2 → H2SiO3 + K2CO3
Растворы K 2 SiO 3 иNa 2 SiO 3 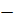 это «жидкие стекла» это «жидкие стекла»
|
Это свойство демонстритуетъ, что H2SiO3 слабее даже угольной кислоты.
Особенности химических свойств H2SiO3:
· Не реагируетъ съ металлами
· Не реагируетъ съ солями
· Не реагируетъ съ нерастворимыми основаниями
· Реагируетъ со щелочами: H2SiO3 + KOH → K2SiO3 + H2O
· При нагревании разлагается: H2SiO3 → H2O + SiO2
________________________________________________________________________________________
Оксиды азота: N2O, NO, N2O3, NO2, N2O5
N2O – несолеобразующий оксид (закись азота, веселящий газ). Это бесцветный газ сладковатого вкуса, растворимый в воде. Используется для ингаляционного наркоза в медицине.
Получение: путем разложения нитрата аммония при нагревании:
NH4NO3 → N2O + H2O
Химические свойства:
При нагревании разлагается до азота и кислорода:
N2O → N2 + О2
NO – несолеобразующий оксид (окись азота). Это бесцветный газ не растворимый в воде.
Получение:
1. В промышленности получают путем каталитического окисления аммиака кислородом воздуха:
NH3 + O2 → NO + H2O (на катализаторе)
2. В лаборатории получают действием разбавленной азотной кислоты на малоактивные металлы:
Cu + HNO3 (разб.) → Cu(NO3)2 + NO + H2O
Химические свойства:
1. Окисляется кислородом до NO2:
NO + O2 → NO2
2. Окисляется галогенами, например, хлором:
NO + Cl2 → NOCl2
3. Конпропрционирует с оксидом азота (IV):
NO + NO2 ↔ N2O3 Реакция обратима!!!
N2O3 – темно-синяя жидкость.
Получение:
Получают путем конпропорционирования оксидов азота (II) и (IV):
NO + NO2 ↔ N2O3 Реакция обратима!!!
Химические свойства:
Date: 2015-05-22; view: 720; Нарушение авторских прав