
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

II.1. Скорость химической реакции
|
|
Скорость химической реакции обычно характеризуется изменением концентрации одного из исходных веществ или конечных продуктов в единицу времени.
Скорость гомогенной и скорость гетерогенной реакции определяются различно.
Для гомогенной реакции скорость рассчитывается через количество вещества, вступившего в реакцию или образовавшегося при реакции в единицу времени в единице объема. Cкорость гомогенной реакции рассчитывается u =dc/dt и измеряется в (моль/л∙с). Для гетерогенной реакции скорость рассчитывается по выражению u =dc/S∙dt и измеряется в (моль/м2∙с).
На рис.4 представлены кривые, соответствующие изменению концентраций исходных веществ и продуктов реакций со временем. Концентрации исходных веществ со временем уменьшаются, а концентрации продуктов увеличиваются. Скорость реакции всегда остается положительной величиной, обычно рассчитывается средняя скорость реакции.

Рис.4. Изменение концентрации исходного вещества (a) и продукта реакции (b) со временем.
Если в момент времени τ1 и τ2 концентрации одного из веществ равны С1 и С2 (рис.3), то среднюю скорость реакции u выражают уравнением:
u =|С2 – С1|/(τ2-t1) = ΔС/Δτ, моль/л∙с
Скорость реакции равна первой производной зависимости концентрации от времени, физический смысл первой производной dc/dt - она равна тангенсу угла наклона касательной кривой С = f(τ). На рис.5 представлена зависимость изменения концентрации продукта реакции от времени и расчет скорости реакции.
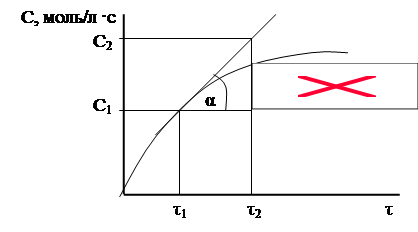 |
Рис.5. Зависимость изменения концентрации продукта реакции от времени
Скорость реакции может быть измерена также по изменению объема выделяющегося газа, изменению количества образующегося осадка, вязкости раствора, его оптической плотности, рН раствора, электропроводности и др.
На скорость реакции влияют следующие факторы: природа реагирующих веществ, концентрация, температура, давление, наличие в системе катализатора.
Date: 2015-05-09; view: 896; Нарушение авторских прав