
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Влияние температуры на направление реакции
|
|
Рассмотрим влияние температуры на направление реакции на примере синтеза аммиака.
3 H2 (г) + N2 (г) = 2 NH3 (г)
Рассчитаем ΔH0 и ΔS0 для данной реакции:
Соединения NH3 (г) H2 (г) N2 (г)
ΔН0обр., кДж/моль ……………… -46,19 0 0
S0, Дж/(моль К) …………………192,5 130,6 191,5
ΔН0 = 2ΔН0NH3 (г) - (ΔН0N2 (г) + 3 ΔН0H2 (г)) = 2·(-46,19) – (0 +3·0) = -92,38 кДж
ΔS0 = 2S0NH3 (г) - (S0N2 (г) + 3S0H2 (г)) = 2·(192,5) – (191,5 + 3·130,6) = -193,3 Дж/К
Найдем ΔG0 этой реакции для следующих температур: 250С и 3500С.
а) при 250С, (25 +273=298К)
ΔG0 = ΔH0 - T·ΔS0 = -92,38 –298· (-198,3 ·10-3) = -33,29 кДж,
То есть ΔG0<0
б)при 3500С, (350+273=623К)
ΔG0 = ΔH0 - T·ΔS0 = -92,38 –623· (-198,3 ·10-3) = +31,16 кДж,
То есть ΔG0>0
Следовательно, при 250С принципиально возможно протекание реакции синтеза аммиака, а при сильном нагревании системы аммиак получить нельзя. Правда, при 250С реакция протекает очень медленно и с малым выходом. Ускорение реакции достигается факторами химической кинетики, которые будут рассмотрены далее.
В соответствии с уравнением
ΔG = ΔH - T·ΔS
влияние температуры на ΔG определяется знаком и величиной ΔS.
На рисунке 3 показана зависимость ΔG для реакций:
а) 2C (графит) + O2(г) =2CO(г), ΔS>0
б) 2Hg (ж) + O2(г) =2HgO (к), ΔS < 0
с) C(графит) + O2(г) =CO2(г), ΔS≈0
а) Реакция 2С (графит) + О2 (г) = 2СО (г) протекает с увеличением объема, поэтому ΔS>0. Судя по графику повышение температуры приводит к увеличению отрицательного значения ΔG, т.е. благоприятно для протекания процесса.
б) Реакция 2Hg(ж) + O2(г) = 2HgO(к) протекает с уменьшением объема системы, изменение энтропии ΔS < 0. При повышении температуры отрицательное значение ΔG уменьшается. Значит, в этом случае, высокотемпературный режим препятствует протеканию процесса. При температуре 500 К происходит изменение знака ΔG на положительное. Выше этой температуры реакция протекает в обратном направлении. Значит, при температуре ниже 500 К происходит образование оксида ртути (II), а выше 500 К он будет распадаться на простые вещества.
с) Для реакции С (графит) + О2 (г) = СО2 (г) энтропия практически не меняется
ΔS≈0, так как в левой и правой части уравнения одинаковое число молей газообразных веществ. Следовательно, зависимость ΔG от температуры соответствует прямой, параллельной оси абсцисс (рис.3). Если в ходе реакции энтропия системы не меняется, то значение ΔG от температуры практически не зависит.
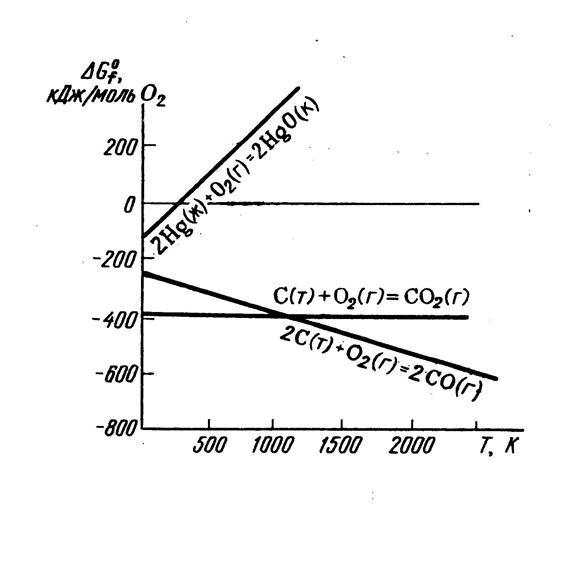
Рис.3. Зависимость ΔG от температуры для ряда оксидов.
Date: 2015-05-09; view: 853; Нарушение авторских прав