
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Процесс парообразования. Основные определения
|
|
При анализе режимов работы теплосиловых установок практически всегда приходиться иметь дело с разного рода жидкостями и их парами.
Процесс парообразования и методика определения основных характеристик процесса парообразования для всех жидкостей практически аналогичны, что дает возможность рассматривать процесс парообразования на примере воды, как одного из наиболее распространенных веществ в природе.
Рассмотрим изобарный процесс парообразования 1 кг воды в
координатах р – v (рис. 19).
В исходном состоянии (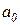 ) вода представляет из себя недогретую жидкость, имеет температуру (
) вода представляет из себя недогретую жидкость, имеет температуру (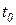 ), значение которой ниже температуры насыщения (
), значение которой ниже температуры насыщения (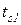 ), а давление воды в этой точке равно р1. В результате изобарного подвода теплоты в процессе (
), а давление воды в этой точке равно р1. В результате изобарного подвода теплоты в процессе (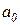 -
- 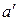 ) вода нагревается до температуры насыщения ts1 и в токе (
) вода нагревается до температуры насыщения ts1 и в токе (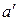 ) начинается процесс кипения.
) начинается процесс кипения.
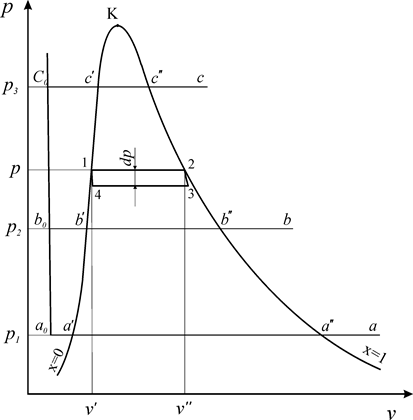
Рис. 19. Диаграмма состояний водяного пара в координатах p-v
Процесс кипения протекает на участке а'- а" при постоянном давлении р 1 и постоянной температуре ts1. В точке (а") вода полностью испаряется. Пар в этом состоянии называется сухим насыщенным. На участке (а'-а") вода находится в двух фазах и состоит из смеси кипящей воды и сухого насыщенного пара. Эта двухфазная равновесная система называется влажным насыщенным паром. При дальнейшем изобарном подводе теплоты сухой насыщенный пар превращается в перегретый (а). Перегретый пар имеет температуру выше температуры кипения (насыщения) при данном давлении. В состоянии (а) параметры перегретого пара имеют следующие
значения: р1, tа > ts1, va.
Аналогичные процессы изобарного подвода теплоты к воде можно провести при других давлениях р2, р3, и т. д. Соответствующие процессы изображаются линиями b0 -b'-b"-b и с0- с'-с"-с. Точки, характеризующие состояния кипящей воды и сухого насыщенного пара при различных давлениях, соединяются плавными линиями.
Линия a'-b'-с' показывает зависимость удельного объема кипящей воды от давления насыщения 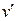 = f(p). Эта линия называется нижней пограничной кривой.
= f(p). Эта линия называется нижней пограничной кривой.
Точки на линии a"-b"-с" характеризуют состояние сухого насыщенного пара, а кривая определяет зависимость удельного объема сухого пара от давления 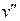 = f(p) и называется верхней пограничной кривой. Пограничные кривые пересекаются в точке (К), называемой критической.
= f(p) и называется верхней пограничной кривой. Пограничные кривые пересекаются в точке (К), называемой критической.
Параметры и функции состояния кипящей воды на нижней пограничной кривой линии насыщения обозначаются одним штрихом, а сухого насыщенного пара - двумя штрихами. Для однозначного определения состояния кипящей воды и сухого насыщенного пара достаточно знание давления р или температуры насыщения ts, по значению которых в термодинамических таблицах водяного пара можно найти свойства кипящей воды - v', u', h', s' и сухого насыщенного пара - v", u", h", s".
В области между пограничными кривыми находится влажный насыщенный пар. Каждой температуре насыщенного пара соответствует определенное давление, то есть между этими параметрами существует однозначная зависимость 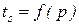 .
.
Для характеристики влажного насыщенного пара, помимо р или ts, в качестве второй независимой переменной используется массовая концентрация сухого насыщенного пара в смеси, называемая степенью сухости или паросодержанием (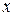 )
)
 , (226)
, (226)
где G" – масса сухого насыщенного пара;  – масса кипящей жидкости;
– масса кипящей жидкости;
G – масса влажного насыщенного пара.
На нижней пограничной кривой 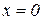 , а на верхней
, а на верхней 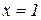 .
.
Отношение массы кипящей жидкости к массе смеси (влажного насыщенного пара) называется влагосодержанием
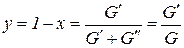 . (227)
. (227)
Количество теплоты, которое необходимо подвести при постоянном давлении к 1 кг кипящей жидкости для превращения ее в сухой насыщенный пар, называется скрытой теплотой парообразования и обозначается символом r. Значение скрытой теплоты парообразования (r) можно определить из математического выражения первого начала термодинамики
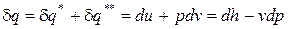 . (228)
. (228)
Так как процесс парообразования протекает при постоянном давлении (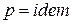 ), скрытая теплота парообразования может быть определена из следующего соотношения:
), скрытая теплота парообразования может быть определена из следующего соотношения:
 . (229)
. (229)
С ростом давления или температуры кипения (насыщения) жидкостей величина скрытой теплоты парообразования 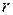 уменьшается и в критической точке становятся равными нулю.
уменьшается и в критической точке становятся равными нулю.
Свойства влажного насыщенного и перегретого пара
Влажный насыщенный пар является бинарной смесью. Свойства влажного насыщенного пара зависят от давления, при котором он находится, от концентраций жидкой и парообразной фаз в системе, которые определяются значением паросодержания 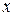 .
.
Известно, что объем  , внутренняя энергия
, внутренняя энергия 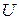 , энтальпия
, энтальпия 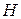 и энтропия
и энтропия 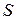 системы являются экстенсивными функциями, значения которых зависят от массы вещества (
системы являются экстенсивными функциями, значения которых зависят от массы вещества (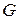 ). Обозначим любую экстенсивную функцию
). Обозначим любую экстенсивную функцию 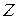 , а ее удельное значение
, а ее удельное значение 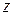 . Тогда
. Тогда 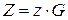 .
.
Для вычисления экстенсивной характеристики системы - влажного насыщенного пара, воспользуемся правилом аддитивности
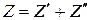 , (230)
, (230)
где 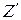 и
и 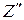 – экстенсивные характеристики кипящей воды и сухого насыщенного пара.
– экстенсивные характеристики кипящей воды и сухого насыщенного пара.
Выразим экстенсивные характеристики через соответствующие удельные величины и после их подстановки в уравнение (230) получим
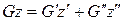 . (231 )
. (231 )
Разделим члены уравнения (231) на массу влажного насыщенного пара 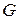 и, с учетом соотношений (226), (227), получим выражение для определения удельных значений характеристик влажного насыщенного пара
и, с учетом соотношений (226), (227), получим выражение для определения удельных значений характеристик влажного насыщенного пара
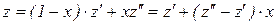 . (232)
. (232)
С помощью соотношения (232) можно записать соотношения для определения основных параметров и удельных значений функций состояния влажного насыщенного пара (удельного объема, внутренней энергии, энтальпии и энтропии):
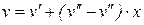 ; (233)
; (233)
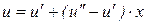 ; (234)
; (234)
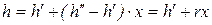 ; (235)
; (235)
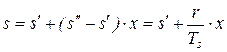 . (236)
. (236)
Энтальпия, энтропия и внутренняя энергия перегретого пара определяются из уравнений приращения этих параметров в изобарическом процессе перегрева. В связи с тем, что перегретый пар по своим свойствам близок к идеальному газу, для изобарного процесса перегрева сухого насыщенного пара с некоторой долей приближения справедливы следующие соотношения:
 ;
; 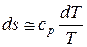 . (237)
. (237)
После интегрирования соотношений (237) от температуры насыщения Тs до температуры перегретого пара Т, получаем систему выражений для определения удельных значений функций состояния перегретого пара:
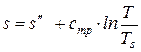 ; (238)
; (238)
 ; (239)
; (239)
 , (240)
, (240)
где 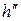 ,
, 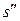 – удельные значения энтальпии и энтропии сухого насыщенного пара; сpm,
– удельные значения энтальпии и энтропии сухого насыщенного пара; сpm, 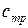 – первая и вторая средние удельные теплоемкости перегретого пара в интервале температур Т-Тs; v – удельный объем перегретого пара;
– первая и вторая средние удельные теплоемкости перегретого пара в интервале температур Т-Тs; v – удельный объем перегретого пара;
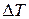 – степень перегрева.
– степень перегрева.
Область перегретого пара заключена между критической изобарой и верхней пограничной кривой (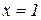 ) (рис. 20).
) (рис. 20).

Рис. 20. Диаграмма состояния h-s водяного пара
Характеристики перегретых паров различных веществ v, h, s, u, сp и сv приводятся в термодинамических таблицах водяного пара в функции от давления и температуры.
При проведении термодинамических расчетов, наряду с аналитическими методами, достаточно часто используются и графические методы расчета, проводимые с использованием энтропийных диаграмм (Т - s и h - s). На этих диаграммах (рис. 20) обычно нанесены линии нижней пограничной кривой (x=0), верхней пограничной кривой (х=1), изобары (p=idem), изохоры (v=idem), изотермы (T=idem) и линии постоянной степени сухости (x=idem).
В области влажного насыщенного пара изобары и изотермы совпадают друг с другом, так как 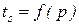 . При переходе в область перегретого пара изобары и изотермы разделяются и каждая представляет собой отдельную кривую. В области влажного насыщенного пара изобары и изотермы изображаются в диаграмме Т- s в виде горизонтальных прямых, а в диаграмме h - s – в виде наклонных прямых.
. При переходе в область перегретого пара изобары и изотермы разделяются и каждая представляет собой отдельную кривую. В области влажного насыщенного пара изобары и изотермы изображаются в диаграмме Т- s в виде горизонтальных прямых, а в диаграмме h - s – в виде наклонных прямых.
Наибольший практический интерес из этих диаграмм имеет диаграмма h - s прежде всего в силу того, что удельная работа (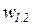 ) в адиабатном процессе, исходя из первого начала термодинамики, по этой диаграмме определяется как величина отрезка между начальными и конечными точками процесса (h1 – h2).
) в адиабатном процессе, исходя из первого начала термодинамики, по этой диаграмме определяется как величина отрезка между начальными и конечными точками процесса (h1 – h2).
В энтропийных диаграммах Т - s и h - s обратимые адиабатные (изоэнтропийные) процессы изображаются вертикальными отрезками.
Диаграмма Т - s, в основном, пользуется для термодинамического анализа различных циклов. Она позволяет по соответствующим площадям определить количество теплоты, подведенного и отведенного к рабочему телу в рассматриваемом цикле и работу цикла. При расчете процессов, в которых имеет место процесс парообразования, а рабочими телами являются различные вещества, преимущественно используется диаграмма h - s.
Date: 2015-05-09; view: 1876; Нарушение авторских прав