
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Молекулярно-кинетическая теория газов
|
|
Рассмотрим идеальный газ, содержащийся в контейнере, объем которого V. Контейнер имеет форму куба со стороной d. Молекула, двигающаяся внутри контейнера со скоростью 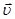 , сталкивается со стенкой контейнера. Поскольку столкновение упругое, компонента uх изменит направление, тогда как компоненты uу и uz не изменяются
, сталкивается со стенкой контейнера. Поскольку столкновение упругое, компонента uх изменит направление, тогда как компоненты uу и uz не изменяются
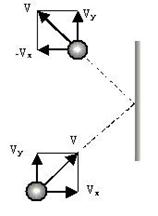
| Рис. 7.1. Движение молекулы со скоростью 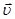 внутри контейнера и упругое столкновение ее со стенкой контейнера, вследствие чего компонента uх изменяет направление, тогда как направления компонентов uу и uz не изменяются внутри контейнера и упругое столкновение ее со стенкой контейнера, вследствие чего компонента uх изменяет направление, тогда как направления компонентов uу и uz не изменяются
|
(рис. 7.1). Изменение х- компоненты импульса молекулы можно определить выражением:
Dрx = – muх – (muх) = – 2muх. (7.4)
Для того, чтобы молекула снова столкнулась с той же самой стенкой, ей необходимо пройти расстояние 2 d за промежуток времени Dt = 2 d/uх.
Если допустить, что сила, с которой действует молекула на стенку, есть F, импульс силы будет равен:
FDt = Dр = 2muх. (7.5)
Отсюда:
F = 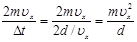 . (7.6)
. (7.6)
Общее давление, с которым действуют все молекулы на стенку, равно:
p = 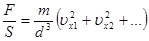 , (7.7)
, (7.7)
где 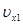 ,
, 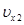 , … - х- компоненты скорости первой, второй и других молекул.
, … - х- компоненты скорости первой, второй и других молекул.
Введем понятие средней квадратической скорости молекул:
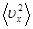 =
= 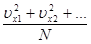 . (7.8)
. (7.8)
С учетом того, что объем V = d3, можно записать выражение для давления в виде:
р = Nm 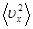 / V. (7.9)
/ V. (7.9)
Поскольку квадрат скорости одной молекулы равен:
u2 = 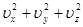 , (7.10)
, (7.10)
то с учетом того, что движение молекулы хаотическое и любое из направлений движения не имеет преимущества, можно допустить, что:
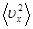 =
= 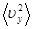 =
= 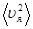 =
= 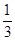
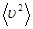 . (7.11)
. (7.11)
Здесь множитель 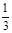 свидетельствует о том, что только треть молекул двигается вдоль ребра куба.
свидетельствует о том, что только треть молекул двигается вдоль ребра куба.
Таким образом, давление, создаваемое молекулами, равно:
р = Nm 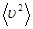 /3V. (7.12)
/3V. (7.12)
Это и есть основное уравнение молекулярно-кинетической теории газа.
7.3. МОЛЕКУЛЯРНАЯ ИНТЕРПРЕТАЦИЯ
ТЕМПЕРАТУРЫ
Уравнение (7.12) можно переписать как:
р = 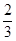 (N/V)(
(N/V)(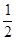 m
m 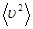 ) (7.13)
) (7.13)
или
рV = 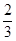 N (
N (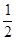 m
m 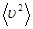 ). (7.14)
). (7.14)
Сравнивая это выражение с уравнением состояния идеального газа (7.3), получим:
T = 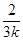
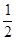 m<u2> =
m<u2> = 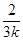 <Е>, (7.15)
<Е>, (7.15)
где <Е> = 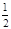 m<u2> - средняя кинетическая энергия поступательного движения одной молекулы.
m<u2> - средняя кинетическая энергия поступательного движения одной молекулы.
Таким образом, абсолютная температура идеального газа прямо пропорциональна средней кинетической энергии поступательного движения молекул.
Пример
Контейнер содержит три моля идеального газа при 20 0С. Найти полную кинетическую энергию поступательного движения молекул идеального газа.
Date: 2015-05-09; view: 712; Нарушение авторских прав