
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Уравнение состояния идеального газа. В рассмотренных ранее изопроцессах, описываемых законами Бойля - Мариотта, Гей-Люссака и Шарля, один из параметров (p,V,T) газа оставался постоянным
|
|
В рассмотренных ранее изопроцессах, описываемых законами Бойля - Мариотта, Гей-Люссака и Шарля, один из параметров (p,V,T) газа оставался постоянным. Однако чаще всего имеют место процессы, при которых изменяются все три параметра.
Поскольку изопроцессы выражаются равенствами:
pV=const, если T=const;
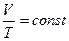 , если p=const;
, если p=const;
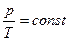 , если V=const,
, если V=const,
нетрудно догадаться, что в общем виде должно быть:
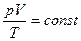 . (1.2)
. (1.2)
Действительно, эта формула в частных случаях описывает все три изопроцесса (например, если T=const, то pV=const). К этому же соотношению можно прийти без использования интуиции - путем анализа газовых процессов.
Приведем эти рассуждения в качестве примера термодинамического метода исследования систем.
Ответы на вопросы тренировочного задания, сформулированные на стр. 11
1) Т2>Т1. Если провести вертикальную прямую, соответствующую некоторому объему V*, она пересечет нижний график в точке a и верхний - в точке b. Поскольку давление в точке b больше, чем в точке a, значит, согласно закону Шарля состояние, соответствующее точке b, отвечает большей температуре.
2) р2 < р1. Точки a и b обоих графиков на рис. 1.4, отвечающие одной и той же температуре, имеют разный объем. Согласно закону Бойля - Мариотта больший объем соответствует меньшему давлению. В точке b объем больше, а, значит, давление меньше.
3) V2<V1. В точках a и b на рис. 1.5 температура одинакова, а давление разное. Используя закон Бойля - Мариотта, делаем вывод, что поскольку давление в точке b больше, чем в точке a, объем в точке a будет больше, чем в точке b.
Пусть в результате какого-то процесса изменились все три параметра (были p1, V1, T1, стали p2, V2, T2). Найдем связь между старыми и новыми параметрами газа.
Будем считать, что переход от первого состояния ко второму произошел в два этапа:
- сначала без изменения температуры T1 давление достигло значения p2 (объем тоже изменился и принял значение V');
- далее прошел изобарический процесс, в результате которого температура и объем достигли значений T2, V2.
Для нахождения объема V' можно воспользоваться законом Бойля - Мариотта:
р1V1=p2V¢=const, т.е. V¢=V1 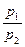 . (1.3)
. (1.3)
На втором этапе справедлив закон Гей - Люссака, следовательно, можно записать:
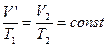 , т.е.
, т.е. 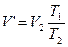 . (1.4)
. (1.4)
Так как левые части формул (1.3) и (1.4) равны, то должны быть равны и правые:
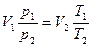 ,
,
что можно записать в виде:
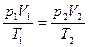 . (1.5)
. (1.5)
Таким образом, при любом процессе в разреженном газе начальные и конечные параметрами связаны равенством (1.5), а поскольку конечное состояние выбрано произвольно, можно заключить, что при любом состоянии разреженного газа произведение давления на объем, деленное на абсолютную температуру, для данной массы газа есть величина постоянная:
 . (1.6)
. (1.6)
Значение постоянной B зависит от массы и рода газа.
Date: 2015-05-09; view: 806; Нарушение авторских прав