
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Адсорбция түрлері мен теориясы
|
|
Қатты дене – сұйық зат жанасу шегіндегі адсорбция түрінің біріне жататын ион алмастырғыш адсорбцияның маңызы аса зор. Ол жан-жақты зерттелген.
Ион алмастырғыш адсорбция. Ерітіндідегі күшті электролиттер толығымен дерлік диссоциация әсерінен иондарға ыдырайтындықтан, оларға кәдімгі адсорбциялық және әр түрлі электр күштері әсер ету нәтижесінде осы электролиттерді қатты адсорбент бетінде адсорбциялаудың өз ерекшеліктері болады. Күшті электролит иондарын адсорбциялау екі тектегі күштің әсері арқылы жүреді екен. Олар адсорбенттің беттік молекулалық және иондар адсорбцияланғанда пайда болатын электр күші.
Электролит адсорбциясының үш түрі бар: эквивалентті; ауыспалы; ерекше немесе таңдамалы.
Эквивалентті адсорбция кезінде электролит молекуласы түгелдей сіңіріледі. Оны былай түсіндіруге болады. Берілген электролиттің жақсы адсорбцияланатын ионы өзінің екінші нашар адсорбцияланатын ион жұбын (электролит молекуласы екі ионнан тұрады) адсорбент бетіне тартады. Мұнда екінші ионның адсорбцияланғыш қабілеті артады да, ерітінді дегі адсорбция лайтын басқа иондар бірінші ионның адсорбциялануын төмендетеді. Сөйтіп, екі ион да бірдей (эквиваленттік жағдайда) адсорбцияланады, сондықтан да эквивалентті адсорбцияны молекулалық деп те атай береді. Ол әлсіз электролиттерге тән. Эквивалентті адсорбция жағдайында, фазалардың жанасу шегіндегі электр нейтралдылық сақталады.
Ал ауыспалы адсорбция құбылысында электролит иондарының біреуі іріктеле келіп, адсорбент бетіне жақындағанда қатты адсорбенттен осы мәндегі зарядтас басқа ион ерітіндіге алмасады. Сөйтіп электролит ерітіндісіндегі және қатты адсорбенттегі аттас иондар бірімен-бірі орын алмасады екен. Мұндай ион алмастыру құбылысы тепе-теңдік жағдайында, яғни эквивалентті түрде алмасқандықтан, екі фазаның жанасу шегі әркез электр нейтралды болады. Әдетте ауыспалы адсорбция басқа адсорбциядан баяу жүреді және оны хемосорбция процесі ретінде де қарастыруға болады.
Егер ауыспалы адсорбция кезінде адсорбент өзіне сіңірген ион орнына ерітіндіге сутектің немесе гидроксидтің эквивалентті ионын берсе, онда мұндай адсорбцияны гидролиттік деп атайды. Мысалы, натрий хлориді, калий хлориді немесе нитраты секілді нейтрал тұздардың ерітіндісін активтелген көмір арқылы өткізсе, онда активтелген көмір осы ерітіндіден өзіне аниондарды адсорбциялап, олардың орнына гидроксил тобын береді, сөйтіп ерітінді әлсіз сілтілік орта көрсетеді. Олай болса, гидролиттік ауыспалы адсорбция кезінде активті бетте, жанасу шегінде болатын көптеген ауыспалы не басқа да құбылыстарға қарамастан су болады.
“Адсорбция” тақырыбына типтік есептерді шешу.
1-Мысал.
Фрейндлих адсорбциясының изотермінің теңдеуін есептеу (к немесе 1/n) келесіге:
| Адсорбент өлшендісі, кг. | СН3СООН – тың концентрациясы. | Қосылған қышқыл, Vм3 | |
| Адсорбцияға дейінгі С1, кмоль/м3 | Адсорбциядан кейінгі Ср, кмоль/м3 | ||
| 0,65∙10-3 | 0,5522 | 0,5129 | 2,5∙10-5 |
| 0,58∙10-3 | 0,1586 | 0,1413 | 2,5∙10-5 |
| 0,57∙10-3 | 0,1248 | 0,1096 | 2,5∙10-5 |
Шешу. Фрейндлих теңдеуінің тұрақтысын анықтау.
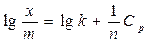 ,
, 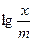 -нің
-нің 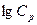 тәуелділік графигін тұрғызамыз.
тәуелділік графигін тұрғызамыз.
Бұл мәндерді есептейміз. 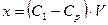 ,
,
Сонда
х1 = (0,5522-0,5129)∙2,5∙10-5 = 9,8∙10-6, x2 = (0,1586-0,1413)∙2,5∙10-5 = 4,32∙10-6
x3 = (0,1248-0,1096)∙2,5∙10-5 = 3,80∙10-6, 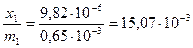
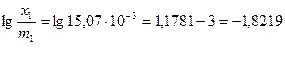
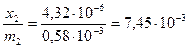
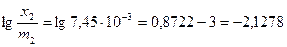 ,
, 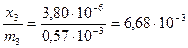
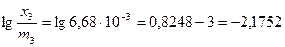 ,
, 
 ,
, 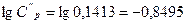 ,
, 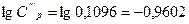
К тұрақтысын К және 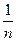 Фрейндлих теңдеуін есептейміз.
Фрейндлих теңдеуін есептейміз. 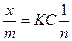
ОА = 0,35 = lg k; k=2,24 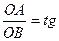
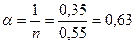
Фрейндлих теңдеуінің тұрақтысы: k = 2,24 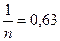
2-Мысал.
Есептелген,яғни 6∙10-3 кг памадий қарсының бетінің ауданы 2., 40,0м2 –ке тең. 1∙10-3 памадий қаарсы 1∙10-5 м3 газ тәрізді сутекті жұтады. (қалыпты жағдайжа) 1 молекула Н-нің алатын көлемін табу керек.
Есептеу. Қараның 1∙10-3 кг беттік ауданын табу:

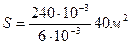
Қалыпты жағдайдағы 1∙10-5 м3 сутегі 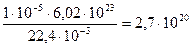 молекуласы бар.
молекуласы бар.
Бір молекуланың алатын көлемі, 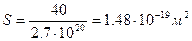
Есептер:
1. Фрейндлих адсорбциясының изотермінің теңдеуінің тұрақтысын есептеу. таблица бойынша (К және 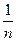 ).
).
| Адсорбент өлшендісі, кг | СН3СООН концентрациясы | Қосылған қышқыл (әдіске алынған),Vм3 | |
| Адсорбцияға дейінгі С1 кмоль/м3,(орташа мәні) | Адсорбциядан кейінгі С2, кмоль/м3 (орташа мәні) | ||
| 3∙10-3 а) 3∙10-3 3∙10-3 | C1=0.7389 C1=0.2594 C1=0.0933 | C2=0.7079 C2=0.2399 C2=0.0851 | 1.5∙10-4 1.5∙10-4 1.5∙10-4 |
| 3,5∙10-5 б) 3,5∙10-5 3,5∙10-5 | C1=0.6647 C1=0.3019 C1=0.1104 | C2=0.6310 C2=0.2818 C2=0.100 | 1.5∙10-4 1.5∙10-4 1.5∙10-4 |
| 2∙10-3 в) 2∙10-3 2∙10-3 | C1=0.8275 C1=0.2134 C1=0.1218 | C2=0.7943 C2=0.1995 C2=0.1122 | 1∙10-4 1∙10-4 1∙10-4 |
| 1∙10-3 г) 1∙10-3 1∙10-3 | C1=0.8026 C1=0.2348 C1=0.1022 | C2=0.7943 C2=0.2399 C2=0.100 | 2∙10-4 2∙10-4 2∙10-4 |
| 1,5∙10-3 д) 1,5∙10-3 1,5∙10-3 | C1=0.5693 C1=0.2947 C1=0.1497 | C2=0.5495 C2=0.2818 C2=0.1413 | 1∙10-4 1∙10-4 1∙10-4 |
| 2∙10-3 е) 2∙10-3 2∙10-3 | C1=0.6491 C1=0.2082 C1=0.0902 | C2=0.6310 C2=0.1995 C2=0.0851 | 1.6∙10-4 1.6∙10-4 1.6∙10-4 |
Есепті шешу үшін тәуелділік графигін тұрғызу керек. 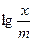 және
және 
2. Яғни 1 молекула сутектің алатын көлемі 1,38∙10-19м2, ал 1∙10-3 кг платина қарасымен адсорбцияланған сутектің мөлшері 12,0∙10-6 м3, қалыпты жағдайда. Бетін анықтау.
а)2∙10-3кг платина қарасы, б)3∙10-3кг платина қарасы, в)4∙10-3кг платина қарасы, г) 5∙10-3кг платина қарасы, д) 6∙10-3кг платина қарасы
е) 7∙10-3кг платина қарасы
3. Олеин қышқылының 1 молекуласын алатын көлемі 4*10-19м2, ал активтелген көмірдің ауданы 3*105м2/кг. Неше молекула олеин қышқылы адсорбциялануы мүмкін.
а) 2∙10-3 активтелген көмір, б) 3∙10-3 активтелген көмір,в) 4∙10-3 активтелген көмір, г) 5∙10-3 активтелген көмір,д) 6∙10-3 активтелген көмір, е) 7∙10-3 активтелген көмір.
4. 1∙10-6м3 көмірдің ауданы 800м2, қалыпты жағдайда қанша көлем аммиак адсорбцияла нады,шекті жағдайда, яғни молекулалар бір-біріне жақындағанда:
а) 2∙10-6м3 б) 3∙10-6м3 в) 4∙10-6м3 г) 5∙10-6м3
д) 6∙10-6м3 е) 7∙10-6м3 ж) 8∙10-6м3
Аммиак молекуласының диаметрі 2,8*10-10м. Молекула ауданын мына формуламен есеп ейміз. 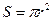
Date: 2015-05-08; view: 3658; Нарушение авторских прав