
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Катты дене газ шегіндегі адсорбция
|
|
Газдардың қатты денемен жанасу бетінде адсорбциялануы екі компоненттен тұратын ең қарапайым жүйе. Көптеген тәжірибелер көрсетіп отырғандай, адсорбцияланған газдың мөлшері оны адсорбциялайтын активті беттің ауданы көбейген сайын артады екен. Үлкен мәндегі адсорбция құбылысын жүргізу үшін сіңіретін заттың активті беті (ауданы) үлкен болуы қажет. Адсорбенттің өзіне сіңіру қабілеті, оның тек қуыстығымен ғана анықталып қоймастан, оның физикалық күйімен де сипатталады: айталық, аморфты күйдегі адсорбент, кристалды күйден гөрі әлдеқайда артықтау адсорбциялайды, яғни аморфты күйдегі адсорбенттің адсорбциялау қабілеті басым.
Қолданылмалы жағдайда қатты адсорбенттер ретінде ағаштан және сүйектен алынатын активтелген көмір, силикагель, оксидін тотықсыздандыру арқылы алынған аса жоғары дисперстелген (ұнтақталған) металдар жиі қолданылады. Активтелген көмірді арнайы жағдайдағы шартқа сәйкес, ағаштардың арнайы түрін өңдеп алады. Осылайша алынған ағаш көмірі әлі активті емес. Оны активтендіру үшін, яғни ағаш көмірінің активті бетін көбейту мақсатымен оны термиялық әдіспен өңдейді. Бұл процесс су буы мен көміртек (IV) оксидінің атмосферасында 973-1173К температурада жүреді. Мұндай жағдайдағы ағаш көмірі көміртек (IV) оксидімен және су буымен әрекеттесіп, көміртек (II) оксидін және сутек түзеді. Осы өңдеу нәтижесіндегі көмір құрылымының өзгеруі 3-сурет көрсетілген. Активтелген көмір улы газдармен жұмыс істегенде, өнеркәсіптегі өңдірістік ауаны тазартуда қолданады.
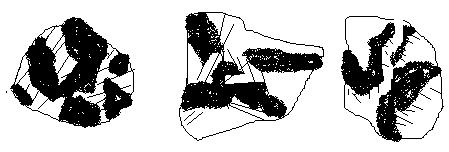
а б в
4-сурет. Көмір құрылымының өзгеруі
Активтелген көмірдің өте жоғары адсорбциялық қабілет көрсетуі ондағы активті беттің жақсы дамуында. Мысалы, мұндай активтелген көмірдің бір грамындағы қуыс беттерді жинастырса, онда ол 300-1000м2 ауданға теңеледі. Әрине мұнда үлкен молекулалық күш өрісі туындайды да, ол көмір-газ арасындағы жанасу беттегі энергия қорын арттырады. Осы беттегі бос энергия есебінен газ көмір бетіне адсорбцияланады, яғни активті көмір бетіндегі газ концентрациясы артып, айналадағы газ азаяды. Көптеген зерттеулер көрсеткендей, газ молекулаларының активті көмір бетінде болу мерзімі өте аз екен; ол адсорбент бетінде бір секундтың жүзден, тіпті, мыңнан бір бөлігіндей ғана уақыт болып, басқа бөлшекпен ауысады. Бұл құбылыстың соңында бос жүрген молекулалар арасында динамикалық тепе-теңдік орнайды. Мұндай динамикалық тепе-теңдікке жету жылдамдығы әр түрлі газдар үшін әр мәнде болады: мысалы, активтелген көмір көміртек (IV) оксидін адсорбциялағанда тепе-теңдік 20 секундтан кейін орнаса, оттекті адсорбциялағанда 2,5 сағатта, ал азотты адсорбциялағанда 20 сағатта орнайды екен. Ал адсорбция жылдамдығының маңызы ерекше. Мысалы, улы газдармен жұмыс жүргізгендегі адсорбциялық құбылыстың жылдамдығы өзінен-өзі ерекше, өйткені оны тез арада тазаламаса, онда мұндай ортада жұмыс істеу мүмкін емес. Кейде оның жылдамдығын улы газ өтетін адсорбент қабатын қалыңдату арқылы да арттырып, адсорбция әсерін жоғарылатады.
Улы газдармен жұмыс істегенде одан қорғаушы құрал ретінде қолданылатын аспаптағы активтелген көмір көптеген улы газдар мен қосылыстарды өзіне адсорбциялап, ұстап қана қоймай олардың басым көпшілігіне катализатор ретінде әсер етіп, ыдыратады. Мысалға аса улы қосылыс - фосгеннің активтелген көмір бетінде адсорбция әсерінен ұсталып, сонан соң оның катализдік процесс салдарынан ыдырауын келтіруге болады:
COCl2 + H2O 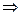 2HCl + CO2 (19)
2HCl + CO2 (19)
немесе хлорпикрин улы қосылысын алсақ:
CCl3NO2 + 2H2O 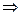 CO2 + 3HCl + HNO3
CO2 + 3HCl + HNO3  (20)
(20)
Көптеген тәжірибе көрсетіп отырғандай, адсорбция құбылысы тек өзіне сіңіретін заттың ғана қаситі мен құрылысына тәуелді емес, ол ондағы сіңетін заттың да сипатына байланысты екен (2-кестеде тұрақты қысым кезінде кейбір газдардың көмірге адсорбциялануы келтірілген).
Адсорбция құбылысын түсіндіруге арналған бірнеше теория бар. Олардың бірі - физикалық теория. Бұл теорияға орай, адсорбциялық күш табиғаты молекулааралық куштердің пайда болуына сәйкес келеді. Ал, енді химиялық теорияға жүгінсек, адсорбция жүретін беттегі орналасқан молекулаларда болатын қанықпаған, яғни бос валенттілік есебінен химиялық күш туындайды және ол күш салдарынан байланыс құралып, адсорбция жүреді.
№ 3-кесте. Тұрақты қысымдағы газдардың көмірге адсорбциялануы.
| Газ | С м3/мкг | Т қайнау К | Т криз К | Газ | С м3/мкг | Т қайнау К | Т криз К |
| COCl2 O2 NH3 H2S HCl N2O | CO2 CO O2 N2 H2 |
Физикалық адсорбция теориясының бірнеше түрлері белгілі. Олардың арасында 1915 жылы Ленгмюр ұсынған мономолекулалық адсорбция теориясы едәуір назар аударарлықтай. Бұл теорияны тұжырымдарда, оның авторы бірнеше қағидаларға сүйенді:
1. Адсорбция валентті күштер не артылып қалған (қосымша) химиялық
валенттілік күштері арқылы жүзеге асады.
2. Адсорбция берілген адсорбент бетінің бәрінде бірдей жүре бермей, тек ондағы активті орталықтарда ғана жүреді. Осы активті орталықтардың әсері онда пайда болатын қанықпаған күш өрісінің күшті болу салдарынан және соның нәтижесінде осы орталықтарда газ молекулалары ұсталынып тұрады. Әрине, мұндағы адсорбент атомы не молекуласы аз қаныққан сайын, активті орталықтардың активтілігі артық болады.
3. Адсорбциялық күштердің әсер етуші радиусы кіші және осының салдарынан әрбір активті орталық адсорбтив молекуласының біреуін ғана адсорбциялайды, сөйтіп адсорбент бетінде адсорбтив молекуласының бір молекулалық (мономолекулалық) қабаты пайда болады.
4. Адсорбент бетіне адсорбцияланған газ молекулалары онда берік ұсталмайды: олар ылғи тоқтаусыз газды орта мен сол шеңберде алмасуда болады және бұл құбылыс динамикалық адсорбция тепе-теңдігі орнағанша жүреді. Осы құбылыстар кезіндегі әрбір молекула өзі адсорбцияланған бетте, дәлірек айтқанда активті орталықта аса ұзақ уақыт ұсталып тұра бермейді, энергияның басқа молекулаларға ауысуына орай, әуелгі молекулалар жаңадан келгендерге орнын береді.
Химиялық адсорбцияны немесе хемосорбцияны физикалық адсорбциямен салыстырғанда ол химиялық күш арқылы не соның көмегімен жүзеге асады. Адсорбцияның бұл түрі басқалардан мынадай өзгешеліктерімен оқшауланады: физикалық адсорбция - қайтымды құбылыс, ал хемосорбция қайтымсыз және физикалық адсорбция жылуы небәрі 8,4-33,5 кДж/моль шамасында болса, ал химиялық адсорбция жылуы бірнеше жүздеген кДж/мольге тең. Температура жоғарлаған сайын физикалық адсорбция төмендесе, химиялық адсорбия жоғарылайды. Химиялық адсорбция жүру үшін, оған біршама көбірек активтендіру энергиясы (40-120 кДж/моль) қажет.
Химиялық адсорбция қайтымсыз болғандықтан, бұл процестегі десорбция адсорбцияланған молекуланы жай ғана жұлып алумен аяқталмайды, адсорбцияланған беттегі химиялық қосылыстың ыдырауымен бітеді. Химиялық адсорбцияға бірден-бір мысал ретінде активті көмірдің оттекті адсорбциялауын алуға болады.
Егер оттекпен адсорбцияланған активтелген көмірді ауасыз ортада қыздырса, одан таза көмір (көміртек) бөлінбестен, көміртек (IV) оксиді бөлінеді.
Адсорбция құбылысына қазіргі теория мен қолданылмалық тарапынан қарасақ, онда физикалық әрі химиялық күштердің болатыны аңғарылады, яғни адсорбция физикалық-химиялық құбылыс екен. Оны совет ғалымдары Н. А. Шилов, М. М. Думанский мұқият зерттей келіп, адсорбент пен адсорбцияланушы заттар арасындағы әрекеттесулерде физикалық және химиялық құбылыстардың өзіндік орны болатынын дәлелдеді. Бұл, әсіресе, газдар адсорбцияланған кезде айқын көрінеді. Мұндағы зерттеулерге назар салса, әуелі газдар таза адсорбент бетімен жанасқанда химиялық адсорбция жүреді екен, өйткені осы тұста химиялық күш әсер етеді, ал сонан соң адсорбция құбылысы онан әрі жалғасса және осы кезде қысымды арттырса, онда физикалық адсорбция жүреді.
Date: 2015-05-08; view: 2136; Нарушение авторских прав