
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Номенклатура кислот. Кислотные остатки
|
|
Традиционные русские названия бескислородных кислот составляются в последовательности: «корень русского названия соответствующего галогена или халькогена» + «суффикс «о» + «водородная»: HF – фтор о водородная, HCl – хлор о водородная, HBr – бром о водородная, H2S – сер о водородная. Кислота HCN имеет название «циан о водородная».
Названия кислородосодержащих кислот производятся от русских названий кислотоообразующих элементов с различными суффиксами, которые необходимо строго выдерживать.
Если элемент образует две кислоты, то используются суффиксы - н и - ист: первый – при максимальной степени окисления кислотообразующего элемента, а второй – если степень окисления данного элемента ниже максимальной. Пример:
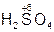 – сер н ая кислота,
– сер н ая кислота,  – серн ист ая кислота;
– серн ист ая кислота;
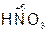 – азот н ая кислота,
– азот н ая кислота,  – азот ист ая кислота.
– азот ист ая кислота.
В названиях некоторых кислот суффикс -н заменяется суффиксами - ов и -ев: H2CrO4 – хром ов ая кислота, H2SiO3 – кремни ев ая кислота.
Галогены хлор, бром и иод, кроме бескислородных образуют по четыре кислородосодержащих кислоты, в которых степени окисления атомов галогенов равны +7, +5, +3 и +1. В названиях этих кислот используются соответственно суффиксы -н, -оват, -ист и -оватист: HClO4 – хлор н ая, HClO3 – хлорн оват ая, HClO2 – хлор ист ая, HClO – хлорн оватист ая.
Существуют кислоты различного состава, в молекулах которого атомы элемента-кислотообразователя находятся в одной и той же степени окисления. В этом случае к названию кислоты с наименьшим содержанием атомов водорода и кислорода добавляется префикс (приставка) мета -, с наибольшим – орто -, а при промежуточном содержании атомов водорода и кислорода (в расчёте на один атом кислотообразуещего элемента) – пиро-: HPO3 – мета фосфорная кислота, H3PO4 – орто фосфорная кислота, H4P2O7 – пиро фосфорная кислота.
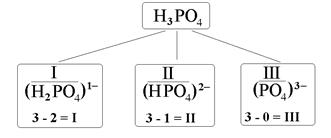 При отщеплении атомов водорода от молекул кислот образуются кислотные остатки. Общее число остатков кислоты совпадает с её основностью. Как вы уже знаете, валентность кислотного остатка равна разности между числами атомов H в формулах кислоты и данного остатка. Заряды кислотных остатков всегда отрицательны и численно совпадают с их валентностью. Например, фосфорной кислоте соответствуют три кислотных остатка – H2PO4, HPO4 и PO4, валентность которых равна, соответственно, I, II и III, а их заряды составляют 1–, 2– и 3– (рис. 2).
При отщеплении атомов водорода от молекул кислот образуются кислотные остатки. Общее число остатков кислоты совпадает с её основностью. Как вы уже знаете, валентность кислотного остатка равна разности между числами атомов H в формулах кислоты и данного остатка. Заряды кислотных остатков всегда отрицательны и численно совпадают с их валентностью. Например, фосфорной кислоте соответствуют три кислотных остатка – H2PO4, HPO4 и PO4, валентность которых равна, соответственно, I, II и III, а их заряды составляют 1–, 2– и 3– (рис. 2).
 Названия важнейших кислот и соответствующих кислотных остатков приведены в Приложении 1.
Названия важнейших кислот и соответствующих кислотных остатков приведены в Приложении 1.
Date: 2015-11-13; view: 637; Нарушение авторских прав