
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Химическая кинетика. Химическая кинетика –это раздел химии, изучающий скорость протекания химических реакций и факторы, влияющие на нее
|
|
Химическая кинетика – это раздел химии, изучающий скорость протекания химических реакций и факторы, влияющие на нее. Химические реакции бывают гомогенными и гетерогенными. Если реагирующие вещества находятся в одной фазе – это гомогенная реакция, а если в разных – гетерогенная.
Фаза – это часть системы, отделенная от других частей поверхностью раздела, при переходе через которую свойства системы изменяются скачкообразно.
Примером гомогенной реакции служит взаимодействие растворов AqNO3 и NaCl. Эта реакция протекает быстро и по всему объему:
AqNO3 + NaCl = AqCl + NaNO3.
 Примером гетерогенной реакции является процесс растворения цинка в растворе серной кислоты:
Примером гетерогенной реакции является процесс растворения цинка в растворе серной кислоты:
Zn + H2SO4 = ZnSO4 + H2
Скоростью гомогенной реакции называется изменение концентрации вещества, вступающего в реакцию или образующегося в ходе реакции ∆С в единицу времени ∆t 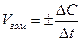 ,
,
(+) – ставится в том случае, если следят за изменением концентрации продуктов реакции, которая в ходе реакции увеличивается;
(-) – когда следят за изменением концентрации исходных веществ, которая в ходе реакции уменьшается.
Скоростью гетерогенной реакции называется изменение количества вещества, вступающего в реакцию или образующегося в ходе реакции ∆n в единицу времени ∆t на единице площади ∆S:
 .
.
Date: 2015-10-19; view: 442; Нарушение авторских прав