
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Химические свойства металлов. Цель работы:практически ознакомиться с характерными химическими свойствами металлов различной активности и их соединений; изучить особенности металлов с
|
|
Цель работы: практически ознакомиться с характерными химическими свойствами металлов различной активности и их соединений; изучить особенности металлов с амфотерными свойствами; окислительно-восстановительные реакции уравнять методом электронно-ионного баланса.
Теоретическая часть
Физические свойства металлов. Вобычных условиях все металлы, кроме ртути, – твердые вещества, резко отличающиеся по степени твердости. Металлы, являясь проводниками первого рода, обладают высокой электропроводностью и теплопроводностью. Эти свойства связаны со строением кристаллической решетки, в узлах которой находятся ионы металлов, между которыми перемещаются свободные электроны. Перенос электричества и тепла происходит за счет движения этих электронов.
Химические свойства металлов. Все металлы являются восстановителями, т. е. при химических реакциях они теряют электроны и превращаются в положительно заряженные ионы. Вследствие этого большинство металлов реагирует с типичными окислителями, например, кислородом, образуя оксиды, которые в большинстве случаев покрывают плотным слоем поверхность металлов.
Mg° +O2°=2Mg+2O-2;
Mg – 2 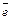 =Mg+2;
=Mg+2;
О2+4 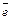 =2О-2.
=2О-2.
Восстановительная активность металлов в растворах зависит от положения металла в ряду напряжений или от величины электродного потенциала металла (табл.8.1). Чем меньшей величиной электродного потенциала обладает данный металл, тем более активным восстановителем он является. Все металлы можно разделить на 3 группы:
1. Активные металлы – от начала ряда напряжений (т. е. от Li) до Mg;
2. Металлы средней активности от Mg до H;
3. Малоактивные металлы – от Н до конца ряда напряжений (до Au).
Date: 2015-09-24; view: 958; Нарушение авторских прав