
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Способи добування кислот
|
|
1. Взаємодія кислотних оксидів з водою. Більшість кислотних оксидів безпосередньо реагують з водою з утворенням оксигеновмісних кислот.
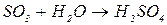
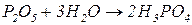
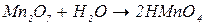
2. Реакціями обміну між солями слабких кислот та сильними кислотами добувають відповідні слабкі кислоти:
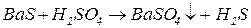
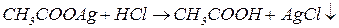
3. Реакціями обміну, в результаті яких утворюється нерозчинні солі:
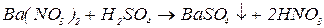
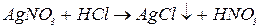
4. Взаємодією неметалів з воднем можна добути деякі сполуки, водні розчини яких є безоксигеновими кислотами:
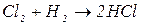
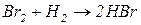
Основи
Основами називають сполуки, які складаються з катіона металу та гідроксогруп 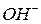 . Необхідно зазначити, що
. Необхідно зазначити, що 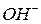 - це гідроксид-аніон, заряд якого дорівнює -1. Число гідроксид-аніонів в основі визначається ступенем окислення металу.
- це гідроксид-аніон, заряд якого дорівнює -1. Число гідроксид-аніонів в основі визначається ступенем окислення металу.
Назва основи складається зі слів гідроксид + назва металу в родовому відмінку. Якщо метал виявляє змінну валентність, її вказують римською цифрою в дужках після назви металу. Наприклад, 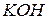 - гідроксид калію;
- гідроксид калію; 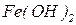 - гідроксид феруму (ІІ);
- гідроксид феруму (ІІ); 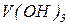 - гідроксид ванадію (ІІІ).
- гідроксид ванадію (ІІІ).
Число гідроксигруп 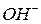 , зв’язаних з катіоном металу, визначає кислотність основи. Наприклад,
, зв’язаних з катіоном металу, визначає кислотність основи. Наприклад, 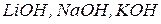 - однокислотні основи;
- однокислотні основи; 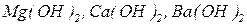 - двокислотні;
- двокислотні; 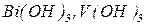 - трикислотні.
- трикислотні.
Основи можна розділити за їхньою здатністю до дисоціації у водних розчинах на слабкі (наприклад 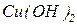 ,
,  ,
, 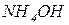 , які дисоціюють частково та оборотно) та сильні (
, які дисоціюють частково та оборотно) та сильні (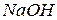 ,
, 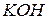 ,
, 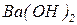 тощо), які дисоціюють практично повністю та необоротно. Сильні основи часто також називають лугами.
тощо), які дисоціюють практично повністю та необоротно. Сильні основи часто також називають лугами.
Основи реагують:
а. з кислотами з утворенням солей та води:
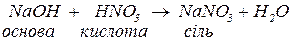
Якщо основа багатокислотна, в реакціях з кислотами можуть утворюватись декілька солей в залежності від молярних співвідношень основи та кислоти. Наприклад, в реакції між гідроксидом магнію та хлоридною кислотою з молярним співвідношенням 1:1 утворюється основна сіль (продукт неповного заміщення гідроксигруп основи на кислотні залишки):
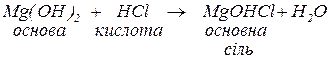
Якщо це співвіднонення становитиме 1:2 (надлишок кислоти) утворюється середня сіль як продукт повного заміщення гідроксигруп основи кислотними залишками:
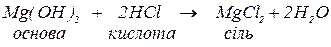
б. з кислотними оксидами з утворенням солей тих кислот, яким відповідають ці кислотні оксиди:
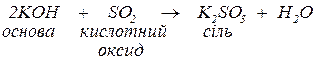
Кислотному оксиду 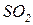 відповідає кислота
відповідає кислота 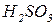 , тому в цій реакції утворюється її сіль
, тому в цій реакції утворюється її сіль 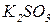 .
.
в. з амфотерними гідроксидами:
Якщо ця реакція проходить у водному розчині, утворюється комплексна сіль.
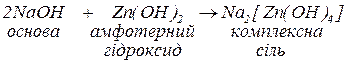
Якщо ця реакція проходить за високої температури, утворюється сіль.
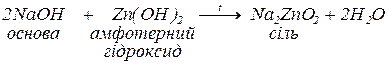
г. з амфотерними оксидами з утворенням солей (за високої температури):
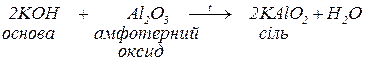
д. з солями, якщо в результаті реакції обміну утворюється нерозчинний у воді гідроксид або нерозчинна сіль:
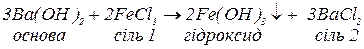
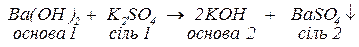
Date: 2015-09-05; view: 974; Нарушение авторских прав