
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Кислотно-основное взаимодействие
|
|
Кислотно-основные методы
Краткие теоретические основы метода
Кислотно-основное взаимодействие
Методы кислотно-основного титрования основаны на использовании реакции нейтрализации между кислотами и основаниями, которую можно представить уравнением:
HCl + NaOH → NaCl + H2O
или в общем виде:
H3O+ + B 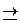 BH+ + H2O
BH+ + H2O
Согласно протолитической теории Бренстеда и Лоури – кислота – вещество (или частица), способное отдавать протоны, а основание – вещество (или частица), способное их присоединять. Таким образом, суть кислотно-основного взаимодействия состоит в переносе протонов от кислоты (донор протонов) к основанию (акцептор протонов).
Свойство соединений вступать в кислотно-основное взаимодействие характеризуется константой диссоциации, которая представляет отношение равновесных концентраций продиссоциированных молекул к их общей концентрации:
AB 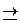 A+ + B-
A+ + B-
K дисс = 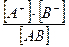
Сила кислоты в водном растворе определяется тем, насколько она полно будет отдавать протоны молекулам воды, а сила основания – насколько полно оно акцептирует протоны молекулы воды, и оценивается константой равновесия реакции переноса протона между ними и молекулой растворителя. Чем наибольшее значение константы равновесия, тем сильнее кислота и основание. Для кислот константа равновесия обозначается KA, а для оснований – KB. Однако, обычно используют значения отрицательных логарифмов этих величин, соответственно, рКА и рКВ:
рКА = - lg КА рКВ = - lg КВ
На практике для унификации используемых характеристик для кислот и оснований в настоящее время принято обозначение «рКА». Для водного раствора исходят из уравнения:
рКА + рКВ = 14, отсюда,
рКА = 14 - рКВ
Исходя из этого, чем больше рКА основания, тем оно сильнее и соответственно, чем меньше рКА кислоты, тем она сильнее.
В табл.2 приведена ориентировочная классификация кислот и оснований по «силе» в зависимости от величин их рКА.
Таблица 2
Классификация кислот и оснований в зависимости от величины их рКА
| Кислота | рКА | Основание | рКА |
| сильная | < 3 | сильное | > 10 |
| средней силы | 3 – 5 | средней силы | 10 – 8 |
| слабая | 5 – 8 | слабое | 8 – 6 |
| очень слабая | > 8 | очень слабое | < 6 |
В табл.3, 4 приведены значения рКА для ряда кислот и оснований в различных растворителях.
Таблица 3
Величины рКА кислот в различных растворителях (рКА = -lgКА)
(ГФ XI, вып.1, стр. 128)
| Кислота | Растворитель | |||||||||
| Вода | Метиловый спирт | Этиловый спирт 95% | Ацетон | Диметил-формамид | Диметил-сульфоксид | Пиридин | Уксусная кислота | Муравьиная кислота | Уксусный ангидрид | |
| Соляная | 0,8 | 1,05 | 1,95 | 8,90 | 3,80 | - | 5,4 | 5,30 | 0,89 | 8,9 |
| Муравьиная | 3,75 | - | 9,15 | - | 12,9 | 11,6 | - | - | - | - |
| Бензойная | 4,20 | 9,52 | 10,13 | 11,95 | 11,55 | - | 8,84 | - | - | - |
| Салициловая | 2,89 | 7,90 | 8,60 | 9,53 | 8,95 | 7,40 | - | - | - | - |
| Никотиновая | 4,73 | - | - | 16,6 | 8,30 | 6,80 | - | - | - | - |
| Фенол | 9,89 | 14,2 | - | - | 10,6 | - | - | - | - | - |
| Ацетилсалициловая | 3,50 | - | - | - | - | - | - | - | - | - |
| Барбитал | 7,43 | 12,69 | - | - | 11,30 | - | - | - | - | - |
| Фенобарбитал | 7,21 | - | - | 19,20 | - | 13,0 | - | - | - | - |
| Уксусная | 4,75 | 9,70 | 10,41 | 12,55 | 1,80 | - | 4,36 | - | - | 4,90 |
| Барбитуровая | 4,01 | - | - | - | 10,80 | 9,60 | - | - | - | - |
| Винная (I) | 3,03 | 7,04 | - | - | - | - | 6,67 | - | - | - |
| Лимонная (I) | 3,10 | - | - | - | 8,90 | - | - | - | - | - |
| Метилурацил | 9,70 | - | - | - | 13,0 | - | - | - | - | - |
| Рутин (I) | 8,96 | 10,34 | - | 3,15 | 12,20 | 10,80 | - | - | - | - |
| Неодикумарин (I) | 4,37 | 5,71 | - | 7,37 | 5,75 | 6,23 | - | - | - | - |
| Сульфадимезин | 7,51 | - | - | 19,60 | 13,40 | 10,98 | - | - | - | - |
Таблица 4
Величины рКА оснований в различных растворителях
(рКА=рКI – рКВ=рКТ) (ГФ XI, вып.1, стр.130 – 131)
| Основание | Растворитель | |||||||||
| Вода | Метиловый спирт | Этиловый спирт 95% | Ацетон | Метилэтил-кетон | Диметил-формамид | Диметил-сульфоксид | Муравьиная кислота | Уксусная кислота | Уксусный ангидрид | |
| Аммиак | 9,30 | - | - | - | - | 9,45 | 10,50 | - | - | - |
| Эфедрин | 9,70 | - | - | - | - | 9,50 | - | - | - | 8,90 |
| Атропин | 9,60 | - | - | - | 13,71 | - | - | - | - | 11,30 |
| Новокаин | 8,80 | - | - | - | - | 8,60 | - | - | - | 11,30 |
| Димедрол | 8,20 | - | - | - | - | 7,70 | - | - | - | - |
| Кодеин | 8,0 | 8,60 | 11,40 | 9,62 | 11,18 | 8,30 | - | 5,11 | - | 10,80 |
| Морфин | 7,80 | 8,60 | - | 9,57 | - | 8,30 | - | 5,08 | - | - |
| Хинин | 8,0 | - | - | - | - | 8,75 | - | - | - | 11,50 |
| Этилморфин | 7,90 | - | - | - | - | - | - | - | - | 11,10 |
| Гексаметилен- тетрамин | 4,90 | - | - | - | 9,80 | - | - | - | 9,70 | 7,00 |
| Платифилин | 8,10 | - | - | - | - | - | - | - | - | 11,50 |
| Пилокарпин | 6,80 | - | - | - | - | - | - | - | - | 10,90 |
| Дибазол | 4,20 | - | - | - | - | 6,40 | - | - | - | 9,0 |
| Кофеин | 0,60 | - | - | - | - | - | - | 5,17 | - | 6,30 |
| Папаверин | 5,90 | 6,92 | - | 8,03 | - | 6,60 | - | - | - | 10,80 |
Date: 2015-09-18; view: 3745; Нарушение авторских прав