
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

ЭЛЕКТРОСТАТИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ 9 page
|
|
| а) б) ' 9 ДЯ ' SSL -0,4-0,2 0 0t2 Ofi Тл |
|
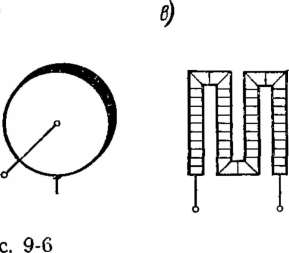
у которой один электрод укреплен в центре, а другой — в виде обода на окружности. У такого преобразователя нет граней для концентрации носителей заряда, вследствие чего уменьшается влияние эффекта Холла. Недостатком маг- ниторезисторов в виде дисков Корбино и коротких прямоугольных пластинок является их малое начальное сопротивление. Для увеличения этого сопротивления маг- ниторезисторы выполняются в виде ряда коротких полупроводниковых резисторов, соединенных последовательно проводящими слоями (растрами) (рис. 9-6, в). Это позволяет создавать магииторезисторы с сопротивлением несколько кнлоом при сохранении большого значения коэффициента А.
В последнее время магниторези- сторы выполняют из эвтектического сплава, в котором методом направленной кристаллизации образуются тонкие (d = 1 мкм) иглы из антимонида никеля (NiSb), которые равномерно располагаются параллельно друг к Другу на расстоянии 20—400 мкм в толще полупроводника. Поскольку удельная проводимость NiSb на 2—3 порядка больше, чем у InSb, то эти иглы выполняют роль проводящих растров высокоомных магниторези- сторов.

|
Основными метрологическими характеристиками магниторезисторов являются начальное сопротивление RG, которое лежит в пределах от долей ома до десятков ки- лоом, и магниторезистивиая чувствительность SB = dR/dB. Обычно для характеристики магниторезистивных преобразователей используют зависимости hRB/RQ = — F (jB), где ARB = RB — На рис. 9-7 показано семейство таких зависимостей для четырех магниторезисторов, отличающихся отношением длины резистора к площади его сечения. Наибольшую чувствительность имеет магниторезистор в виде диска Корбино (кривая 4). Ток питания магниторезистора, находящегося в магнитном поле с индукцией Въ должен выбираться значительно меньше (см. § 5-1) начального допустимого тока /0 (при В — 0), указываемого в таблицах. Значение допустимого тока fBl определятся по формуле = Начальный ток /0 для разных типов магниторезисторов лежит в диапазоне 1—100 мА. Рабочий' диапазон температур магниторезисторов составляет от —271 до +327 °С. Для работы при низких температурах весьма перспективны магниторезисторы из антимонида индия.
Температурный коэффициент сопротивления магниторезисторов (ТКС) зависит от состава материала, магнитной индукции и температуры. Чем больше чувствительность магниторезистора, тем больше его ТКС. Значения ТКС различных типов магниторезисторов имеют пределы 0,0002—0,012 К"1.
Частотные характеристики магниторезисторов в основном определяются межэлектродными емкостями. У дисков Корбино частотная погрешность меньше, чем у прямоугольных преобразователей, для которых при изменении частоты от 0 до 10 МГц магниторезистивная чувствительность уменьшается на 5—10%.
Магниторезистивные преобразователи находят применение в качестве бесконтактных переменных резисторов и делителей напряжения с плавно регулируемым коэффициентом деления, модуляторов малых постоянных токов и напряжений, Таблица 9-3 используются для создания тесламетров для работы при сверхнизких температурах и датчиков для измерения ряда неэлектрических величин, легко преобразуемых в изменение магнитной индукции, и бесконтактного измерения токов [8].
Магнито диоды представляют собой диоды с несимметричным р-я-переходом, в котором под действием магнитного поля уменьшается подвижность и концентрация носителей зарядов, вследствие чего увеличивается прямое сопротивление перехода и при заданном токе увеличивается падение напряжения на р-и-переходе. Характеристики выпускаемых магнитодиодов приведены в табл. 9-3. Допустимая мощность для всех приведенных в табл. 9-3 диодов составляет 0,2 Вт при температуре окружающей среды ©оКр = 25 °С, допустимый диапазон температур от —60 до Н-85 °С, частотный диапазон по электрическому и магнитному полям 0—1 кГц.
| i в | 2 / | |
| Рис. 9-8 |
Очевидным преимуществом магнитодиодов является их высокая чувствительность, однако пока метрологические характеристики магнитодиодов, такие, как нелинейность и разброс характеристик, чувствительность к температуре, трудность ориентации в магнитном поле, затрудняют их применение для измерения параметров магнитных полей. Магнитодиоды применяются в качестве бесконтактных потенциометров, переключателей и реле.
9-3. ГАЛЬВАНОМАГНИТОРЕКОМБИНАЦИОННЫЕ
ПРЕОБРАЗОВАТЕЛИ
Гальваномагниторекомбинационные преобразователи (ГМРП) основаны на изменении средней концентрации носителей заряда под действием магнитного поля, проявляющемся в проводниках, которые имеют поверхности с разной скоростью
рекомбинации носителей зарядов. ГМРП.обычно представляет собой тонкую полупроводниковую пластинку (рис. 9-8), у которой одна из боковых поверхностей (/) грубо обработана (пескоструйка, грубая шлифовка), а другая (2) — отполирована. Вследствие этого у поверхности / скорость рекомбинации носителей зарядов на 2—3 порядка больше, чем у поверхности 2.
| Тип | Параметр | |
| магнито- | и, в | S, В/Тл |
| диода | (при / =3 мА, | (при I = |
| В =0) | = 3 мА) | |
| КД 301А | 6—7,5 | |
| КД 301Б | 7,5—9 | |
| КД 301В | 9—10,5 | |
| КД 301Г | 10,5—12 | |
| КД 301Д | 12—13,5 | |
| КД 301Е | 13,5—15 | |
| КД 301Ж | 15—20 |
Если ГМРП находится в магнитном поле так, что вектор магнитной индукции направлен перпендикулярно вектору плотности тока через ГМРП и параллельно плоскостям рекомбинации, то под действием силы Лоренца произойдет смещение носителей зарядов к одной из боковых поверхностей. Если направление магнитного поля таково, что заряды перемещаются к поверхности У, то общая концентрация
Таблица 9-4
|
носителей зарядов уменьшается и соответственно возрастает сопротивление ГМРП. При обратном направлении вектора магнитной индукции изменяется направление силы Лоренца, что приведет к перемещению зарядов к поверхности 2, у которой малая скорость рекомбинации, и к общему увеличению концентрации зарядов, т. е. к уменьшению сопротивления ГМРП.
Таким образом, в отличие от магниторезисторов, у которых изменение сопротивления не зависит от полярности магнитной индукции, у ГМРП изменение сопротивления зависит от направления вектора магнитной индукции. При неизменном направлении магнитной индукции изменения знака приращения сопротивления можно достигнуть изменением направления тока через ГМРП. Следовательно, в магнитном поле Ш ГМРП имеет свойства, аналогичные свойствам диода.
В табл. 9-4 приведены параметры некоторых типов ГМРП, разработанных Институтом физики полупроводников АН ЛССР.
|
| -IK"® |
| Рис. 9-9 |
ГМРП обычно включается последовательно с сопротивлением нагрузки в цепь, питаемую от стабилизированного источника постоянного или переменного напряжения. При питании ГМРП переменным током (рис. 9-9, а) и воздействии постоянного магнитного поля пронсходат модуляция сопротивления ГМРП RTJ обусловливающая переход цепи в режим квадратичного детектирования, что приводит к появлению
| / | ||||
| /г | <А | |||
| / | к т. | ,=20 кОм ~+20°С~ 1 1 « | ||
| / |
| В 8 3 |
| мВ 150 100 50 |
| О 0,02 0,04 0,06 0,08 Тл |
| е) и В ВО 60 40 |
| Увых |
| В=1мГл ■Rh-20I(0M- Т=+20,°С I I I |
| / |
| О 0,5 1,0 1,5 2,0 мА |
| иВых | |||||
| N | |||||
| 1 | |||||
| В п | \=1мТл:н=20 к0> I I | ||||
| К | м | © |
| 0] -40 -20 |
| О 20 40 60 °С |
Рис. 9-10
на зажимах ГМРП постоянной составляющей, пропорциональной значению магнитной индукции.
При питании ГМРП постоянным током и воздействии переменного магнитного ноля (рис. 9-9, б) на зажимах ГМРП возникает переменная составляющая падения
напряжения. На рис. 9-10 приведены зависимости выходного напряжения от магнитной индукции (й), тока (б) и температуры {в) для ГМРП типа ГМР-1.
Как видно из табл. 9-4 и рис. 9-10, а, чувствительность к магнитной индукции ГМРП SB — Аивых/&В на 2—3 порядка больше чувствительности преобразователей Холла.
Однако порог чу ветви тельности ГМРП нз-за сильной зависимости сопротивления ГМРП от температуры, влияния шумов и выпрямляющего действия контактов такого же порядка, как у преобразователей Холла. Частотный диапазон указанных типов ГМРП составляет О—1С14 Гц. В переменных магнитных полях достигнут порог чувствительности ГМРП 5-10"'' Тл. ГМРП применяются дня измерений магнитной индукции переменных и постоянных магнитных полей, бесконтактного измерения токов, малых перемещений и других величин.
ГЛАВА ДЕСЯТАЯ
ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ
10-1. ОБЩИЕ ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ЭЛЕКТРОХИМИЧЕСКИХ ПРЕОБРАЗОВАТЕЛЕЙ
В общем случае электрохимический преобразователь состоит из заполненной электролитом ячейки и электродной системы из двух или нескольких электродов, включаемых в измерительную цепь.
Как элемент электрической цепи электролитическая ячейка может характеризоваться развиваемой ею ЭДС, падением напряжения от проходящего тока, электрическим зарядом, сопротивлением, емкостью и индуктивностью. Выделяя зависимость между одним из этих электрических параметров и измеряемой величиной и подавляя действие других факторов, можно создать электрохимические преобразователи для измерения состава и концентрации веществ, количества электричества, времени, давления, перемещения, скорости, ускорения и ряда других физических величин.
Электрические параметры ячейки зависят от природы и состава электролита и электродов, химических превращений в ячейке, температуры, скорости перемещения раствора и других величин.Связи между этими величинами и электрическими параметрами электрохимических преобразователей определяются законами электрохимии.
Диссоциация. При растворении солей, кислот и оснований в воде и в ряде других растворителей (спирт, этиленгликоль, диметилформамид и др.) происходит диссоциация — расщепление молекул на положительные ионы (катионы) и отрицательные ионы (анионы). Такие электропроводящие растворы называются электролитами или проводниками второго рода. К электролитам относятся также многие твердые вещества и расплавленные соли. Разработаны твердые электролиты (иодид серебра — рубидий, бета-глиноземы и др.)» обладающие большой проводимостью при температурах от —55 до +75 °С.
Перемещение ионов может происходить за счет диффузии, обусловленной различной концентрацией ионов в отдельных частях электро- лита, конвекции — переноса ионов вместе с потоком движущейся жидкости и миграции (электропроводности) — движения заряженных частиц под действием электрического поля.
Миграционный ток подчиняется закону Ома J = уЕу где J — плотность тока; Е — напряженность электрического поля; у — электрическая проводимость.
Зависимость проводимости электролитов от концентрации. Проводимость чистой, тщательно дистиллированной воды близка к нулю
и возрастает по мере повышения концентрации растворенных в ней веществ.
Растворы характеризуются весовой концентрацией р, измеряемой в граммах на литр, эквивалентной или молярной концентрацией с, измеряемой соответственно в грамм-эквивалентах (г-экв) или грамм-молекулах (г-моль) на литр, и химической активностью а.
Раствор с эквивалентной концентрацией 1 г-экв растворенного вещества на 1 л раствора называется нормальным (н) раствором.
Химическая активность а равна произведению эквивалентной концентрации с на коэффициент активности f, равный единице для растворов бесконечного разбавления и уменьшающийся по мере повышения концентрации, так как химическая активность растворенного вещества падает с ростом концентрации из-за уменьшения степени диссоциации и подвижности ионов.
Удельная проводимость раствора пропорциональна его химической активности:
y = %fc==%a, (10-1)
Коэффициент X называется эквивалентной электропроводимостью*
Удельная проводимость зависит от концентрации нелинейно (рис. 10-1).
Зависимость проводимости электролитов от значения химической активности а, не имеющего в общем случае однозначной связи с концентрацией, позволяет создавать измерительные преобразователи для контроля параметров реальных химико-технологических процессов, так как они наиболее точно характеризуются именно значением химической активности а.
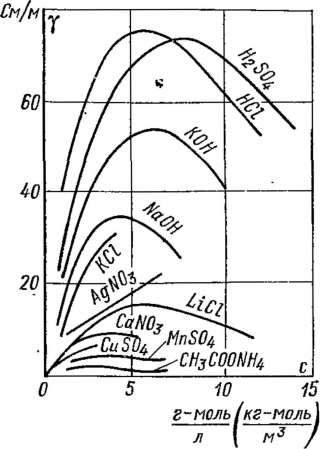 Рис. 10-1
Рис. 10-1
|
Зависимость проводимости электролитов от температуры. Подвижность ионов сильно зависит от температуры раствора, и поэтому с увеличением температуры проводимость возрастает. Температурная зависимость проводимости водных растворов при небольших концентра-
днях (до 0,05н) можно определить как
Те = Ye [ 1 + (в — вв) р],, (10-2)
где Р—температурный коэффициент проводимости.
Примерные значения р равны: 0,016 К"1 для кислот, 0,019 К"1 для оснований и 0,024 К"1 для солей.
Электродные и граничные потенциалы. Между двумя электродами, опущенными в электролит, возникает разность потенциалов, т. е. электролитическая ячейка является источником гальванической ЭДС. Возникновение ЭДС между металлом электрода и раствором при малой его концентрации объясняется тем, что металл частично растворяется, т. е. в раствор переходят положительно заряженные ионы металла, и раствор заряжается положительно, а на электроде остаются избыточные электроны и он заряжается отрицательно относительно раствора. При больших концентрациях раствора, наоборот, положительные ионы могут выделяться на электроде, заряжая его положительно относительно раствора. Потенциал электрода относительно раствора, в который он опущен, называется электродным потенциалом. Практически могут быть измерены не абсолютные значения электродных потенциалов отдельных электродов, а лишь разности потенциалов различных пар электродов. В электрохимии за начало отсчета (условный нуль) принят потенциал «водородного электрода» относительно раствора с нормальной активностью {а — 1 г-экв/л) водородных ионов. Изготовить электрод из газообразного водорода не представляется возможным, поэтому практически водородный электрод выполняется в виде пластинки из губчатой платины, которая частично погружается в раствор, содержащий ионы водорода Н+. Через раствор непрерывно пропускается газообразный водород (рис. 10-2), и на электроде / происходит реакция
Н2 = 2Н+ + 2е.
Платина электрода в реакции не участвует и является лишь проводником электронов и носителем водорода, который хорошо адсорбируется на поверхности платины.
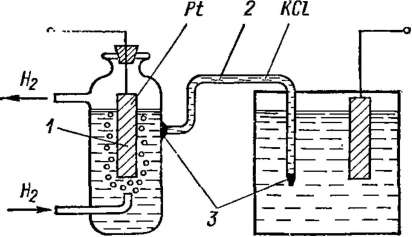 Рис. 10-2
Рис. 10-2
|
Значения электродных потенциалов различных веществ, отсчитанные относительно водородного электрода, лежат в пределах ±3 В. Так, электродный потенциал калия равен Е0 = —2,92 В, цинка £0 = —0,76 В, меди Еь === +0,34 В и т. д. Приведенные значения потенциалов Eq называются нормальными потенциалами электрода, так как они измерены при нормальной температуре (18° С) и нормальной концентрации электролита. При других температурах и концентрациях зависимость между электродным потенциалом в вольтах и кон
центрацией раствора определяется уравнением Нернста
E^Eo+^plnfc, (10-3)
где R = 8,317 Дж/К — универсальная газовая постоянная; Т — абсолютная температура, К; п — валентность ионов; F — = 96 552 Кл/г-экв — постоянная Фарадея; с — концентрация ионов, г-экв/л; / — коэффициент активности раствора. Переходя к десятичным логарифмам и заменяя R и F их численными значениями, получаем выражение для электродного потенциала при температуре 18 °С
E = E0+^\gfc. (10-4)
В общем случае электролитическая ячейка может быть составлена из разных электродов, помещенных в разные растворы, как это показано на рис. 10-2. Каждая половина такого гальванического элемента называется полуэлементом. ЭДС между двумя полуэлементами, содержащими растворы разных эквивалентных концентраций, равна
Егг = Е01 + In/id - £02 - ~ In ксг = Е01 - Еп + (10-5)
Таким образом, разность потенциалов, развиваемая двумя полуэлементами, определяется не только материалом электродов, но и отношением активностей f\Cxl(f^ растворов,
Если же используемые электроды одинаковы и погружены в растворы тех же ионов, отличающиеся только концентрацией, то концентрационная ЭДС такой цепи будет
(10-6)
Разность потенциалов возникает также на границе двух растворов. Граничная ЭДС может возникнуть в результате разной подвижности ионов в.растворах и, следовательно, разной скорости диффузии. В зависимости от вида и концентрации соприкасающихся растворов эта, так называемая диффузионная, ЭДС составляет от нескольких единиц до десятков милливольт. Для ее уменьшения между растворами включают промежуточный концентрированный раствор с возможно близкими подвижностями катионов и анионов, например КС1 или KNOa (электролитический ключ). На рис. 10-2 показано соединение двух полуэлемеитов в гальваническую цепь при помощи электролитического ключа 2. Концы электролитического ключа закрываются. полунепроницаемыми пробками 3.
Граничная ЭДС возникает также на границе двух растворов, разделенных полупроницаемой перегородкой (мембраной), которая пропускает одни ионы и задерживает другие (например, из-за слишком больших их размеров по сравнению с диаметром пор). Мембранные ЭДС представляют большой интерес для медицинских и биологических исследований, так как они имеют место в животных и растительных тканях.
Электролиз, поляризация и потенциалы выделения. Прохождение электрического тока через электролиты сопровождается электролизом— химическими превращениями и выделением вещества из раствора. Для электрохимического превращения 1 г-экв любого вещества необходимо одно и то же количество электричества, равное произведению числа Авогадро N на заряд электрона и называемое постоянной Фара- дея F = Ne = 96 552 Кл/г-экв.
Таким образом, прохождение через электролит любого сколь угодно малого количества электричества всегда сопровождается выделением на одном электроде и растворением на другом соответствующего, совершенно определенного количества вещества. В результате этого концентрация ионов вблизи электродов оказывается не такой, как в остальном растворе.
Деление поляризации заключается в изменении электродных потенциалов вследствие изменения приэлектродной концентрации при протекании через электролитическую ячейку электрического тока от внешнего источника. Вследствие этого внешнее напряжение, приложенное к электролитической ячейке, должно уравновешивать не только падение напряжения на столбе электролита, но еще и сумму потенциалов поляризации электродов.
Зависимость суммарного напряжения поляризации Д£/ от изменения плотности тока на электродах различна для разных сочетаний растворов и электродов. Общий характер этих зависимостей заключается в том, что напряжение поляризации AU быстро возрастает при очень малых плотностях тока, а затем остается почти постоянным, слабо изменяясь с дальнейшим ростом плотности тока. Поэтому в первом приближении при достаточно большой плотности тока значение AU можно считать не зависящим от плотности тока, а только от сочетания материалов электрода и электролита.
Вследствие конечной скорости диффузии при данной концентрации электролита к катоду в единицу времени может подходить только конечное число носителей заряда — ионов вещества. Поэтому, если пытаться беспредельно увеличивать электрический ток через ячейку, то при каком-то токе будут использованы все ионы, приносимые к катоду диффузией, и дальнейший рост тока прекратится. Предельный ток диффузии можно определить из приближенного выражения
Лф — nFDSco/8, (1U-7)
где D — коэффициент диффузии; с0 — концентрация реагирующих ионов в толще электролита; 5 — площадь электрода; б —.толщина диффузионного слоя.
Потенциал, при котором в процесс электролиза вступает основная масса ионов данного вида, называется потенциалом выделения данного иона. Если в растворе содержатся разные виды ионов, то зависимость / = f (£/) имеет форму ступенчатой кривой. Потенциал выделения, при котором начинается очередной рост тока, зависит от вида йона, а высота ступеней тока пропорциональна концентрации этих ионов. На использовании этого явления основан полярографический метод качественного и количественного анализа растворов (см. § 10-5).
Проводимость электролитов для переменного тока. Явление поляризации затрудняет измерение сопротивления электролитов, так как падение напряжения на электролитической ячейке складывается из падения напряжения на столбе электролита и потенциалов поляризации электродов, которые могут достигать 1,5—2 В. При измерении сопротивления электролита постоянному току явление поляризации может обусловить значительную погрешность, поэтому такие измерения обычно производят на переменном токе.
При прохождении через ячейку переменного синусоидального тока изменение концентрации ионов в приэлектродном слое относительно средней концентрации будет происходить также по синусоидальному закону. Однако в течение всего положительного полупериода электрод (являющийся в это время анодом) будет непрерывно отдавать в раствор катионы и их концентрация у электрода будет повышаться. Максимум концентрации, а следовательно, и максимум напряжения поляризации будут достигнуты только в конце полупериода, т. е. тогда, когда ток упадет до нуля.
| R |
| С1 с2 |
В течение отрицательного полупериода электрод, являясь катодом, наоборот, будет непрерывно забирать катионы из раствора, их концентрациями напряжение поляризации будут непрерывно понижаться и достигнут миниму- б) % ма только в конце полупе-
Ч'г
риода, когда ток вновь будет проходить через нуль.
Таким образом, отличие явления поляризации при р 10 3 переменном токе заключает-
IlC JV ° ся в том, что напряжение
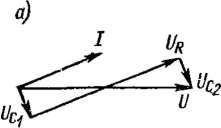
поляризации в этом случае является также переменным и отстает по фазе от тока на 90°. Падение напряжения на столбе электролита по фазе совпадает с током. Исходя из этого, векторную диаграмму падений напряжений в электролитической ячейке можно изобразить так, как показано на рис. 10-3, где UR — вектор падения напряжения на столбе электролита, a Uct и Uc2 — напряжения, уравновешивающие ЭДС поляризации электродов. Согласно этой диаграмме электролитическая ячейка (при данном значении тока /) может быть заменена эквивалентной схемой, показанной на рис. 10-3, б и состоящей из сопротивления R столба электролита и емкостей Сх и С2. При использовании этой схемы необходимо всегда иметь в виду, что емкостям С± и С2 не может быть приписано какого-либо постоянного значения. Действительно, реально существующим параметром ячейки является напряжение АV поляризации электродов, которое не пропорционально протекающему току /, а, скорее, не зависит от него. В широком диапазоне изменения токов напряжение AU примерно остается постоянным и равным 0,1—1,5 В в зависимости от сочетания материалов электродов и электролита. Емкость в эквивалентной схеме определяется из соотношения
Ш = 1ХС = Jc ^ const = 0,1 -ь 1,5 В
и -равна
г- 1
^ -(0,1 4-1,5) со-
Каждому значению тока и частоты соответствует свое значение емкости С. Вследствие малого падения напряжения AU при значительных токах емкость С достигает больших значений (до 0,1—0,5 Ф на 1 м2 поверхности электродов).
Кроме емкостей С, и С2, иногда необходимо учитывать и емкость С3, обусловленную размерами электролитической ячейки как конденсатора и диэлектрической постоянной раствора. Значения С3 обычно лежат в пределах 10"10—10"12 Ф.
Преимущество измерения сопротивления электролитической ячейки переменному току заключается в том, что благодаря 90-градусному углу сдвига между падением напряжения на столбе электролита и напряжением поляризации эти напряжения суммируются не арифметически (как при постоянном токе), а геометрически. При AU ^ U погрешность равна
, 1 шла
и может быть в значительной степени устранена при применении фазо- чувствительных указателей, в то время как при измерении на постоянном токе она составляет 6 — Д U/U.
Электрокинетические явления. Как было показано выше, на границе твердого тела и электролита происходит скачок потенциала. Заряженный слой жидкости имеет диффузное строение, при котором плотность зарядов быстро убывает с их удалением от поверхности твердого тела. Скачок потенциала в диффузионном слое жидкости называется электрокинетическим потенциалом. В случае если твердое тело является диэлектриком, образование электрокинетического потенциала обусловлено неодинаковой адсорбцией ионов обоих знаков.
Если на концах капилляра или пористой перегородки поместить электроды и создать электрическое поле, то возникнет движение жидкости в капилляре. Это явление называется электроосмосом. Скорость течения жидкости в результате электроосмоса определяется выражением
v^Q/S^tEE/Wnii), (10-8)
где Е — напряженность электрического поля в капилляре, В/м; 5 — сечение капилляра (или сумма сечений пор), м2; е — диэлектрическая постоянная жидкости, Ф/м; \х — динамическая вязкость жидкости, Па-с; £—электрокинетический потенциал, В; Q — расход жидкости, м3/с.
Date: 2015-09-18; view: 597; Нарушение авторских прав