
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Визначення сухого залишку
|
|
Визначення сульфатного іону.
Іони SO42- попадають у воду головним чином внаслідок розчинення осадових порід, що містять гіпс. Іноди іони SO42- утворюються при окисленні сульфідів та самородної сірки, а також внаслідок забруднення води промисловими та іншими стоками. Якщо вода містить від 2,5 до 70 мг/л SO42-, то визначення його проводять турбодиметричним методом Бутиріна. При цьому вода має бути цілком прозора. Непрозорі води потрібно профільтрувати. Визначення засновано на вимірюванні інтенсивності замутнення води у мутномірній пробірці при утворенні осаду BaSO4.
Необхідні хімічні реактиви та обладнання:
дистильована вода;
розчин соляної кислоти (розведення 1:1);
10% розчину хлориду барію BaCl2;
мішалка;
піпетка;
мутномірна пробірка.
Х і д а н а л і з у. У мутномірну пробірку наливають 10 мл досліджуваної води, додають дві краплі розчину соляної кислоти (розведення 1:1) та 1мл 10% розчину хлориду барію BaCl2. Суміш перемішують мішалкою. Через 10 хвилин суміш знов перемішують та розглядають чорний хрест та крапки на денці пробірки. Якщо їх не видно, то рідину відбирають потроху піпеткою, доки не з‘явиться зображення крапок та хреста. Вимірюють висоту стовпа рідини у мутномірній пробірці та за таблицею знаходять кількість іону SO42-. Визначення роблять тричі. Якщо висота рідини у пробірці меньше 33 мм, визначення роблять спочатку, відміряючи менше досліджуваної води та додаючи дистильовану до об‘єму 10мл. При розрахунку вмісту SO42- у воді розведення враховують.
Таблиця визначення сульфат-іону.
| Висота стовпа рідини, мм | Вміст SO42- | Висота стовпа рідини, мм | Вміст SO42- | ||
| мг/л | мг-екв/л | мг/л | мг-екв/л | ||
| 0,52 | 1,04 | ||||
| 0,56 | 1,15 | ||||
| 0,62 | 1,25 | ||||
| 0,74 | 1,35 | ||||
| 0,83 | 1,46 | ||||
| 0,94 | 1,56 |
Визначення сухого залишку
Сухим залишком називають вагу нелетких речовин, що залишились після випаровування та висушування води. Величина сухого залишку характеризує мінералізацію води та дозволяє контролювати точність зробленого хімічного аналізу. Головними джерелами помилок при визначенні сухого залишку можуть бути:
1) утворення кристалогідратів солей. Речовини, що мають у своєму складі іон SO42-, при випаровуванні води утворюють кристалогідрати, (наприклад CaSO4 . 2H2O), що не віддають кристалізаційну воду навіть при високій температурі;
2) гідроліз солей. Хлориди кальцію та магнію, що містяться майже у кожній природній воді, при нагріванні гідролізують, утворюючи основні солі:
2MgCl2 + H2O ↔ Mg2OCl2 + 2 HCl
3) гігроскопічність солей. Деякі солі (головним чином хлориди) сильно поглинають вологу повітря, тим самим викривляючи вагу сухого залишку.
Для запобігання усіх цих помилок пробу досліджуваної води нагрівають, додаючи тверду соду (Na2CO3). При цьому хлориди, сульфати та інші солі кальцію та магнію переходять у безводні, негідролізуючі та негігроскопічні карбонати кальцію та магнію.
MgCl2 + Na2CO3 → MgCO3 + 2NaCl
Необхідні хімічні реактиви та обладнання:
аналітичні ваги;
порцеляновий тигель;
сода (Na2CO3);
сушильна шафа;
ексікатор.
Х і д а н а л і з у. Висушують порцеляновий тигель до постійної ваги. В нього вносять безводну соду (Na2CO3) в кількості, що у 2-3 рази перекриває передбачуваний вміст розчинних солей (останні можуть бути орієнтовно підраховані виходячи з аналізу вже визначених катіонів та аніонів). Тигель з содою зважують на аналітичних вагах, наливають певний об‘єм досліджуваної води та випаровують досуха на водяній бані. Залишок висушують у сушильний шафі при температурі 150-180 оС на протязі 2-3 годин. Після охолодження в ексікаторі тигель знову зважують.
Вміст сухого залишку (у г/л) вираховують за формулою:
С.з. = 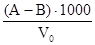
де А - вага тигля з сухим залишком, г;
В - вага тигля з содою, г;
V0 – об‘єм досліджуваної води, мл.
Date: 2015-07-27; view: 722; Нарушение авторских прав