
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Електрометричний метод визначення pH
|
|
Електричний метод визначення pH заснований на використанні приладу (pH-метр), який має два електроди (один скляний, чутливий до вмісту іонів водню, другий - електрод порівняння, що утворює з першим електродну пару). Електрорушійна сила (е.р.с.) концентраційного електричного кола відображається на шкалі приладу у одиницях pH з точністю до 0,02 pH. Електричний метод дозволяє визначити реакцію середовища дуже точно та в будь-яких водах (каламутних, забарвлених інш).
Необхідні хімічні реактиви та обладнання:
прилад-pH-метр;
дистильована вода;
фільтрувальний папір
Х і д а н а л і з у. Досліджувану воду наливають у чисту та суху скляночку. Промивають електроди дистильованою водою з промивалки та обсушують їх фільтрувальним папером, не торкаючись електродів пальцями. Занурюють електроди у досліджувану воду.
Коли стрілка на шкалі приладу зупиниться, проводять відлік приблизного pH по нижній шкалі приладу. Далі ручку перемикача границь вимірювання встановлюють так, щоб приблизне значення pH входило в цей інтервал. Після зупинки стрілки записують точне значення pH розчину, користуючись верхньою шкалою приладу.
Визначення агресивної вуглекислоти.
Під терміном "агресивна вуглекислота" розуміють ту частину розчиненого у воді вуглецевого газу (CO2 агр.), що може розчиняти твердий CaCO3 по реакції
CaCO3 (тв.) + H2O + CO2 агр. ↔ Ca2+ + 2НCO3-.
Ця реакція може йти у обох напрямках в залежності від співвідношення концентрацій CO2 та НCO3-. Кількісно агресивну вуглекислоту визначають із спеціальної проби води, яка відбирається одночасно з пробою на загальній аналіз.
Необхідні хімічні реактиви та обладнання:
хімічно чистий карбонат кальцію (CaCO3)
індикатор метиловий оранжевий
5 % розчин соляної кислоти
конічнна колба місткістю 200 мл
Х і д а н а л і з у. У чисту суху пляшку ємністю 250мл набирають воду по вінця, додають 2г хімічно чистого карбонату кальцію (CaCO3), пляшку закорковують й залишають на декілька днів, періодично збовтуючи. Через кілька днів воду з пляшки фільтрують у суху колбу, з якої піпеткою відбирають 50 мл фільтрату у конічну колбу місткістю 200 мл, додають дві краплі індикатору метилового оранжевого та тітрують розчином соляної кислоти до персикового забарвлення.
Одночасно визначають вміст у воді іону HCO3- (без CaCO3). Кількість агресивної вуглекислоти у мг/л вираховують за формулою:
 [СО2] агр =
[СО2] агр = 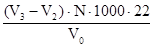 ,
,
де V3 – об‘єм соляної кислоти витраченої на тітрування фільтрату,мл;
V2 - об‘єм соляної кислоти, який витрачено на тітрування іону HCO3- у воді, мл
V0 - об‘єм води, що взяли на тітрування, мл;
N - нормальність розчину соляної кислоти;
22 - еквівалентна вага CО2.
Date: 2015-07-27; view: 824; Нарушение авторских прав