
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Кинетические основы газовых реакций
|
|
Закон действующих масс: скорость реакции при постоянной температуре пропорциональна концентрации реагирующих веществ («действующих масс»).
Скорость химической реакции (υ) - количество вещества, реагирующего в единицу времени (dt) в единице объема (dV).
Рассмотрим реакцию, протекающую по уравнению:
А + В = С + Д.
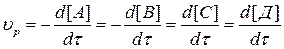 , (3.1)
, (3.1)
Т = const:
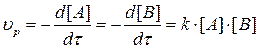 , (3.2)
, (3.2)
где: k – константа скорости химической реакции.
аА + bB = cC + dД
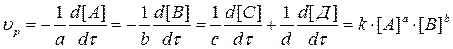 … (3.3)
… (3.3)
a, b, c, d - порядки реакции по компонентам А, В, С, Д, сумма показателей – общий порядок реакции.
А ® bB + cC – I порядка,
2А = bB + cC – II порядка,
А + B = cC + dД – III порядка.
Кинетическое уравнение I порядка типа
А=bB+cC…,
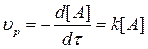 . (3.4)
. (3.4)
[A0] - концентрацию компонента А до начала реакции:
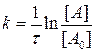 , или [A]=[A0]×e-kt. (3.5)
, или [A]=[A0]×e-kt. (3.5)
Скорость химической реакции зависит не от количества столкновений всех молекул, а только активированных.
По закону Больцмана, число активных молекул
nA = nо * e-E/RT, (3.6)
где: Е – энергия активации,
Т – температура газовой смеси,
nо – общее число молекул.
Тогда и число эффективных соударений, совпадающее со скоростью реакции, равно:
υр = Zэфф = Z0 * e-E/RT, (3.7)
где: Z0 – общее число соударений молекул.
1) скорость реакции пропорциональна концентрации активных молекул, число которых зависит от температуры и давления в смеси, так как давление и есть количество молекул, сталкивающихся с какой-либо поверхностью;
2) реакция возможна лишь в том случае, если взаимодействующие молекулы получают определенный запас энергии, достаточный для разрыва или ослабления межатомных связей. Активация заключается в переходе молекул в такое состояние, в котором возможно химическое превращение.
Минимальное количество тепловой энергии, необходимое для «запуска» химической реакции, называется энергией активации.
Date: 2015-07-24; view: 827; Нарушение авторских прав