
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Тепловой эффект реакции
|
|
Закон Гесса: Тепловой эффект химической реакции зависит только от природы начальных и конечных продуктов и не зависит от числа промежуточных реакций перехода от одного состояния к другому.
Следствие 1 этого закона: Тепловой эффект химической реакции равен разности между суммой теплот образования конечных продуктов и суммой теплот образования исходных веществ с учетом коэффициентов при формулах этих веществ в уравнении реакции.
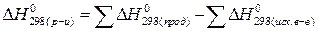 .
.
Например, в реакции 2Н2+О2=2Н2О±DН.
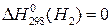 ;
; 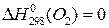 ;
; 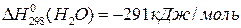 .
.
Тогда:
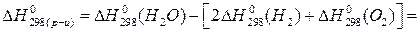
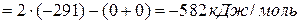 .
.
В итоге общее уравнение реакции будет выглядеть так:
2Н2+О2=2Н2О – 582 кДж/моль.
И если DН со знаком (-), то реакция экзотермическая.
Следствие 2. По закону Лавуазье-Лапласа тепловой эффект разложения химического соединения равен и противоположен по знаку тепловому эффекту его образования.
Тогда реакция разложения воды будет:
2Н2О=2Н2+О2+582 кДж/моль, т.е. эта реакция эндотермическая.
Пример более сложной реакции:
СН4+2О2=СО2+2Н2О.
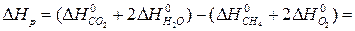
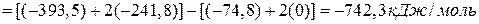 .
.
Тогда реакция запишется так:
СН4 + 2О2 = СО2 + 2Н2О – 742,3 кДж/моль, значит реакция экзотермическая.
Материальный баланс горения – это расчеты количеств вещества принимающих участие в процессе горения на основании закона сохранения масс.
Мг+Мок=Мпс
Горючее составляющее топливо вступает в определенных количественных отношениях называемых стехиометрическими.
V020 =1,866Ср/100+0,7Sр/100+5,55Hр/100-Qр/100ρO2 [м3/кг]
Ср,Нр,Ор,Sр,– массовое содержание С,Н,О,S, в топливе [%];ρO2 [кг/ м3]
В воздухе содержится 21% O2
V0 =V020/0,21=0,0889(Ср+0,375Sр)*0,265Hр-0,0333Ор
L0 =0,115(Ср+0,375Sр)+0,342Hр-0,0431Ор [кг/кг]
V0 - теоретически необходимый объем воздуха для полного сгорания воздуха;
L0 - теоретически необходимый объем воздуха до полного сгорания одного кг топлива.
Коэффициент избытка воздуха – это отношение кол-ва воздуха действительно поступившего в топку, к теоретически необходимому: α = Vg/V0
Date: 2015-07-24; view: 696; Нарушение авторских прав