
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Свойства газов
|
|
Основное уравнение кинетической теории газов имеет вид:
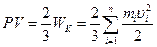 , (2.1)
, (2.1)
где: WK – суммарная кинетическая энергия поступательного движеия n молекул газа, находящегося в объеме V;
mi, ui – масса и скорость движения i-той молекулы.
Теплопроводность – процесс самопроизвольного выравнивания температур, возникающий в веществе при наличии градиента температур:
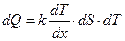 , (2.2)
, (2.2)
где: dQ – количество теплоты переносимой за время dT через поверхность dS по направлению нормали Х к этой поверхности в сторону убывания температуры;
(dT/dх) – градиент температуры;
k – коэффициент теплопроводности, равный количеству теплоты, перенесенный через единицу поверхности за единицу времени при градиенте dT/dх =1.
Согласно кинетической теории газов:
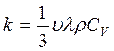 , Дж/(см×сек×град) (2.3)
, Дж/(см×сек×град) (2.3)
где: υ – средняя скорость теплового движения молекул;
l - средняя длина свободного пробега молекул;
r - плотность газа;
CV – удельная теплоемкость газа при постоянном объеме.
Диффузия – процесс установления внутри фаз какой-то системы равномерного распределения концентрации газа.
Фаза – совокупность всех гомогенных частей системы.
В двухкомпонентной системе явление диффузии описывается законом Фика:
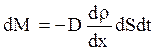 , (2.4)
, (2.4)
где: dM – масса первого компонента, которая переносится за время dt через площадь dS в направлении нормали Х к этой площадке в сторону убывания плотности первого компонента;
dr/dx – градиент плотности;
D – коэффициент диффузии.
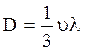 , см2/сек. (2.5)
, см2/сек. (2.5)
Теплоемкость – количество тепла, необходимое для повышения температуры вещества на один градус:
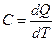 , Дж/К (2.6)
, Дж/К (2.6)
Газовые законы:
1. Закон Авогадро: Равные объемы газов при одинаковых температуре и давлении содержат одинаковое число молекул.
2. Закон Гей-Люссака: при P=const объем массы газа прямо пропорционален его абсолютной температуре:
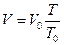 , (2.8)
, (2.8)
где: Т0=273 К;
V0 – объем газа при Т0.
3. Закон Шарля: при V=const давление данной массы газа прямо пропорционально его абсолютной температуре:
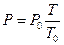 , (2.9)
, (2.9)
где: P0 – давление при Т0=273 К.
4. Уравнение состояния идеального газа для 1 моля газа:
 , (2.10)
, (2.10)
где: P, Vμ и T – давление, молекулярный объем и абсолютная температура газа.
5.Уравнение Менделеева-Клайперона для произвольной массы газа (М):
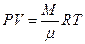 , (2.11)
, (2.11)
Date: 2015-07-24; view: 603; Нарушение авторских прав