
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

А) Синтетические средства
|
|
Эта группа резервных противотуберкулезных средств представлена соединениями различного химического строения. К ним относятся ПАСК и тиоацетазон (см. структуры веществ). Каждое из этих веществ применяют в комбинации с другими препаратами.
Натрия пара-аминосалицилат (ПАСК) оказывает бактериостатическое действие на микобактерии туберкулеза. Механизм его действия обусловлен конкурентными взаимоотношениями с пара-аминобензойной кислотой, необходимой для роста и размножения микобактерии туберкулеза. На другие микроорганизмы он не влияет.
Активность натрия пара-аминосалицилата невысокая. В связи с этим применяют его только в комбинации с другими, более активными препаратами. Как уже отмечалось, устойчивость к ПАСК развивается медленно.
Натрия пара-аминосалицилат хорошо всасывается из пищеварительного тракта. Максимальная концентрация в плазме крови определяется через 1-2 ч. Значительная часть препарата (около 50%) связывается с белками плазмы крови. В серозных полостях накапливается в достаточных количествах. Через гематоэнцефалический барьер проникает в небольшой степени. Через 6 ч в плазме крови обнаруживается в незначительной концентрации. Из организма выводится почками в неизмененном виде, а также в виде метаболитов и конъюгатов (в основном ацетилированное производное пара-аминосалициловой кислоты). За 6 ч выделяется около 60%, а за 24 ч — примерно 90% от введенной дозы.
Применяют при всех формах туберкулеза. Назначают обычно внутрь, иногда прибегают к внутривенному введению.
Из побочных эффектов наиболее часты диспепсические расстройства, связанные с раздражающим действием препарата. При этом наблюдаются тошнота, рвота, диарея, боли в области живота, нарушается аппетит. Редко возникают агранулоцитоз, гепатит, кристаллурия. У ряда больных отмечается развитие зоба с явлениями гипотиреоза. Возможны осложнения аллергического происхождения, которые проявляются кожными реакциями, лихорадкой, артритами, эозинофилией и др.
Спектр противомикробного действия тиоацетазона (тибон, контебен) ограничивается микобактериями туберкулеза и возбудителем проказы. По противотуберкулезной активности тиоацетазон уступает препаратам I и II групп. Устойчивость микобактерии туберкулеза к тиоацетазону развивается относительно медленно.
Препарат хорошо всасывается из желудочно-кишечного тракта. Частично инактивируется в печени. Выделяется из организма в течение 1 -х суток. Большая часть препарата выводится почками.
Применяют тиоацетазон внутрь, главным образом при внелегочных формах туберкулеза (при туберкулезе слизистых и серозных оболочек, лимфатических узлов и др.). В ряде случаев тиоацетазон назначают при проказе.
Тиоацетазон обладает значительной токсичностью. Он относительно часто вызывает тяжелые осложнения со стороны кроветворения (анемию, лейкопению, агранулоцитоз), почек (альбуминурию, цилиндрурию) и печени (вплоть до желтой атрофии печени). Кроме того, при его использовании отмечаются диспепсические расстройства, аллергические реакции и другие побочные эффекты.
Применение тиоацетазона требует постоянного контроля состояния кроветворения, функций печени и почек.
| Препараты | ||
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Изониазид — Isoniazidum | Внутрь 0,3 г; внутривенно капельно 0,01—0,015 г/кг (в виде 0,2% раствора) | Порошок; таблетки по 0,1; 0,2 и 0,3 г; 10% раствор в ампулах по 5 мл |
| Рифампицин — Rifampicinum | Внутрь 0,45 г; внутривенно по 0,3-0,9 г | Капсулы по 0,05 и 0,15 г; ампулы по 0,15 г (растворяют перед употреблением) |
| Этамбутол — Ethambutolum | Внутрь 0,025 г/кг | Таблетки по 0,1; 0,2 и 0,4 г |
| Этионамид — Ethionamide | Внутрь 0,25 г | Таблетки, покрытые оболочкой, по 0,25 г |
| Протионамид — Protionamide | Внутрь 0,25 г | Таблетки (драже) по 0,25 г |
| Пиразинамид — Piraznamide | Внутрь 1 г | Таблетки по 0,5 и 0,75 г |
| Циклосерин — Cycloserinum | Внутрь 0,25 г | Таблетки и капсулы по 0,25 г |
| Канамицина сульфат — Kanamycini sulfas | Внутримышечно 1 г; ингалляционно 0,25—0,5 г в 3—5 мл изотонического раствора натрия хлорида или дистиллированной воды | Флаконы по 0,5 и 1 г (растворяют перед употреблением); 5% раствор в ампулах по 5 и 10 мл |
| Флоримицина сульфат — Florimycini sulfas | Внутримышечно 0,5—1 г | Флаконы по 0,5 и 1 г |
| Натрия парааминосалицилат — Natrii paraaminosalicylas | Внутрь 3—4 г; внутривенно капельно 250 мл 3% раствора | Порошок; таблетки по 0,5 г; таблетки, растворимые в кишечнике, по 0,5 г; гранулы (2 г препарата в 6 г гранул); флаконы по 250 и 500 мл 3% раствора |
| Тиоацетазон — Thioacetazonum | Внутрь 0,05 г | Таблетки по 0,025 и 0,05 г |
Глава 30 ПРОТИВОВИРУСНЫЕ СРЕДСТВА
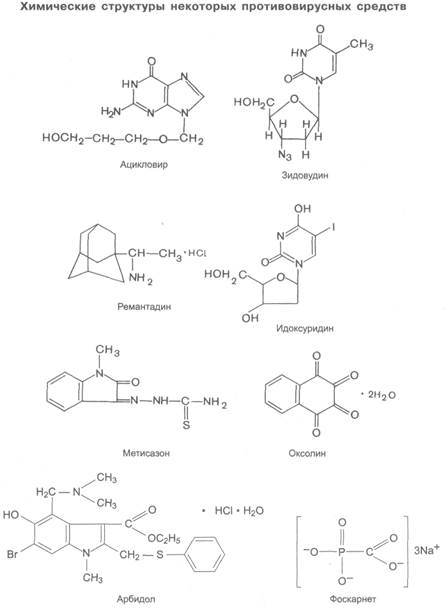
Создание противовирусных средств — одна из наиболее сложных задач химиотерапии инфекций. Связано это с тем, что РНК- и ДНК-содержащие вирусы являются облигатными внутриклеточными паразитами. В процессе размножения вирусы в основном используют аппарат биосинтеза клеток макроорганизма, определенным образом модифицируя его. В связи с этим крайне трудно находить избирательно действующие средства, которые поражали бы вирусы, не повреждая клетки «хозяина». Однако некоторые вирусы (например, вирус простого герпеса, вирус опоясывающего лишая и др.) после проникновения в клетки индуцируют образование своих ферментов, которые могут отличаться от аналогичных ферментов самой клетки. К числу таких ферментов относится, например, ДНК-полимераза. Так, ациклогуанозин (ацикловир), проникая в клетку, фосфорилируется и в виде трифосфата угнетает ДНК-полимеразу вируса простого герпеса (в большей степени, чем ДНК-полимеразу клетки). Кроме того, это соединение встраивается в ДНК вируса. Рибавирин в виде 5-трифосфата специфически угнетает вирусную РНК-полимеразу. Показано, что азидотимидин ингибирует обратную транскриптазу вирионов ВИЧ-инфекции. Препараты пептидной структуры (саквинавир) избирательно ингибируют протеазы ВИЧ. Открыты противогриппозные средства, ингибирующие вирусный фермент нейраминидазу. Полученные данные весьма перспективны для создания новых избирательно действующих противовирусных средств.
Направленность действия противовирусных средств может быть различной и касается разных стадий взаимодействия вируса с клеткой. Так, известны вещества, которые угнетают:
1) адсорбцию вируса на клетке и(или) проникновение его в клетку (γ-глобулин);
2) процесс высвобождения («депротеинизации») вирусного генома (мидантан, ремантадин);
3) синтез «ранних» вирусных белков-ферментов (гуанидин);
4) синтез нуклеиновых кислот (зидовудин, ацикловир, видарабин, идоксуридин и другие аналоги нуклеозидов);
5) синтез «поздних» вирусных белков (саквинавир);
6) «сборку» вирионов (метисазон).
Кроме того, попадая в организм, вирусы вызывают образование клетками биологически активного гликопротеина интерферона и включение гуморального и клеточного звеньев иммунитета. Вирусные белки, являясь сильными антигенами, вызывают образование антител, нейтрализующих действие вирусов. Создание лекарственных средств, стимулирующих биосинтез интерферона и антителообразование, также перспективно в борьбе с вирусными инфекциями.
Противовирусные вещества, которые применяют в качестве лекарственных средств, могут быть представлены следующими группами (подробнее см. в табл. 30.1).
Синтетические средства
Аналоги нуклеозидов — зидовудин, ацикловир, видарабин, ганцикловир, трифлуридин, идоксуридин
Производные пептидов — саквинавир
Производные адамантана — мидантан, ремантадин
Производное индолкарбоновой кислоты — арбидол
Производное фосфономуравьиной кислоты — фоскарнет
Производное тиосемикарбазона — метисазон
Биологические вещества, продуцируемые клетками макроорганизма
Интерфероны
Большая группа эффективных противовирусных средств представлена производными пуриновых и пиримидиновых нуклеозидов. Они являются антиметаболитами, ингибирующими синтез нуклеиновых кислот (см. табл. 30.1).
В последние годы особенно большое внимание привлекли противоретровирусные препараты, к которым относятся ингибиторы обратной транскриптазы и ингибиторы протеаз. Повышенный интерес к этой группе веществ связан с их применением при лечении синдрома приобретенного иммунодефицита (СПИД). Вызывается он специальным ретровирусом — вирусом иммунодефицита человека (ВИЧ; HIV). Терапия СПИДа требует применения противоретровирусных, а также симптоматических средств.
| Таблица 30.1. Показания к применению ряда противовирусных препаратов | ||
| Семейство вирусов | Вирусы/заболевания | Препарат |
| ДНК-содержащие вирусы | ||
| Герпесвирусы | Вирус простого герпеса Герпес кожи, слизистых оболочек, половых органов, герпетический энцефалит Герпетический кератит | Ацикловир, валацикловир, фоскарнет, видарабин Трифлуридин, идоксуридин |
| Цитомегаловирусы Ретинит, колит, пневмония и др.1 | Ганцикловир, фоскарнет, витравен | |
| Вирус varicella zoster Опоясывающий лишай, ветряная оспа | Ацикловир, фоскарнет | |
| Поксвирусы | Вирус натуральной оспы Оспа | Метисазон |
| Гепаднавирусы | Вирусы гепатита В и С Хронический активный гепатит | Интерферон-α-2b |
| РНК-содержащие вирусы | ||
| Ретровирусы | Вирус иммунодефицита человека (ВИЧ; HIV) ВИЧ-инфекция (включая СПИД) | Зидовудин, диданозин, зальцитабин, ставудин, саквинавир, ритонавир, индинавир, нельфинавир, невирапин, делавирдин |
| Ортомиксовирусы | Вирусы гриппа Грипп: а) вирус гриппа типа А б) вирус гриппа типа А и В | Ремантадин, мидантан (амантадин) Арбидол, занамивир, осельтамивир, рибавирин |
| Парамиксовирусы | Респираторно-синцитиалъный вирус Бронхиолит, пневмония | Рибавирин |
| 1 Клиническая картина цитомегаловирусной инфекции весьма разнообразна. Цитомегаловирусы являются частой причиной внутриутробной и перинатальной инфекции, иногда с тяжелым исходом. Активация этих вирусов отмечается при иммунодепрессии, связанной с применением цитостатиков, а также при ВИЧ-инфекции (СПИД) |
Противоретровирусные препараты, эффективные при ВИЧ-инфекции, представлены следующими группами.
1. Ингибиторы обратной транскриптазы
А. Нуклеозиды
Зидовудин
Диданозин
Зальцитабин
Ставудин
Б. Ненуклеозидные соединения
Невирапин
Делавирдин
Эфавиренц
2. Ингибиторы ВИЧ-протеазы
Индинавир
Ритонавир
Саквинавир
Нельфинавир
Одним из противоретровирусных соединений является производное нуклеозидов азидотимидин (3-азидо-3-дезокситимидин), получивший название зидовудин (азидотимидин, ретровир). Принцип действия зидовудина заключается в том, что он, фосфорилируясь в клетках и превращаясь в трифосфат, ингибирует обратную транскриптазу вирионов, препятствуя образованию ДНК из вирусной РНК. Это подавляет синтез иРНК и вирусных белков, что и обеспечивает лечебный эффект. Препарат хорошо всасывается. Биодоступность значительная. Легко проникает через гематоэнцефалический барьер. Около 75% препарата метаболизируется в печени (образуется глюкуронид азидотимидина). Часть зидовудина выделяется в неизмененном виде почками (табл. 30.2).
Применение зидовудина следует начинать возможно раньше. Его терапевтический эффект проявляется в основном в первые 6-8 мес от начала лечения. Зидовудин не излечивает больных, а лишь задерживает развитие заболевания. Следует учитывать, что к нему развивается устойчивость ретровируса.
Из побочных эффектов на первое место выступают гематологические нарушения: анемия, нейтропения, тромбоцитопения, панцитемия. Возможны головная боль, бессонница, миалгия, угнетение функции почек.
В отношении ВИЧ эффективен также ставудин (зерит). Он является синтетическим аналогом тимидина. В организме превращается в трифосфат, который и подавляет репликацию вирусов ВИЧ за счет ингибирования обратной транскриптазы и угнетения синтеза ДНК, иРНК и вирусных белков.
| Таблица 30.2 Сравнительная характеристика некоторых ингибиторов обратной транскриптазы | |||||||
| Препарат | Противовирусная активность | Биодоступность, % | Время накопления препарата и максимальных концентраций в плазме крови (Tmax), ч | Время «полужизни» (t1/2), ч. | Связывание с белками плазмы крови, % | Метаболизм в печени, % | Выведение неизмененного препарата, % |
| Нуклеозиды | |||||||
| Зидовудин | ++ | 60-70 | 0,5-1 | 0,8-1,9 | 20-38 | 60-80 | |
| Диданозин | ++ | 0,5-0,75 | 1,0 | <5 | 20-50 | ||
| Зальцитабин | + | ~90 | 0,8 | 1-2 | <5 | 60-70 | |
| Ставудин | ++ | 80-90 | 0,5-0,75 | 1,4 | <5 | ||
| Ламивудин | ++ | 0,5-1,5 | 5-7 | <35 | 20-30 | 50-85 | |
| Абакавир | +++ | >70 | 0,5-0,63 | 0,8-1,5 | ~50 | >80 | <5 |
| Ненуклеозидные соединения | |||||||
| Невирапин | +++ | 2-4 | 25-30 | >97 | <3 | ||
| Делавирдин | +++ | 0,5 | 2-11 | 40-50 | >97 | <3 | |
| Эфавиренц | +++ | 3,5-5 | 40-50 | >97 | <1 |
Хорошо и быстро всасывается при энтеральном введении; биодоступность высокая. Быстро накапливается в плазме крови. С белками плазмы крови связывается в незначительной степени. Основная часть препарата и его метаболитов выделяется почками.
Применяется для лечения ВИЧ-инфицированных больных после продолжительного использования зидовудина. Вводится энтерально.
Из побочных эффектов отмечаются периферическая нейропатия, головная боль, лихорадка, диспепсические нарушения, анорексия, бессонница, аллергические реакции.
Для лечения ВИЧ-инфекций, в том числе СПИДа, предложены также диданозин (видекс) и зальцитабин (хивид). Оба препарата ингибируют обратную транскриптазу вирусов. Из побочных эффектов чаще всего наблюдается периферическая нейропатия. Возможны обострение хронического панкреатита, анемия, лейкопения, тромбоцитопения, диспепсические явления, нарушения со стороны функции печени (для диданозина). Применяют эти препараты последовательно с зидовудином или в случае неэффективности последнего. Вводят внутрь.
К этой же группе относятся ламивудин, абакавир (см. табл. 30.2).
К ненуклеозидным противоретровирусным препаратам относятся невирапин (вирамун), делавирдин (рескриптор), эфавиренц (сустива). Они оказывают прямое неконкурентное ингибирующее действие на обратную транскриптазу. Связываются с этим ферментом в другом месте по сравнению с нуклеозидными соединениями. Имеются данные о том, что эти вещества оказывают блокирующее влияние на ДНК-полимеразу. Активно метаболизируются в печени цитохромом Р-450. Метаболиты выделяются почками. Применяются только при инфицировании ВИЧ-1.
Из побочных эффектов чаще всего возникает кожная сыпь, повышается уровень трансаминазы.
Для лечения ВИЧ-инфекции предложена новая группа препаратов — ингибиторы протеаз ВИЧ. Эти ферменты, регулирующие образование структурных белков и ферментов вирионов ВИЧ, необходимы для размножения ретровирусов. При недостаточном их количестве образуются незрелые предшественники вируса, что задерживает развитие инфекции. Аспартатпротеаза ВИЧ по структуре существенно отличается от аналогичных ферментов человека, что позволяет создавать препараты указанного типа с выраженной избирательностью противовирусного действия.
К этой группе относятся производные пептидов — саквинавир (инвираза), нельфинавир (вирасепт), индинавир, ритонавир и др. Имеющиеся клинические данные свидетельствуют о выраженной противоретровирусной активности синтезированных ингибиторов ВИЧ-протеаз.
Более широко исследован в клинике саквинавир (инвираза). Он является высокоактивным и избирательным ингибитором протеаз ВИЧ-1 и ВИЧ-2. Несмотря на низкую биодоступность препарата (~ 4%), удается достигать таких концентраций его в плазме крови, которые подавляют размножение ретровирусов. Большая часть вещества связывается с белками плазмы крови. Вводится препарат внутрь. Из побочных эффектов отмечаются диспепсические расстройства, повышение активности печеночных трансаминаз, нарушения липидного обмена, гипергликемия. Возможно развитие устойчивости вирусов к саквинавиру.
Фармакокинетика других препаратов представлена в табл. 30.3.
При лечении ВИЧ-инфекции наиболее эффективно сочетанное применение ингибиторов протеаз ВИЧ с другими препаратами (например, саквинавир + зидовудин; саквинавир + зидовудин + зальцитабин).
Значительным достижением является создание избирательно действующих противогерпетических средств, являющихся синтетическими производными нуклеозидов. К числу высокоэффективных препаратов данной группы относится ацикловир (зовиракс). По химической структуре это аналог пуриновых нуклеозидов. В клетках ацикловир фосфорилируется. В инфицированных клетках действует в виде трифосфата, оказывая ингибирующее влияние на ДНК-полимеразу вируса, что угнетает репликацию вирусной ДНК. Как уже отмечалось, последняя
| Таблица 30.3 Сравнительная характеристика некоторых ингибиторов ВИЧ-протеаз | ||||||||
| Препарат | Противовирусная активность | Биодоступность, % | Время накопления препарата и максимальных концентраций в плазме крови (Tmax), ч | Время «полужизни» (t1/2), ч. | Связывание с белками плазмы крови, % | Метаболизм в печени, % | Содержание в цереброспинальной жидкости, % | Выведение неизмененного препарата, % |
| Саквинавир | ++ | < 4-12 | 2-4 | 7-12 | >97 | < 1 | ~ 1 | |
| Нельфинавир | +++ | >78 | 2-4 | 3,5-5 | >98 | >78 | < 1 | 1-2 |
| Индинавир | +++ | 60-65 | 0,8 | 1,8 | 60-65 | 88-90 | ~ 12 | 5-12 |
| Ритонавир | +++ | 66-75 | 2-4 | 3-5 | 98-99 | >95 | 3,5-5 |
значительно (в сотни раз) чувствительнее аналогичного фермента клеток макроорганизма.
Всасывание ацикловира из желудочно-кишечного тракта неполное. Максимальная концентрация определяется через 1-2 ч. Биодоступность около 20%. С белками плазмы связывается 12-15% вещества. Вполне удовлетворительно проходит через гематоэнцефалический барьер.
Назначают препарат в основном при простом герпесе (Herpes simplex), при поражении глаз, гениталий и герпетических поражениях другой локализации, иногда при опоясывающем лишае (Herpes zoster), а также при цитомегаловирусной инфекции. Вводят ацикловир внутрь, внутривенно (в виде натриевой соли) и местно. При местном применении может отмечаться небольшой раздражающий эффект. При внутривенном введении ацикловира иногда возникают нарушение функции почек, энцефалопатия, флебит, кожная сыпь. При энтеральном введении отмечаются тошнота, рвота, диарея, головная боль.
Новый противогерпетический препарат валацикловир (валтрекс) — L-валиловый эфир ацикловира — отличается от ацикловира большей биодоступностью при энтеральном приеме (для валацикловира биодоступность ~ 54%, т.е. существенно выше, чем у ацикловира). Это пролекарство; при первом его прохождении через кишечник и печень высвобождается ацикловир, который и обеспечивает противогерпетическое действие.
К этой же группе относятся фамцикловир и его активный метаболит ганцикловир, сходные по фармакодинамике с ацикловиром.
Эффективным препаратом является также видарабин (аденин арабинозид). Проникнув в клетку, видарабин фосфорилируется. Угнетает вирусную ДНК-полимеразу. При этом подавляется репликация крупных ДНК-содержащих вирусов. В организме частично превращается в менее активный в отношении вирусов гипоксантина арабинозид.
Видарбин с успехом применяется при герпетическом энцефалите (вводят путем внутривенной инфузии), снижая летальность при этом заболевании на 30-75%. Иногда его используют при осложненном опоясывающем лишае. Эффективен при герпетическом кератоконъюнктивите (назначают местно в мазях). В последнем случае он в меньшей степени вызывает раздражение и меньше угнетает заживление роговицы, чем идоксуридин (см. ниже). Легче проникает в более глубокие слои ткани (при лечении герпетического кератита). Возможно применение видарабина при аллергических реакциях на идоксуридин и при неэффективности последнего.
Из побочных эффектов возможны диспепсические явления (тошнота, рвота, диарея), кожная сыпь, нарушения со стороны ЦНС (галлюцинации, психозы, тремор и др.), тромбофлебит на месте введения.
Местно используют трифлуридин и идоксуридин.
Трифлуридин является фторированным пиримидиновым нуклеозидом. Угнетает синтез ДНК. Применяется при первичном кератоконъюнктивите и возвратном эпителиальном кератите, вызванном вирусом простого герпеса (тип 1 и 2). Раствор трифлуридина наносят местно на слизистую оболочку глаза. Возможны преходящее раздражающее действие, отек век.
Идоксуридин (керецид, идуридин, офтан-IDU), являющийся аналогом тимидина, встраивается в молекулу ДНК. В связи с этим он подавляет репликацию отдельных ДНК-содержащих вирусов. Применяют идоксуридин местно при герпетической инфекции глаз (кератите). Может вызывать раздражение, отек век. Для резорбтивного действия малопригоден, так как токсичность у препарата значительная (подавляет лейкопоэз).
При цитомегаловирусной инфекции используют ганцикловир и фоскарнет. Ганцикловир (цимевен) является синтетическим аналогом 2-дезоксигуанозинового нуклеозида. По механизму действия сходен с ацикловиром. Угнетает синтез вирусной ДНК. Препарат применяют при цитомегаловирусном ретините. Вводят внутривенно и в полость конъюнктивы. Побочные эффекты наблюдаются часто; многие из них приводят к тяжелым нарушениям функций различных органов и систем. Так, у 20-40% пациентов отмечаются гранулоцитопения, тромбоцитопения. Нередки неблагоприятные неврологические эффекты: головная боль, острый психоз, судороги и др. Возможны развитие анемии, кожные аллергические реакции, гепатотоксическое действие. В экспериментах на животных установлено его мутагенное и тератогенное влияние.
В связи с тем что ганцикловир плохо всасывается при энтеральном введении, было создано пролекарство валганцикловир (вальцит). Последний хорошо и быстро всасывается из пищеварительного тракта. В кишечнике и печени под влиянием эстераз превращается в ганцикловир, который и оказывает противовирусное действие. При приеме внутрь биодоступность ганцикловира соответствует 5-9%, а при использовании валганцикловира — 60%.
Фоскарнет (фоскарвир) — производное фосфономуравьиной кислоты. Ингибирует ДНК-полимеразу вирусов. Применяется при цитомегаловирусном ретините у больных СПИДом. Используется также в случае неэффективности ацикловира при простом герпесе и опоясывающем лишае. Вводится внутривенно, так как плохо всасывается из пищеварительного тракта. В виде мази применяется также при герпесе, но менее эффективен, чем ацикловир. В целом фоскарнет переносится хуже, чем ганцикловир. Однако лейкопоэз угнетает в меньшей степени. Препарат нефротоксичен. Может вызвать гипокальциемию. При его применении могут возникать лихорадка, тошнота, рвота, диарея, головная боль, судороги.
Исходя из идеи создания так называемых «антисенсовых олигонуклеозидов», предложен первый препарат такого типа — витравен, рекомендованный для лечения ретинита при цитомегаловирусной инфекции.
Ряд препаратов эффективен в качестве противогриппозных средств.
Противовирусные препараты, эффективные при гриппозной инфекции, могут быть представлены следующими группами.
1. Ингибиторы вирусного белка М2
Ремантадин
Мидантан (амантадин)
2. Ингибиторы вирусного фермента нейраминидазы
Занамивир
Осельтамивир
3. Ингибиторы вирусной РНК-полимеразы
Рибавирин
4. Разные препараты
Арбидол
Оксолин
Первая группа относится к ингибиторам М2-белка. Мембранный белок М2, функционирующий в качестве ионного канала, обнаружен только у вируса гриппа типа А. Ингибиторы этого белка нарушают процесс «раздевания» вируса и препятствуют высвобождению в клетке вирусного генома. В итоге подавляется репликация вируса.
К этой группе относится мидантан (адамантанамина гидрохлорид, амантадин, симметрел). Хорошо всасывается из желудочно-кишечного тракта. Выделяется в основном почками.
Иногда препарат примененяется для профилактики гриппа типа А. В качестве лечебного средства малоэффективен. Более широко мидантан используется как противопаркинсоническое средство (см. главу 10). Вводят его внутрь.
Мидантан может оказывать отрицательное влияние на ЦНС (возникают повышенная возбудимость, сонливость, тремор, атаксия). Возможны диспепсические нарушения, кожные поражения.
Аналогичными свойствами, показаниями к применению и побочными эффектами обладает ремантадин (ремантадина гидрохлорид), сходный по химической структуре с мидантаном. У ремантадина t1/2 в 2 раза продолжительнее, чем у мидантана, и соответствует 24-30 ч. В меньшей степени, чем мидантан, препарат влияет на ЦНС. В связи с этим применяется значительно чаще, чем последний.
К обоим препаратам довольно быстро развивается резистентность вирусов.
Вторая группа препаратов ингибирует вирусный фермент нейраминидазу, которая представляет собой гликопротеин, образующийся на поверхности вирусов гриппа типа А и В. Этот фермент способствует попаданию вируса к клеткам-«мишеням» в респираторном тракте. Специфические ингибиторы нейраминидазы (конкурентное, обратимое действие) препятствуют распространению вируса, связанного с инфицированными клетками. Нарушается репликация вируса.
Одним из ингибиторов этого фермента является занамивир (реленца). Его применяют интраназально или ингаляционно (в порошке). При ингаляции препарата биодоступность соответствует примерно 15%. t1/2 ~ 2 ч. Выделяется препарат почками. При местном применении побочных эффектов не отмечено. В редких случаях на фоне имеющейся патологии дыхательных путей наблюдается бронхоспазм.
Второй препарат — осельтамивир (тамифлу) — используется в виде этилового эфира. Он хорошо всасывается из пищеварительного тракта, быстро гидролизуется (в кишечнике, печени, крови). Биодоступность активного метаболита около 80%. Максимальная концентрация в плазме крови определяется через 3-4 ч. t1/2 ~ 6-10 ч. Выделяется почками.
Переносится препарат относительно хорошо. Однако около 15% больных отмечают тошноту, реже возникает рвота. Для уменьшения диспепсических явлений рекомендуется принимать препарат во время еды.
Созданы препараты, применяемые как при гриппе, так и при других вирусных инфекциях. К группе синтетических препаратов, ингибирующих синтез нуклеиновых кислот, относится рибавирин (рибамидил). Он является гуанозиновым аналогом. В организме препарат фосфорилируется. Монофосфат рибавирина угнетает синтез гуаниновых нуклеотидов, а трифосфат ингибирует вирусную РНК-полимеразу и нарушает образование иРНК.
Эффективен при гриппе типа А и В, тяжелой респираторной синцитиальной вирусной инфекции (вводят ингаляционно), геморрагической лихорадке с почечным синдромом и при ласской лихорадке (внутривенно). Из побочных эффектов отмечаются кожная сыпь, конъюнктивит. В эксперименте показано, что рибавирин обладает мутагенным, тератогенным и канцерогенным эффектами.
К числу разных препаратов относится арбидол. Он является производным индола. Применяется для профилактики и лечения гриппа, вызванного вирусами гриппа типа А и В, а также при острых респираторных вирусных инфекциях. По имеющимся данным, арбидол, помимо умеренного противовирусного действия, обладает интерфероногенной активностью. Кроме того, он стимулирует клеточный и гуморальный иммунитет. Вводится препарат внутрь. Переносится хорошо.
К этой группе можно отнести и препарат оксолин, оказывающий вирулицидное действие. Он характеризуется умеренной эффективностью в профилактике гриппа, при ринитах вирусной этиологии, аденовирусном кератоконъюнктивите, герпетическом кератите, некоторых вирусных заболеваниях кожи (при пузырьковом простом лишае, опоясывающем лишае). Применяют его местно. Оксолин может вызывать ощущение жжения.
Важнейшей проблемой является изыскание средств против пикорнавирусов, в частности риновирусов (относятся к РНК-содержащим вирусам). Эти вирусы являются причиной острых респираторных вирусных инфекций (ОРВИ), известных как простудные заболевания. Встречается эта патология очень часто. Вакцинация в данном случае бесполезна, так как имеется более 100 серотипов риновирусов. Поэтому необходимы лекарственные препараты, которые губительно действуют на любые штаммы риновирусов. Определенные успехи в этом достигнуты за последнее время. Поиски эффективных соединений проводились в следующих направлениях:
1. Создание веществ, препятствующих связыванию вируса с рецепторами поверхности клетки-«мишени».
2.Поиск ингибиторов протеаз, участвующих в синтезе белка, необходимого для репликации вирусов.
3. Создание ингибиторов функции белковой оболочки вируса-капсида, препятствующих фиксации вируса на рецепторах клетки-«мишени», проникновению в клетку и процессу его депротеинизации с высвобождением вирусной РНК.
В каждом из этих направлений были получены эффективные вещества, которые, однако, по совокупности свойств оказались недостаточно совершенными для клинического применения.
Единственным перспективным соединением является плеконарил (ингибитор функции капсида). По предварительным данным, он обладает высокой эффективностью, хорошей биодоступностью и достаточной безопасностью. Плеконарил в настоящее время находится в процессе исследования, и прогнозировать его перспективы пока затруднительно. Однако он заслуживает упоминания как первое специфическое противопикорнавирусное соединение.
Выраженной противовирусной активностью обладает метисазон (марборан). Он эффективен в отношении вируса оспы. Механизм действия, по-видимому, связан с тем, что метисазон нарушает процесс сборки вирионов, угнетая синтез вирусного структурного белка.
Применяют препарат для профилактики оспы, а также для уменьшения осложнений при противооспенной вакцинации. Назначают метисазон внутрь.
Из побочных эффектов чаще всего возникают диспепсические явления (тошнота, рвота). Противопоказаниями к применению метисазона являются тяжелые заболевания печени, почек, желудочно-кишечного тракта.
Приведенные препараты относятся к синтетическим соединениям. Вместе с тем для противовирусной терапии применяют и биогенные вещества, особенно интерфероны.
Интерфероны используют для профилактики вирусных инфекций. Это группа соединений, относящихся к низкомолекулярным гликопротеинам, вырабатывается клетками организма при воздействии на них вирусов, а также ряда биологически активных веществ эндо- и экзогенного происхождения. Образуются интерфероны в самом начале инфекции. Они повышают устойчивость клеток к поражению вирусами. Характеризуются широким противовирусным спектром. Специфичностью действия в отношении отдельных вирусов не обладают, однако имеют выраженную видовую специфичность в отношении клеток макроорганизма. Резистентности к интерферонам у вирусов не возникает. Через несколько недель после выздоровления интерфероны в крови не обнаруживаются.
Интерфероны связываются со специфическими рецепторами на поверхности клеток. Механизм их противовирусного действия, по-видимому, обусловлен тем, что они вызывают образование рибосомами клеток макроорганизма ряда ферментов, которые ингибируют иРНК и ее трансляцию в вирусный белок. Это приводит к угнетению репродукции вирусов.
Для интерферонов человека t1/2 при внутривенном введении составляет 2-4 ч. Через гематоэнцефалический барьер интерфероны практически не проходят.
Известны 3 основных типа интерферонов: α (лейкоцитарный; IFN-α), β (фибробластный; IFN-β) и γ (иммунный интерферон, продуцируемый в основном Т-лимфоцитами; IFN-γ). В настоящее время методом генной инженерии получены все 3 разновидности интерферонов человека. В качестве противовирусных средств в основном используются препараты α-интерферонов (α-2а и α-2b), как естественных, так и рекомбинантных (интрон-А, роферон-А, алферон и др.). Место интерферонов в лечении вирусных инфекций требует уточнения. Отмечена более или менее выраженная эффективность интерферонов при герпетическом кератите, герпетических поражениях кожи и половых органов, ОРВИ, при опоясывающем лишае, вирусном гепатите В и С, при СПИДе. Применяют интерфероны местно и парентерально (внутривенно, внутримышечно, подкожно).
Из побочных эффектов возможны повышение температуры, развитие эритемы и болезненность в месте введения препарата, отмечается прогрессирующая утомляемость. В больших дозах интерфероны могут угнетать кроветворение (развиваются гранулоцитопения и тромбоцитопения). Описаны отдельные случаи аллергических реакций.
Предложен препарат пегасис, представляющий собой конъюгат интерферона α-2а с бис-монометоксиполиэтиленгликолем. Вводят подкожно один раз в неделю. Рекомендован для лечения больных хроническим гепатитом С без цирроза или с компенсированным циррозом у взрослых.
Помимо противовирусного действия, интерфероны обладают антиклеточной, противоопухолевой и иммуномодулирующей активностью. Показано, что они подавляют рост нормальных и опухолевых клеток. Очевидно, это связано с угнетением деления клеток. Иммунный интерферон (γ-интерферон, Т-интерферон), продуцируемый в основном Т-лимфоцитами, является цитокином. Он характеризуется антипролиферативной активностью, а также повышает активность макрофагов и цитотоксичность естественных клеток-киллеров.
Способностью вызывать образование интерферонов обладают не только вирусы, но и многие бактерии, риккетсии, экстракты грибов и плесеней, а также различные химические соединения. Некоторые интерфероногены используют в медицинской практике. Так, при вирусных инфекциях глаз иногда применяют интерфероноген полудан. По химическому строению он является полиаденилуридиловой кислотой. Препарат закапывают в конъюнктивальный мешок, а также вводят субконъюнктивально.
Для введения внутрь создан индуктор эндогенного интерферона амиксин — низкомолекулярное синтетическое соединение из группы флуоренов. Он повышает продукцию интерферона Т-клетками. Является также иммуностимулятором и оказывает прямое противовирусное действие.
Применяется при гриппе и других острых респираторных вирусных инфекциях, при гепатите А и В, нейровирусных инфекциях, герпесе, цитомегаловирусных инфекциях.
Переносится препарат хорошо. При 1-2-кратном применении побочные эффекты не воникают. При многократном введении он кумулирует. Широта химиотерапевтического действия невелика (коэффициент безопасности 2-4). Возможна индивидуальная непереносимость. Противопоказан при беременности.
Принципиально новым направлением является использование интерферона-β для лечения рассеянного склероза, который относится к группе хронических демиелинизирующих заболеваний нервной системы. Встречается эта патология довольно часто, особенно в молодом возрасте, и быстро приводит к инвалидизации. Недавно для практического применения при рассеянном склерозе был предложен интерферон β-1b, полученный методом генной инженерии. Соответствующий препарат получил название «бетаферон». Предпосылкой для испытания данного цитокина явились данные о том, что вирусы играют определенную роль (возможно, в качестве триггерного фактора) в развитии рассеянного склероза. Основой современного лечения этого заболевания является иммунотерапия. Однако среди комплекса применяемых средств только бетаферон оказался действительно эффективным препаратом. Он не излечивает больных, но заметно уменьшает частоту и тяжесть обострений и замедляет прогрессирование заболевания. Соответственно понижается частота госпитализации больных. Бетаферон — первое лекарственное средство для лечения ремиттирующего и вторично-прогрессирующего рассеянного склероза.
Вводят препарат подкожно. Дозируют в международных единицах.
Переносится он обычно хорошо, однако часто отмечаются реакции в месте его введения (покраснение кожи, боли). Поэтому следует менять места инъекций. Нередко возникают лихорадка, общая слабость, мышечные боли (гриппоподобное состояние). Иногда развиваются лимфопения, анемия, нейтрофилопения, тромбоцитопения. Возможны нарушения менструального цикла.
Для окончательного суждения об эффективности и безопасности бетаферона понадобятся более длительные и масштабные исследования.
| Препараты | ||
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Мидантан — Midantanum | Внутрь 0,1 г | Таблетки, покрытые оболочкой, по 0,1 г |
| Ремантадин — Remantadinum | Внутрь 0,05-0,1 г | Таблетки по 0,05 г |
| Идоксуридин — Idoxuridine | В полость конъюнктивы 2 капли 0,1% раствора | 0,1% раствор |
| Оксолин — Oxolinum | В полость конъюнктивы 1-2 капли 0,1-0,2% раствора, 0,25% мазь; для смазывания слизистой оболочки носа 0,25—0,5% мазь; наружно 1—3% мазь | Порошок; 0,25%; 0,5%; 1%; 2% и 3% мазь |
| Ацикловир — Acyclovir | Внутрь 0,2 г; внутривенно 5—10 мг/кг; накожно 5% мазь | Таблетки по 0,2 г; 5% мазь в тубах по 5 г; 3% глазная мазь в тубах по 4,5 или 5 г; во флаконах по 0,25 г |
| Валацикловир — Valacyclovir | Внутрь 0,5—1 г | Таблетки по 0,5 г |
| Ганцикловир — Gancyclovir | Внутривенные инфузии 0,005-0,006 г/кг | Лиофилизированный порошок во флаконах по 0,546 г ганцикловира натрия (соответствует 0,5 г ганцикловира основания) |
| Рибавирин — Ribavirin | Внутрь 0,2 г | Таблетки по 0,2 г |
| Зидовудин — Zidovudine | Внутрь 0,1-0, 2 г | Капсулы по 0,1 г |
| Арбидол — Arbidolum | Внутрь 0,1-0, 2 г | Таблетки по 0,025; 0,05 и 0,1 г |
| Амиксин — Amixinum | Внутрь 0,125-0, 25 г | Таблетки по 0,125 г |
Глава 31 ПРОТИВОПРОТОЗОЙНЫЕ СРЕДСТВА
Для лечения заболеваний, вызываемых патогенными простейшими, предложено значительное число противопротозойных препаратов. Основные представители этой группы химиотерапевтических средств названы в приводимой классификации.
1. Средства, применяемые для профилактики и лечения малярии
Хингамин
Примахин
Хлоридин
Хинин
Сульфаниламиды и сульфоны
Мефлохин
2. Средства, применяемые при лечении амебиаза
Метронидазол
Хингамин
Эметина гидрохлорид
Тетрациклины
Хиниофон
3. Средства, применяемые при лечении лямблиоза
Метронидазол
Фуразолидон
Акрихин
4. Средства, применяемые при лечении трихомоноза
Метронидазол
Тинидазол
Трихомонацид
Фуразолидон
5. Средства, применяемые при лечении токсоплазмоза
Хлоридин
Сульфадимезин
6. Средства, применяемые при лечении балантидиаза
Тетрациклины
Мономицин
Хиниофон
7. Средства, применяемые при лечении лейшманиозов
Солюсурьмин
Натрия стибоглюконат
Метронидазол
31.1. СРЕДСТВА, ПРИМЕНЯЕМЫЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ МАЛЯРИИ
Во многих странах с жарким климатом малярия до сих пор остается одним из наиболее частых заболеваний. В нашей стране малярия встречается редко.
Возбудителями малярии являются плазмодии. Трехдневную малярию вызывают Plasmodium vivax и P. ovale, тропическую — P.falciparum, четырехдневную — P. malariae. Наиболее частыми возбудителями малярии являются P. vivax и P. falciрагum. Малярийный плазмодий имеет два цикла развития. Бесполый цикл (шизогония) проходит в организме человека, половой (спорогония) — в теле комара.
При укусе комара в организм человека попадают спорозоиты, быстро внедряющиеся в клетки печени. Там они проходят цикл развития (это так называемые преэритроцитарные формы плазмодия) и затем делятся, превращаясь в тканевые мерозоиты. Мерозоиты, попадая в кровь, проникают в эритроциты, где осуществляется развитие эритроцитарных форм. При созревании в них шизонта наступает его множественное деление (меруляция). Образующиеся при этом эритроцитарные мерозоиты (морулы) выходят в кровь и вновь внедряются в эритроциты, повторяя цикл шизогонии. Момент разрушения эритроцитов и выхода мерозоитов в кровь проявляется приступом лихорадки.
Из части эритроцитарных мерозоитов образуются мужские и женские половые клетки — гамонты. Их оплодотворение происходит только в теле комара. Половой цикл завершается образованием спорозоитов, которые при укусе со слюной комара попадают в кровь человека и дают начало новому бесполому циклу развития малярийного плазмодия.
При трех- и, возможно, четырехдневной малярии после окончания преэритроцитарного цикла часть тканевых мерозоитов вновь внедряется в клетки печени, где в течение длительного времени они повторяют циклы развития, не вызывая каких-либо клинических проявлений. Эти формы плазмодия получили название параэритроцитарных. Они обусловливают возобновление эритроцитарного цикла развития плазмодия и наступление отдаленных рецидивов. При тропической малярии параэритроцитарные формы отсутствуют.
Первоначально для химиотерапии малярии использовали хинин, выделенный из коры хинного дерева. Затем было создано значительное число синтетических препаратов.
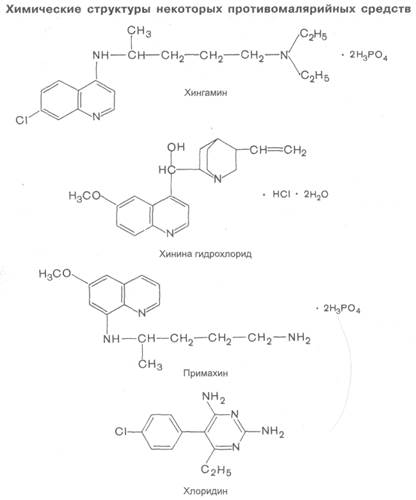
По химическому строению противомалярийные средства подразделяют на следующие группы.
А. Производные хинолина
4-замещенные хинолины
Хингамин (хлорохин)
Хинин
Мефлохин
8-аминохинолины
Примахин
Б. Производные пиримидина 1
Хлоридин (пириметамин)
См. химические структуры.
Противомалярийные средства отличаются друг от друга тропностью в отношении определенных форм развития плазмодия в организме человека (рис. 31.1). В связи с этим различают:
1) гематошизотропные средства (влияют на эритроцитарные шизонты);
2) гистошизотропные средства (влияют на тканевые шизонты);
а) влияющие на преэритроцитарные (первичные тканевые) формы;
б) влияющие на параэритроцитарные (вторичные тканевые) формы;
3) гамонтотропные средства (влияют на половые формы).
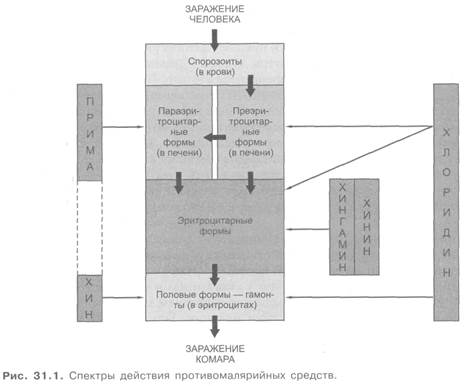
Знание направленности действия противомалярийных средств имеет большое значение для их эффективного применения при лечении и профилактике малярии.
31.1.1. ГЕМАТОШИЗОТРОПНЫЕ СРЕДСТВА
Особенно широко применяется хингамин (хлорохин, делагил, резохин). Он является производным 4-аминохинолина. Главное в его противомалярийном эффекте — гематошизотропное действие, направленное на эритроцитарные формы плазмодиев. В этом отношении он превосходит все другие противомалярийные препараты. В небольшой степени влияет на половые клетки P. vivax. Устойчивость плазмодиев к хингамину развивается сравнительно медленно.
Хингамин оказывает также амебицидное действие. Кроме того, у него имеются иммунодепрессивные и противоаритмические свойства.
Из желудочно-кишечного тракта хингамин всасывается быстро и почти полностью. При этом пути введения препарат накапливается в плазме крови в максимальных концентрациях через 1-2 ч. Около половины вещества вступает в связь с белками плазмы. В больших концентрациях хингамин обнаруживается и в тканях. Выделяется из организма медленно. Для снижения его концентрации в плазме на 50% требуется около 3 дней. Основной путь выведения хингамина и его метаболитов — через почки. Около 70% препарата выделяется в неизмененном виде. Скорость элиминации возрастает в кислой среде и снижается при щелочной реакции мочи.
Применяют хингамин при всех видах малярии, а также при внекишечном амебиазе. Кроме того, он эффективен (очевидно, вследствие иммунодепрессивных свойств) при коллагенозах (например, при ревматизме и ревматоидном артрите). Назначают его также профилактически при нарушениях ритма сердца и при амилоидозе. Вводят хингамин обычно внутрь, иногда — парентерально.
При лечении малярии хингамин переносится хорошо. Побочные эффекты возникают главным образом при длительном его применении в больших дозах (при лечении коллагенозов). Они проявляются в виде дерматита, диспепсических явлений, головокружений. Тяжелым осложнением являются нарушения зрения (включая ретинопатию). Редко отмечаются лейкопения, угнетение функции печени. При длительном применении хингамина требуется контроль за состоянием зрения, функцией печени и кроветворением.
Аналогичными препаратами по фармакологическим свойствам и показаниям к применению являются галохин (циклохин), гидроксихлорохин (плаквенил), амодиахин (камохин).
К гематошизотропным средствам принадлежит также хлоридин (пириметамин). Он, являясь ингибитором дигидрофолатредуктазы, относится к веществам, нарушающим обмен дигидрофолиевой кислоты. Отличается выраженным депонированием в тканях (но меньшим, чем у хингамина) и продолжительным эффектом. В связи с медленно развивающимся действием хлоридин применяют в основном с целью личной профилактики малярии. Устойчивость малярийных плазмодиев к данному препарату развивается довольно быстро. При тропической малярии, устойчивой к хингамину, комбинируют хлоридин с сульфаниламидами. Применяют хлоридин в сочетании с сульфаниламидами не только при малярии, но и при лечении токсоплазмоза.
Губительное действие на эритроцитарные шизонты оказывает алкалоид коры хинного дерева хинин. Он обладает сравнительно низкой противомалярийной активностью. Большим преимуществом хинина является быстрое развитие эффекта. Хинин характеризуется значительной токсичностью. При его применении часто наблюдаются разнообразные побочные эффекты (головокружение, нарушение слуха и зрения, угнетение функции почек, тошнота, рвота, диарея, аллергические реакции).
Наибольший интерес хинин представляет для купирования и лечения тропической малярии, устойчивой к хингамину, а также при множественной устойчивости.
В качестве лекарственных препаратов используют хинина сульфат, гидрохлорид и дигидрохлорид.
К группе производных 4-хинолинметанола относится синтетический препарат мефлохин. Аналогично хинину он оказывает гематошизотропное действие. Характеризуется большой продолжительностью эффекта. t1/2 > 6 дней (для хинина t1/2 ~ 10 ч). Вводится только внутрь. Характеризуется раздражающим действием. Менее токсичен, чем хинин. Возможны диспепсические явления, кожная сыпь, головная боль, головокружение. При использовании препарата в больших дозах могут возникать неврологические нарушения, судороги.
Гематошизотропной активностью обладают также сульфаниламиды и сульфоны. Их эффективность связана со способностью нарушать утилизацию малярийным плазмодием пара-аминобензойной кислоты.
Из сульфаниламидов применяют сульфазин, сульфапиридазин, сульфадиметоксин, сульфален, сульфадоксин. Из группы сульфонов, известных в качестве противолепрозных средств, при лечении и профилактике малярии используют в основном диафенилсульфон (дапсон).
Гематошизотропная активность сульфаниламидов и сульфонов относительно невелика. Действие их развивается медленно. Отдельно эти препараты, как правило, не используют. Их назначают обычно в сочетании с другими противомалярийными средствами, например с хинином, ингибиторами дигидрофолатредуктазы (хлоридином, триметопримом и др.).
Нередко используют комбинированные препараты, например фансидар (хлоридин + сульфадоксин).
При устойчивости к хингамину иногда применяют антибиотик тетрациклинового ряда доксициклин.
31.1.2. ГИСТОШИЗОТРОПНЫЕ СРЕДСТВА
К препаратам, подавляющим преэритроцитарные формы плазмодиев, относится уже рассмотренный хлоридин (см. рис. 31.1).
На параэритроцитарные формы плазмодиев оказывает губительное влияние производное 8-аминохинолина примахин. Он действует также на половые формы плазмодиев (гамонтоцидное действие). Из желудочно-кишечного тракта всасывается хорошо. Максимальная концентрация в плазме достигается через 2 ч. В организме препарат быстро подвергается химическим превращениям. Выделяется почками, преимущественно в виде метаболитов (в течение 1-х суток).
Основным показанием к применению являются предупреждение отдаленных рецидивов трехдневной малярии, а также распространения малярии через переносчика (вследствие гамонтотропного действия).
Из побочных эффектов возможны диспепсические явления, метгемоглобинурия, лейкопения, иногда агранулоцитоз. Улиц с определенным видом генетической энзимопатии (с недостаточностью глюкозо-6-фосфатдегидрогеназы эритроцитов) наступают острый гемолиз и гемоглобинурия.
Примахин можно сочетать с другими препаратами (одновременно и последовательно).
31.1.3. ГАМОНТОТРОПНЫЕ СРЕДСТВА
Препараты, влияющие на половые клетки, могут оказывать как гамонтоцидное (примахин), так и гамонтостатическое (хлоридин) действие. При воздействии гамонтоцидных средств половые клетки плазмодиев гибнут в организме человека. Гамонтостатические средства лишь повреждают половые клетки, в результате чего нарушается процесс спорогонии (на разных стадиях).
31.1.4. ПРИНЦИПЫ ИСПОЛЬЗОВАНИЯ ПРОТИВОМАЛЯРИЙНЫХ СРЕДСТВ
Противомалярийные средства применяют с целью профилактики и лечения малярии.
Личная химиопрофилактика имеет в виду предупреждение развития малярии у здорового человека при его пребывании в опасном по заболеваемости малярией районе. Идеальное средство должно было бы оказывать спорозоитоцидное действие. Однако таких препаратов нет, поэтому используют вещества, влияющие на преэритроцитарные (первичные тканевые) формы. Из таких препаратов был отмечен хлоридин. Кроме того, с целью личной химиопрофилактики используют гематошизотропные средства хингамин, мефлохин и другие, которые предупреждают наступление приступов лихорадки.
Лечение малярии обычно проводят с помощью вводимых внутрь гематошизотропных веществ, влияющих на эритроцитарные формы плазмодиев (хингамин и др.).
При лечении малярии, устойчивой к хингамину и аналогичным препаратам, во многих случаях хороший эффект дает применение хинина, хлоридина, сульфаниламидов и сульфонов.
Нередко назначают комбинации противомалярийных средств с разным механизмом действия.
При быстро развивающейся малярии, особенно при малярийной коме (осложнение тропической малярии), гематошизотропные вещества (например, хинин, хингамин) обычно вводят парентерально в больших дозах.
Радикального излечения только гематошизотропные средства при трех- и четырехдневной малярии не дают, поскольку в связи с развитием параэритроцитарных форм возможны рецидивы заболевания. Поэтому с целью профилактики отдаленных рецидивов (межсезонная, или предэпидемическая, химиопрофилактика) необходимо дополнительно назначать препараты, имеющие тропность к параэритроцитарным формам (примахин). Исключением является тропическая малярия, плазмодии которой, как уже отмечалось, не имеют в цикле своего развития параэритроцитарных форм. Исходя из этого, тропическую малярию можно радикально вылечить одним хлоридином.
Основная задача общественной химиопрофилактики (коллективная эпидемическая химиопрофилактика) — предупреждение передачи малярии от больного человека. С этой целью назначают гамонтотропные средства (примахин, хлоридин). В этом случае в теле комара не образуются спорозоиты.
Таким образом, спектр противомалярийного действия препаратов в значительной степени определяет показания к их применению.
31.2. СРЕДСТВА, ПРИМЕНЯЕМЫЕ ПРИ ЛЕЧЕНИИ АМЕБИАЗА
Возбудителем амебиаза, имеющего очень широкое распространение в странах с жарким климатом, является Entamoeba histolytica. Амебиаз чаще всего поражает толстую кишку (амебная дизентерия). При этом амебы находятся как в просвете кишечника, так и в его стенке. Однако возможен и системный амебиаз с внекишечными очагами поражения. Распространяясь из кишечника по системе воротной вены, амебы могут вызывать гепатит и абсцессы печени. Иногда отмечаются абсцессы легких и других органов.
В зависимости от локализации возбудителя амебиаза требуются те или иные противоамебные средства. Они могут быть представлены следующими основными группами.
Амебициды, эффективные при любой локализации патологического процесса
Метронидазол
Амебициды прямого действия, эффективные преимущественно при локализации амеб в просвете кишечника
Хиниофон
Амебициды непрямого действия, эффективные при локализации амеб в просвете и в стенке кишечника
Тетрациклины
Тканевые амебициды, действующие на амеб в стенке кишечника и в печени
Эметина гидрохлорид
Тканевые амебициды, эффективные преимущественно при локализации амеб в печени
Хингамин
См. химические структуры.
Как отмечено в классификации, универсальным средством, эффективным при кишечном и внекишечном амебиазе, является метронидазол (см. подробно раздел 4 данной главы). Наименее эффективен он в отношении амеб, находящихся в просвете кишечника. Поэтому при амебной дизентерии его обычно сочетают с хиниофоном или йодохинолом. На цисты метронидазол не действует.
Большое значение для радикального излечения амебиаза, предупреждения рецидивов и реинфекции имеют амебициды, активно влияющие на амеб, находящихся в просвете кишечника. Такой направленностью действия обладает производное 8-оксихинолина хиниофон (табл. 31.1).
| Таблица 31.1 Основная направленность действия противоамебных средств | ||||
| Препарат | Средства, применяемые при кишечном амебиазе | Амебициды, применяемые при внекишечном амебиазе | ||
| амебициды, действующие в просвете кишечника | амебициды, действующие в толще слизистой оболочки кишечника | средства, подавляющие бактериальную флору кишечника | ||
| Метронидазол | + | + | + | |
| Эметина гидрохлорид | + | + | ||
| Хиниофон | + | |||
| Хингамин | + | |||
| Тетрациклины | + |
Хиниофон (ятрен) всасывается из желудочно-кишечного тракта лишь на 10-15%, поэтому в кишечнике создаются высокие концентрации вещества, необходимые для амебицидного действия.
Препарат малотоксичен. Из побочных эффектов типична диарея. Возможен неврит зрительного нерва.
Аналогичным хиниофону по структуре и направленности действия препаратом является йодохинол.
Довольно широкое распространение при лечении амебиаза получил алкалоид корня ипекакуаны (Cephaelis ipecacuanha) эметин. В качестве лекарственного препарата используют эметина гидрохлорид. Вводят его внутримышечно, так как при приеме внутрь он вызывает сильное раздражение слизистой оболочки желудочно-кишечного тракта (при этом нередко возникает рвота рефлекторного происхождения).
Действует эметин на амеб, локализованных как внекишечно (например, в печени, где вещество накапливается в высоких концентрациях), так и в стенке кишечника. На амеб, находящихся в просвете кишечника, препарат не влияет.
Выделяется эметин почками в течение длительного времени (более 1 мес). В связи с этим он кумулирует, что является основной причиной передозировки и развития токсических эффектов.
Побочные эффекты касаются сердечно-сосудистой системы (тахикардия, сердечные аритмии, боли в области сердца, гипотония), желудочно-кишечного тракта (тошнота, диарея, рвота), нервно-мышечной системы (мышечная слабость, тремор, невралгия). Возможны нарушения со стороны почек и печени, поэтому во время лечения эметином обязателен периодический контроль функций сердца, почек и печени. При органических заболеваниях сердца и почек препарат противопоказан.
С целью воздействия на амебы, локализованные в печени, с успехом используют хингамин (см. раздел 1 данной главы), который накапливается в ткани печени в высоких концентрациях.
Все перечисленные препараты относятся к амебицидам, оказывающим прямое влияние на возбудителя амебиаза. Вместе с тем при лечении кишечного амебиаза можно воспользоваться тетрациклинами, практически не оказывающими прямого действия на амеб. Как известно, Entamoeba histolytica является анаэробом. Необходимые условия ее существования в кишечнике обеспечивают бактерии, поглощающие кислород. При использовании тетрациклинов кишечная флора подавляется, и это опосредованно неблагоприятно сказывается на росте и размножении амеб, находящихся в просвете и стенке кишечника. Такие препараты могут быть обозначены как противоамебные средства непрямого действия. По эффективности при амебиазе тетрациклины уступают амебицидам прямого действия.
При лечении острого амебиаза кишечника иногда применяют мономицин (вводят внутрь).
Во многих случаях при лечении амебиаза можно ограничиться применением метронидазола. Вместе с тем нередко используют комбинации веществ. Так, при амебной дизентерии целесообразно сочетать препараты, действующие в просвете кишечника, в его стенке, а также предохраняющие печень от попадания в нее амеб (например, метронидазол + хиниофон; эметина гидрохлорид + тетрациклин + хиниофон).
31.3. СРЕДСТВА, ПРИМЕНЯЕМЫЕ ПРИ ЛЕЧЕНИИ ЛЯМБЛИОЗА
Возбудителем лямблиоза является Giardia (lamblia) intestinalis. При наличии лямблий в кишечнике наблюдается его дисфункция (дуоденит, энтерит). Для лечения лямблиоза применяют метронидазол, аминохинол и уразолидон (рис. 31.2; табл. 31.2). О метронидазоле см. в этой главе раздел 4, о фуразолидоне — главу 29.3.
Аминохинол является производным хинолина. Он эффективен при лямблиозе, токсоплазмозе, кожном лейшманиозе, а также при некоторых коллагенозах. В большинстве случаев препарат переносится хорошо. Может вызывать диспепсические нарушения, головную боль, шум в ушах, аллергические реакции.
31.4. СРЕДСТВА, ПРИМЕНЯЕМЫЕ ПРИ ЛЕЧЕНИИ ТРИХОМОНОЗА
При трихомонозе, вызываемом Trichomonas vaginalis (проявляется кольпитом и вульвовагинитом у женщин, уретритом у мужчин), препаратом выбора является метронидазол.

| Таблица 31.2 Фармакотерапия ряда заболеваний, вызываемых простейшими. | ||
| Возбудитель | Заболевание | Препараты |
| Plasmodium vivax, P. ovale, P.falciparum, P. malariae | Малярия | Хингамин Хлоридин Хинин Мефлохин Примахин Фансидар Доксициклин Клиндамицин |
| Entamoeba histolytica | Амебиаз | Метронидазол Тинидазол Орнидазол (тиберал) Хиниофон Йодохинол Хингамин Эметина гидрохлорид Доксициклин Дилоксанид-фуроат Паромомицин |
| Giardia (lamblia) intestinalis | Лямблиоз | Метронидазол Тинидазол Аминохинол Фуразолидон Акрихин |
| Trichomonas vaginalis | Трихомоноз | Метронидазол Тинидазол Нитазол Орнидазол (тиберал) Трихомонацид Фуразолидон Хлоридин +сульфазин |
| Toxoplasma gondii | Токсоплазмоз | Хлоридин Сульфазин Пентамидин Клиндамицин Спирамицин |
| Balantidium coli | Балантидиаз | Тетрациклины Хиниофон Йодохинол Мономицин Метронидазол |
| Leishmania donovani, L. tropica и др. | Лейшманиоз | Солюсурьмин Натрия стибоглюконат Меглумин антимониат Метронидазол Кетоконазол Амфотерицин В Пентамидин Мономицин |
| Tripanosoma gambiense, T. rhodesiense | Сонная болезнь (южноафриканский трипаносомоз) | Меларсопрол Пентамидин Сурамин Эфлорнитин |
| Tripanosoma cruzi | Болезнь Чагаса (южноамериканский трипаносомоз) | Нифуртимокс Бензнидазол Примахин Пуромицин |
| Примечание. Для сведения приведены многие препараты, применяемые для лечения (для профилактики) заболеваний, вызываемых простейшими. Некоторые препараты в тексте не упоминаются. В этом случае н Date: 2015-07-01; view: 1130; Нарушение авторских прав |