
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Монобактамы
|
|
К этой группе относится препарат азтреонам, выделенный из культуры Chromobacterium vialaceum. Устойчив в отношении β-лактамаз, продуцируемых рядом грамотрицательных бактерий, относящихся к группам Klebsiella, Pseudomonas, Serratia. На грамположительные бактерии и анаэробы он не действует. Угнетает синтез клеточной стенки и благодаря этому оказывает бактерицидный эффект. Вводят азтреонам парентерально. t1/2 ~ 1,7 ч. Выводится почками (секрецией). Применяют при инфекциях мочевыводящего тракта, дыхательных путей, кожи и др. Из побочных эффектов отмечаются диспепсические нарушения, кожные аллергические реакции, головная боль, возможна суперинфекция, редко гепатотоксическое действие.
29.1.4. МАКРОЛИДЫ И АЗАЛИДЫ
Антибиотики этой группы в основе своей молекулы содержат макроциклическое лактонное кольцо, связанное с различными сахарами. Представителями макролидов являются эритромицин, олеандомицин, рокситромицин, кларитромицин, а азалидов — азитромицин.
Эритромицин (эритран, эритроцин) продуцируется Streptomyces erythreus. Наиболее чувствительны к нему грамположительные кокки и патогенные спирохеты. Однако в спектр его действия входят также грамотрицательные кокки, палочки дифтерии, патогенные анаэробы, риккетсии, хламидии, микоплазмы, возбудители амебной дизентерии и др. (см. рис. 29.1). Таким образом, по влиянию на различные микроорганизмы эритромицин напоминает бензилпенициллин, но спектр его действия несколько шире.
Механизм действия эритромицина заключается в угнетении синтеза белка рибосомами бактерий. Связано это с угнетением фермента пептидтранслоказы.
Из желудочно-кишечного тракта препарат всасывается не полностью, но в достаточной степени для того, чтобы в крови и тканях создались бактериостатические концентрации. Следует учитывать, что в кислой среде желудка эритромицин частично разрушается, поэтому вводить его следует в кислотоустойчивых капсулах или в таблетках (драже) со специальным покрытием, обеспечивающим высвобождение эритромицина только в тонкой кишке. Препарат легко проникает в различные ткани, в том числе через плаценту. В значительных концентрациях накапливается в фагоцитах (как и другие макролиды). В ткани мозга в обычных условиях не поступает. Длительность действия 4-6 ч. Выделяется с желчью и частично почками.
Применение эритромицина ограничено, так как к нему быстро развивается устойчивость микроорганизмов. Поэтому его относят к антибиотикам резерва и используют в тех случаях, когда пенициллины и другие антибиотики оказываются неэффективными. Назначают эритромицин внутрь (основание эритромицина) и местно.
Эритромицин — малотоксичный антибиотик и относительно редко вызывает побочные эффекты. Иногда возникают диспепсические нарушения, аллергические реакции, возможна суперинфекция.
Аналогичными свойствами и показаниями к применению обладает олеандомицин. Продуцентом его является Streptomyces antibioticus. По активности олеандомицин уступает эритромицину. Спектр и механизм противомикробного действия у них сходны. Продолжительность действия олеандомицина примерно 6 ч. Токсичность низкая. Он обладает более выраженным раздражающим эффектом, чем эритромицин. Относится к антибиотикам резерва. В медицинской практике применяют внутрь олеандомицина фосфат (олеандоцин, ромицил).
Олеандомицина фосфат выпускают в сочетании с тетрациклином (олететрин) и с тетрациклина гидрохлоридом (сигмамицин, тетраолеан).
За последние годы в медицинскую практику внедрен ряд полусинтетических макролидов — кларитромицин, рокситромицин и др. По механизму действия они аналогичны эритромицину.
Кларитромицин (клацид) в 2-4 раза активнее эритромицина в отношении стафилококков и стрептококков. Эффективен при инфекциях, вызванных Micobacterium avium intracellulare и Helicobacter pylory.
Хорошо всасывается из желудочно-кишечного тракта, в том числе после приема пищи. В ткани мозга не проходит. Частично метаболизируется в печени с образованием активного метаболита. Выделяется почками. Действует несколько более продолжительно, чем эритромицин, t1/2 для кларитромицина примерно в 3 раза больше, чем для эритромицина.
Эффективным полусинтетическим макролидом является также рокситромицин (рулид). Он обладает широким антибактериальным спектром действия. Хорошо всасывается при приеме внутрь.
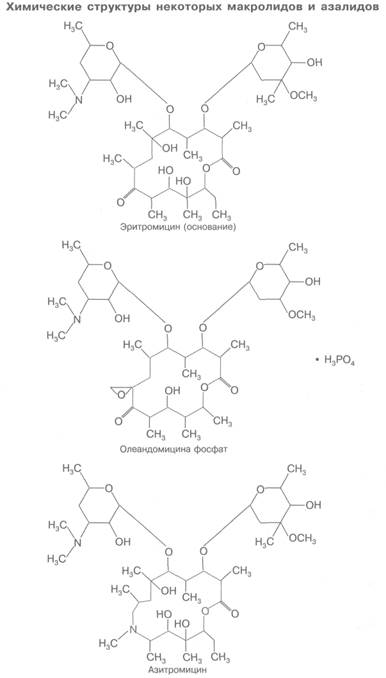
Азалиды химически отличаются от макролидов, однако по основным свойствам сходны с ними. Один из препаратов этой группы, азитромицин (сумамед), в 2-4 раза менее активен по влиянию на стафилококки и стрептококки, чем эритромицин, но превосходит последний по влиянию на Haemophilus influenzae, a также на грамотрицательные кокки. Плохо всасывается в кишечнике, особенно при наличии пищевого содержимого. Для азитромицина характерно накопление в высоких концентрациях в клетках — он может превышать концентрации в плазме крови в 10-100 раз. Действует длительно, t1/2=2-4 дня (для эритромицина t1/2=2-5 ч). Через гематоэнцефалический барьер не проходит. Выделяется почками в неизмененном виде.
Принимают последние два препарата энтерально. Из побочных эффектов иногда отмечаются тошнота, диарея, редко возникает снижение слуха. Стоимость их выше, чем эритромицина.
Следует отметить, что макролиды и азалиды эффективны в отношении облигатных внутриклеточных микроорганизмов — хламидий, микоплазм и легионелл, которые могут быть возбудителями так называемых «атипичных» пневмоний.
29.1.5. ТЕТРАЦИКЛИНЫ
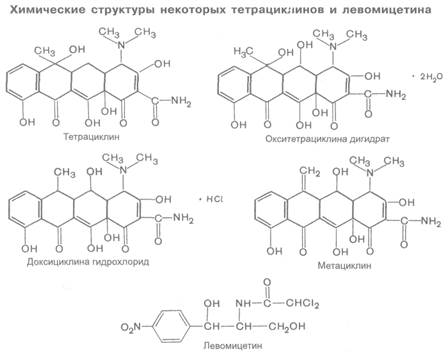
Тетрациклины включают группу антибиотиков, структурную основу которых составляют 4 конденсированных 6-членных цикла (см. структуры). Биосинтетическим путем (ферментацией) получают следующие препараты: окситетрациклина дигидрат (террамицин, тетран, тархоцин) — продуцент Streptomyces rimosus, тетрациклин (десхлорбиомицин) — продуцент Streptomyces aureofaciens. Демеклоциклин продуцируется мутантным штаммом Streptomyces aureofaciens. К числу полусинтетических тетрациклинов относятся метациклина гидрохлорид (рондомицин), доксициклина гидрохлорид (вибрамицин), миноциклин и др.
Тетрациклины обладают широким спектром действия (см. рис. 29.1). Они активны в отношении грамположительных и грамотрицательных кокков; возбудителей бациллярной дизентерии, брюшного тифа; патогенных спирохет; возбудителей особо опасных инфекций — чумы, туляремии, бруцеллеза, холеры; риккетсий; хламидий, некоторых простейших (возбудителей амебной дизентерии). На протей, синегнойную палочку, истинные вирусы и патогенные грибы тетрациклины не действуют. По влиянию на грамположительные микроорганизмы они уступают пенициллинам. Постепенно развивается устойчивость к тетрациклинам.
Механизм их противомикробного действия связан с угнетением внутриклеточного синтеза белка рибосомами бактерий. Кроме того, тетрациклины связывают металлы (Mg2+, Ca2+), образуя с ними хелатные соединения, и ингибируют ферментные системы. Тетрациклины оказывают бактериостатическое влияние. Наиболее активны в отношении размножающихся бактерий. По активности все тетрациклины сходны.
Всасываются тетрациклины из желудка и тонкой кишки. Абсорбция неполная (особенно после приема пищи), но достаточная для того, чтобы обеспечить в организме бактериостатические концентрации. Максимальные концентрации в плазме крови при введении тетрациклинов внутрь достигаются через 2-4 ч.
Тетрациклины образуют хелатные соединения с ионами кальция, железом, алюминием, которые не абсорбируются. Поэтому всасывание тетрациклинов нарушается при содержании в пище этих ионов (например, ионов кальция в молоке и молочных продуктах) или веществ, в состав которых входят эти ионы (например, антацидные средства). В этом отношении особое место занимают доксициклин и миноциклин, которые лишь в небольшой степени образуют хелатные соединения с ионами кальция и поэтому наличие в пищеварительном тракте пищевых масс и ионов кальция не сказывается на их всасывании, которое происходит полно и быстро.
В циркулирующей крови значительная часть тетрациклинов связывается с белками плазмы (от 20 до 80%).
Наиболее продолжительно действуют демеклоциклин, доксициклин и метацикл ин. По длительности действия тетрациклины располагаются в следующем порядке: демеклоциклин > доксициклин > метациклин > окситетрациклин > тетрациклин.
Тетрациклины хорошо проникают через многие тканевые барьеры, в том числе через плацентарный. Определенные их количества проходят через гематоэнцефалический барьер. Однако при введении тетрациклинов внутрь бактериостатические их концентрации в ликворе обычно не накапливаются. Для этого требуется очень высокое содержание антибиотиков в крови, что легче достигается при парентеральном (особенно при внутривенном) введении препаратов (например, доксициклина гидрохлорида). Миноциклин практически не проникает в ткани мозга.
Небольшие количества тетрациклинов обнаруживаются в печени и костях в течение очень длительного времени.
Выделяются тетрациклины с мочой и желчью. Часть выделяющихся с желчью тетрациклинов подвергается повторному всасыванию из тонкой кишки. Доксициклин выделяется преимущественно с желчью. В экскрементах определяется до 90% препарата.
Тетрациклины имеют широкие показания к применению. Они эффективны при риккетсиозах, сыпном тифе, пневмонии, вызванной микоплазмами, при инфицировании хламидиями (пневмонии, пситтакозе, трахоме и др.), при гонорее, сифилисе, возвратном тифе, бруцеллезе, туляремии, холере, при бациллярной и амебной дизентерии, при кокковой инфекции, лептоспирозах и т.д. Тетрациклины используют при развитии устойчивости микроорганизмов к пенициллинам и стрептомицину или при сенсибилизации больного к этим антибиотикам. Назначают их чаще внутрь с интервалом 4-8 ч. Кроме того, их растворимые соли вводят парентерально (внутривенно, внутримышечно, в полости тела). Под мозговые оболочки тетрациклины не инъецируют, так как у них выражено раздражающее действие. Местно их применяют чаще всего в мазях при заболеваниях глаз (особенно при трахоме).
Тетрациклины оказывают ряд неблагоприятных эффектов. Так, они могут вызывать аллергические реакции. При этом поражаются кожные покровы, возможна легкая лихорадка и др. Аллергические реакции на тетрациклины наблюдаются значительно реже, чем на пенициллины и цефалоспорины.
Из побочных эффектов неаллергической природы прежде всего следует отметить раздражающее действие (особенно выражено у окситетрациклина). При приеме препаратов внутрь оно является одной из основных причин диспепсических явлений (тошноты, рвоты, диареи), глоссита, стоматита и других нарушений со стороны слизистой оболочки пищеварительного тракта. Вследствие раздражающего действия внутримышечные инъекции болезненны, внутривенная инфузия может приводить к тромбофлебитам.
Тетрациклины обладают некоторой гепатотоксичностью (главным образом окситетрациклин). С осторожностью нужно назначать тетрациклины во второй половине беременности и детям. Связано это с тем, что тетрациклины депонируются
в костной ткани, в том числе в тканях зубов, и образуют хелатные соединения с солями кальция. При этом формирование скелета нарушается, происходят окрашивание и повреждение зубов.
Одним из нежелательных эффектов тетрациклинов (особенно демеклоциклина) является их способность вызывать фотосенсибилизацию и связанные с ней дерматиты.
Типично для тетрациклинов влияние на обмен веществ. Они угнетают синтез белка (антианаболическое действие), увеличивают выведение из организма ионов натрия, воды, аминокислот, отдельных витаминов и ряда других соединений.
Миноциклин может вызывать вестибулярные расстройства.
Характерным осложнением при лечении тетрациклинами является суперинфекция. Будучи антибиотиками широкого спектра действия, тетрациклины подавляют сапрофитную флору пищеварительного тракта и благоприятствуют развитию кандидамикоза, суперинфекции стафилококками, протеем, синегнойной палочкой. Наибольшие опасения вызывают стафилококковые энтероколит и пневмония, которые могут протекать очень тяжело. Угнетение сапрофитной флоры является одной из причин развития у больных недостаточности витаминов группы В (сапрофиты участвуют в их синтезе), которая отягощает поражение слизистой оболочки пищеварительного тракта, вызываемое раздражающим действием тетрациклинов и суперинфекцией.
Для предупреждения и лечения кандидамикоза тетрациклины сочетают с противогрибковым антибиотиком нистатином. Кроме того, целесообразно одновременно с тетрациклинами назначать витамины группы В. Для подавления суперинфекции стафилококками, протеем или синегнойной палочкой используют противомикробные средства с соответствующим спектром действия.
Изредка может развиваться псевдомембранозный колит, который лечат ванкомицином.
В связи с резистентностью микроорганизмов, развивающейся в отношении известных тетрациклинов, закономерны поиски новых производных этой группы. Одно из последних достижений связано с синтезом глицилциклинов. Перспективным соединением этого ряда является тигилциклин, который проходит клинические испытания.
29.1.6. ГРУППА ЛЕВОМИЦЕТИНА
Антибиотик левомицетин (см. химическую структуру) продуцируется Streptomyces venezuelae. Его получают из культуральной жидкости, а также синтетическим путем.
Левомицетин (хлорамфеникол) обладает широким спектром действия, в который входят грамположительные и грамотрицательные бактерии, в том числе семейство кишечных бактерий, палочки инфлюэнцы, а также риккетсии, хламидии, возбудители бруцеллеза, туляремии. К левомицетину мало или совсем нечувствительны кислотоустойчивые микобактерии, синегнойная палочка, протеи, простейшие.
Механизм противомикробного действия левомицетина связан с его влиянием на рибосомы и угнетением синтеза белка. Он также ингибирует пептидилтрансферазу. Проявляются эти влияния в основном бактериостатическим эффектом. Привыкание микроорганизмов к левомицетину развивается относительно медленно.
Из желудочно-кишечного тракта левомицетин всасывается хорошо. Максимальная концентрация в плазме создается примерно через 2 ч. Для поддержания бактериостатических концентраций в крови левомицетин назначают с интервалом 6 ч. Значительная часть антибиотика связывается с альбуминами плазмы. Левомицетин хорошо проникает в различные ткани, в том числе проходит через гематоэнцефалический барьер. В ликворе концентрация левомицетина в 2 раза меньше, чем в плазме. Основное его количество подвергается в печени химическим превращениям. Образующиеся при этом конъюгаты и около 10% неизмененного препарата выделяются почками.
В связи с серьезными неблагоприятными эффектами в отношении кроветворения (см. ниже) левомицетин, как правило, относят к антибиотикам резерва; применяется он только при неэффективности других антибиотиков (табл. 29.8). Основные показания к его назначению: брюшной тиф, пищевые токсикоинфекции (сальмонеллезы) и риккетсиозы. Иногда его используют при заболеваниях, вызванных палочкой инфлюэнцы (например, при менингите, при инфицировании мочевыводящих путей), при бруцеллезе и ряде других инфекций.
Принимают левомицетин обычно внутрь. Растворы и линимент левомицетина используют местно. Для парентерального введения выпускают левомицетина сукцинат растворимый (хлороцид С). Вводят его подкожно, внутримышечно и внутривенно.
| Таблица 29.8. Некоторые показания к применению ряда основных и резервных антибиотиков | ||
| Инфекции | Основные антибиотики | Резервные антибиотики |
| Стафилококковые (чувствительные к бензилпенициллину) | Бензилпенициллин Феноксиметилпенициллин | Цефалоспорины Макролиды Ванкомицин Имипенем |
| Стафилококковые (устойчивые к бензилпенициллину) | Оксациллин Ванкомицин Амоксициллин | Цефалоспорины Макролиды |
| Стрептококковые | Бензилпенициллин Ампициллин Аминогликозиды | Цефалоспорины Макролиды Тетрациклины |
| Пневмококковые | Бензилпенициллин Ампициллин Ванкомицин | Цефалоспорины Макролиды |
| Энтерококковые | Ампициллин Бензилпенициллин+гентамицин | Аминогликозиды Ванкомицин |
| Гонорея | Амоксициллин Бензилпенициллин Ампициллин Цефтриаксон | Цефалоспорины |
| Менингококковые | Бензилпенициллин Ампициллин | Левомицетин Цефалоспорины |
| Газовая гангрена | Бензилпенициллин | Тетрациклины Левомицетин Цефалоспорины Клиндамицин |
| Столбняк | Бензилпенициллин | Тетрациклины Цефалоспорины Клиндамицин |
| Дифтерия | Макролиды Бензилпенициллин | Амоксициллин Клиндамицин |
| Инфекции, вызываемые протеем: Proteus mirabilis Proteus vulgaris Proteus rettgeri Proteus morganii | Ампициллин Цефалоспорины Канамицин Гентамицин Амикацин Карбенициллин | Левомицетин Гентамицин Левомицетин Цефалоспорины Имипенем |
| Инфекции, вызываемые кишечной палочкой | Ампициллин Цефалоспорины III Аминогликозиды | Тикарциллин Азлоциллин Ципрофлоксацин1 |
| Брюшной тиф | Ципрофлоксацин1 | Левомицетин Ампициллин Тетрациклин |
| Бактериальная дизентерия | Ципрофлоксацин1 | Ампициллин Левомицетин Тетрациклин |
| Бруцеллез | Тетрациклины + стрептомицин | Рифампицин Левомицетин Стрептомицин |
| Туляремия | Тетрациклины | Левомицетин Аминогликозиды |
| Инфекции, вызываемые синегнойной палочкой | Аминогликозиды Карбоксипенициллины Уреидопенициллины | Азтреонам Имипенем Цефтазидим Цефоперазон |
| Холера | Тетрациклины | Левомицетин Ципрофлоксацин1 |
| Чума | Стрептомицин + Тетрациклины | Тетрациклины Левомицетин Аминогликозиды |
| Риккетсиозы | Тетрациклины | Левомицетин |
| Сифилис | Бензилпенициллин | Макролиды Тетрациклины |
Как уже отмечалось, левомицетин может вызывать выраженное угнетение кроветворения, сопровождающееся ретикулоцитопенией, гранулоцитопенией и в тяжелых случаях апластической анемией, которая обычно заканчивается смертельным исходом. Поэтому при применении левомицетина требуется регулярный контроль картины крови. Чтобы уменьшить возможность угнетения кроветворения, антибиотик следует назначать в течение возможно более короткого периода времени. Повторные курсы лечения не рекомендуются.
В ряде случаев отмечаются аллергические реакции в виде кожных высыпаний, лихорадки и др.
Из побочных эффектов неаллергической природы наиболее часто возникает раздражение слизистых оболочек (тошнота, диарея), в том числе аноректальный синдром (с соответствующей локализацией раздражения). Поражаются также кожные покровы (сыпь, дерматит). Иногда отмечаются психомоторные нарушения, угнетающее влияние на миокард.
Тяжелая интоксикация с сердечно-сосудистым коллапсом нередко возникает у новорожденных и на 1-м месяце жизни. Связано это с медленным выведением антибиотика почками и недостаточностью ферментов печени у детей в этот период.
При применении левомицетина может развиться суперинфекция (например, кандидамикоз, инфекция стафилококками, протеем).
29.1.7. ГРУППА АМИНОГЛИКОЗИДОВ
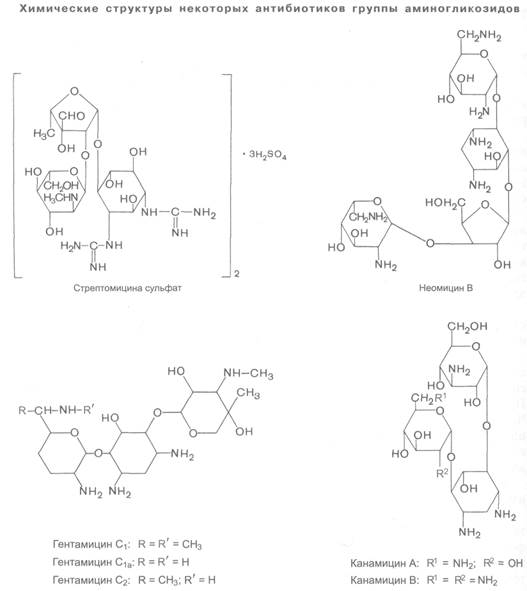
Основными представителями этой группы антибиотиков являются стрептомицин, неомицин, канамицин, гентамицин, амикацин, тобрамицин, сизомицин, мономицин и др. (см. также главу 29.5).
Механизм действия аминогликозидов связывают с непосредственным их влиянием на рибосомы и угнетением синтеза белка. Для аминогликозидов характерен бактерицидный эффект.
Стрептомицин является антибиотиком, продуцируемым Actinomyces globisporus streptomycini. Основным препаратом, применяемым в медицинской практике, является стрептомицина сульфат (см. химическую структуру). Активность стрептомицина определяется в единицах действия (ЕД) и в весовых единицах. 1 ЕД стрептомицина основания соответствует 1 мкг.
Стрептомицин имеет широкий спектр противомикробного действия. Наиболее важно его угнетающее влияние на микобактерии туберкулеза, возбудители туляремии, чумы. Кроме того, он губительно действует на патогенные кокки, некоторые штаммы протея, синегнойную палочку, бруцеллы и другие грамотрицательные и грамположительные бактерии. К стрептомицину нечувствительны анаэробы, спирохеты, риккетсии, вирусы, патогенные грибы, простейшие.
К этому антибиотику относительно быстро развивается привыкание. В ряде случаев наблюдается образование стрептомицинозависимых штаммов, для роста и размножения которых необходим стрептомицин.
Из желудочно-кишечного тракта препарат всасывается плохо. При внутримышечном введении через 1-2 ч стрептомицин накапливается в плазме крови в максимальных концентрациях. Распределяется он в основном экстрацеллюлярно. Проникает в полости брюшины и плевры, при беременности — в ткани плода. Через гематоэнцефалический барьер, как правило, не проходит; при менингите проницаемость гематоэнцефалического барьера для стрептомицина увеличивается. Снижение концентрации стрептомицина в плазме крови на 50% происходит через 2-4 ч.
Выводится стрептомицин большей частью почками (путем фильтрации) в неизмененном виде. Незначительная часть выделяется с желчью в кишечник.
Применяют стрептомицина сульфат главным образом при лечении туберкулеза. Кроме того, его используют при лечении туляремии, чумы, бруцеллеза, инфекций мочевыводящих путей, органов дыхания, а также при других заболеваниях. Вводят препарат чаще внутримышечно (1—2 раза в сутки), а также в полости тела. С целью воздействия на кишечную флору стрептомицина сульфат назначают внутрь. Для инъекции под оболочки мозга при менингите используют только стрептомицин-хлоркалъциевый комплекс (двойная соль стрептомицина гидрохлорида и кальция хлорида). Последний оказывает меньшее раздражающее действие, чем другие препараты стрептомицина. Однако токсичность стрептомицин-хлоркальциевого комплекса значительная, поэтому применяют его лишь в случае крайней необходимости.
Отрицательные эффекты стрептомицина включают неаллергические и аллергические влияния. Наиболее серьезным является ототоксическое его действие. Чаще всего поражается вестибулярная ветвь VIII пары черепных нервов, реже — слуховая ветвь. По мнению ряда авторов, назначение кальция пантотената уменьшает возможность возникновения указанных побочных эффектов. Стрептомицин
оказывает угнетающее влияние на нервно-мышечные синапсы, что может быть причиной угнетения дыхания. Кроме того, он обладает раздражающим эффектом, в связи с чем инъекции его болезненны.
При назначении препаратов стрептомицина отмечаются и аллергические реакции (лихорадка, кожные поражения, эозинофилия, редко анафилактический шок и др.). На фоне действия стрептомицина возможно развитие суперинфекции.
Неомицин представляет собой смесь антибиотиков неомицинов А, В и С, продуцируемых Actinomyces fradiae. Выпускается в виде препарата неомицина сульфата. Обладает широким спектром действия. К нему чувствительны как грамположительные, так и грамотрицательные микроорганизмы. На анаэробы, спирохеты, патогенные грибы и вирусы влияния не оказывает. Устойчивость микроорганизмов к неомицину развивается относительно медленно.
При приеме внутрь препарат всасывается плохо, поэтому его действие при таком пути введения ограничивается в основном пищеварительным трактом. Неомицин используют для лечения энтерита, вызванного чувствительными к нему микроорганизмами. Рационально его применение при резистентности соответствующих возбудителей к другим антибиотикам. Неомицин может быть полезен при подготовке больных к операции на пищеварительном тракте (с целью частичной «стерилизации» кишечника). Положительным качеством является его высокая активность в отношении кишечной палочки, некоторых штаммов протея и синегнойной палочки. Из побочных эффектов возможны диспепсические нарушения, аллергические реакции, кандидамикоз.
Нередко неомицин применяют местно. Его назначают при лечении инфицированных ран, ряда кожных заболеваний (пиодермии и др.), заболеваний глаз (например, конъюнктивита) и т.д. С неповрежденной кожной поверхности и слизистых оболочек всасывается незначительно. Наружно неомицин в ряде случаев используют совместно с глюкокортикоидами (например, с синафланом или флуметазона пивалатом). При этом противомикробный эффект сочетается с противовоспалительным.
Парентерально неомицин не используют в связи с его высокой токсичностью в отношении почек (появляется белок в моче) и слухового нерва (возникают шум в ушах и снижение слуха вплоть до полной глухоты). Кроме того, неомицин обладает курареподобной активностью (может вызывать угнетение и остановку дыхания).
Препарат противопоказан при заболеваниях почек и слухового нерва.
Гентамицин продуцируется Micromonospora purpurea и М. echinospora. Выпускается в виде гентамицина сульфата (гарамицин).
Обладает широким спектром действия, включающим грамположительные и грамотрицательные бактерии. Наибольший практический интерес представляет его активность в отношении синегнойной палочки, протея, кишечной палочки, а также стафилококков, устойчивых к бензилпенициллину. Устойчивость к гентамицину развивается медленно.
Из желудочно-кишечного тракта препарат всасывается недостаточно полно, поэтому для системного действия его назначают внутримышечно. Максимальные количества гентамицина в плазме крови при этом пути введения накапливаются через 60 мин. Противомикробные концентрации сохраняются в организме в течение 8-12 ч. Через гематоэнцефалический барьер в обычных условиях гентамицин почти не проникает. При менингите в ликворе обнаруживаются небольшие его концентрации. Выделяется почками преимущественно в неизмененном виде.
Применяют гентамицин главным образом для лечения заболеваний, вызванных грамотрицательными бактериями. Особенно ценен препарат при инфекции мочевыводящих путей (пиелонефрите, цистите), сепсисе, раневой инфекции, ожогах. Пути введения: внутримышечно или наружно.
Гентамицин менее токсичен, чем неомицин. Однако основные неблагоприятные эффекты, типичные для аминогликозидов, наблюдаются и при использовании гентамицина. Одним из них является ототоксическое действие. В основном гентамицин поражает вестибулярную ветвь VIII пары черепных нервов. Слух страдает реже. Нефротоксичность также выражена в меньшей степени, чем у неомицина. Обладает курареподобными свойствами.
Группу аминогликозидов представляет также тобрамицин (бруламицин). Продуцируется Str. tenebmrius. Обладает широким спектром действия. Высокоактивен в отношении синегнойной палочки. Эффективные противомикробные концентрации после однократного введения сохраняются в течение 6-8 ч. Вводят препарат внутримышечно и внутривенно. Выделяется он преимущественно почками. Показания к применению аналогичны таковым для гентамицина и определяются спектром противомикробного действия. Обладает нефро- и ототоксичностью, но менее выраженной, чем у гентамицина.
К аминогликозидам относится также антибиотик сизомицин. Продуцируется Micromonospora inyoensis. Обладает широким спектром противомикробного действия, подобным таковому гентамицина. Активнее последнего в отношении разных видов протея, синегнойной палочки, клебсиелл, энтеробактера.
Устойчивость к сизомицину развивается медленно. Возникает также перекрестная устойчивость ко всем аминогликозидам.
Из пищеварительного тракта препарат всасывается плохо, поэтому его вводят внутримышечно и внутривенно. Около 25% связывается с белками плазмы крови. Периодичность введения в клинических условиях 8 ч.
Показания к применению и побочные эффекты аналогичны таковым для гентамицина.
К числу наиболее эффективных аминогликозидов относится амикацин (амикин). Он является производным канамицина. Из всех аминогликозидов обладает наиболее широким спектром противомикробного действия, включающим аэробные грамотрицательные бактерии (в том числе синегнойную палочку, протей, клебсиеллы, кишечную палочку и др.) и микобактерии туберкулеза. На большинство грамположительных анаэробных бактерий не влияет. Устойчив к действию ферментов, инактивирующих аминогликозиды. Обладает ототоксичностью и нефротоксичностью. Вводят амикацин внутримышечно и внутривенно.
29.1.8. ЦИКЛИЧЕСКИЕ ПОЛИПЕПТИДЫ (ПОЛИМИКСИНЫ)
Полимиксины в химическом отношении представляют собой группу циклических полипептидов. В нашей стране используется полимиксин М (в виде сульфата), продуцируемый Вас. polymyxa Ross.
У полимиксина М сульфата противомикробное действие выражено преимущественно в отношении грамотрицательных бактерий: синегнойной палочки, семейства кишечных бактерий (кишечной палочки, шигелл, сальмонелл), а также капсульных бактерий, пастерелл и бруцелл, палочек инфлюэнцы. К полимиксину М устойчивы патогенные кокки, протей, патогенные анаэробы, кислотоустойчивые микобактерии, палочка дифтерии и некоторые другие возбудители.
Механизм противомикробного действия связан с повреждающим влиянием полимиксина М на цитоплазматическую мембрану. Нарушая ее проницаемость, полимиксин М способствует выведению многих компонентов цитоплазмы в окружающую среду. Происходит лизис микроорганизмов. Бактерицидный эффект наблюдается как в состоянии покоя, так и в процессе роста и размножения бактерий. Действует полимиксин М только на внеклеточно расположенные микроорганизмы.
Устойчивость к полимиксину М развивается медленно, что является несомненным достоинством препарата.
Назначают полимиксина М сульфат внутрь (в кишечнике накапливаются высокие концентрации препарата, так как из желудочно-кишечного тракта он всасывается плохо) и местно. Парентерально его не применяют, так как при таком пути введения он вызывает тяжелые нейро- и нефротоксические нарушения. Энтерально препарат используют при энтероколите, вызванном синегнойной палочкой, кишечной палочкой, шигеллами, а также для санации кишечника перед операциями. Местно полимиксина М сульфат эффективен при лечении гнойных процессов, вызванных чувствительными к нему возбудителями (главным образом грамотрицательными микроорганизмами, включая синегнойную палочку).
Побочные эффекты при энтеральном и местном применении полимиксина М сульфата возникают редко. При приеме внутрь возможны диспепсические явления, связанные с некоторым раздражающим действием препарата. Иногда возникает суперинфекция. Аллергических реакций практически не наблюдается.
Противопоказанием к назначению полимиксина М сульфата являются заболевания почек.
Учитывая выраженную нефротоксичность этого антибиотика, даже в случае применения его внутрь или местно необходимо систематически контролировать функцию почек.
29.1.9. ЛИНКОЗАМИДЫ
К этой группе относится клиндамицин. Он является ингибитором синтеза белка бактерий и обычно действует бактериостатически. Активен главным образом в отношении анаэробов (Bacteroides fragilis и др.), стрептококков и стафилококков. Хорошо всасывается из кишечника. Через гематоэнцефалический барьер проникает плохо. Метаболизируются в печени. Выделяется почками и с желчью.
Применяется при инфекциях, вызванных бактероидами, особенно при поражении Bacteroides fragilis брюшной полости.
Наиболее опасный побочный эффект — псевдомембранозный колит (развиваются диарея со слизистыми и кровянистыми выделениями, боли в области живота, лихорадка). Это одно из проявлений дисбактериоза, связанного с действием токсина Clostridium difficile, которые могут находиться в кишечнике. Лечат это осложнение ванкомицином и метронидазолом. Редко отмечаются аллергические реакции, поражение печени, лейкопения.
29.1.10. ГЛИКОПЕПТИДЫ
Основным препаратом этой группы является ванкомицин, являющийся сложным гликопептидом. Он продуцируется актиномицетами Streptomyces orientalis. Нарушает синтез клеточной стенки бактерий и действует бактерицидно. Обладает высокой активностью в отношении грамположительных кокков, включая стафилококки, устойчивые к метициллину, и штаммы, продуцирующие β-лактамазы; действует на клостридии, в том числе на Clostridium difficile, а также на коринебактерии. Из пищеварительного тракта всасывается плохо. Если требуется системное действие, препарат вводят внутривенно. Он проходит через гематоэнцефалический барьер, особенно при менингите.
Применяют ванкомицин при инфекциях, вызванных грамположительными кокками, устойчивыми к пенициллину, при энтероколитах, в том числе при псевдомембранозном колите.
Препарат токсичен, что ограничивает его применение. Он обладает ототоксичностью и нефротоксичностью, может вызывать флебиты. Редко возникают аллергические реакции, нейтропения, тромбоцитопения.
К этой же группе относится антибиотик тейкопланин.
29.1.11. ФУЗИДИЕВАЯ КИСЛОТА
Это антибиотик с узким спектром действия. Применяется в виде натриевой соли. В основном влияет на грамположительные бактерии. Угнетает синтез белка бактерий. Действует бактериостатически. Хорошо всасывается при энтеральном введении. В значительных количествах накапливается в костной ткани. Метаболизируется в печени. Выделяется с желчью. Применяется при стафилококковых инфекциях, устойчивых к действию пенициллина, особенно при остеомиелите. Побочные эффекты: диспепсические явления, кожная сыпь, желтуха.
29.1.12. АНТИБИОТИКИ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ
Для местного воздействия предложен антибиотик фюзафюнжин (биопарокс), обладающий противомикробным и противовоспалительным эффектами. Продуцируется специальным штаммом грибов Fusarium lateritium WR. По химическому строению относится к пептидам. Выпускают препарат в виде аэрозоли для ингаляций. Он эффективен в отношении многих кокков, некоторых анаэробов, микоплазм, грибов рода Candida. Рекомендован для применения при инфекциях носоглотки и дыхательных путей. Из побочных эффектов иногда отмечается раздражающее действие.
Для местного применения предложен также антибиотик мупироцин (бактробан). Продуцируется он Pseudomonas fluorescens. Ингибирует синтез белка. В низких концентрациях оказывает бактериостатическое, а в высоких — бактерицидное действие. В незначительной степени всасывается с неповрежденной кожи (0,25-0,3%). Применяется накожно или интраназально в виде мази при поражении кожи и слизистой оболочки носовых ходов стафилококками (в том числе устойчивыми к метициллину) и β-гемолитическими стрептококками.
| Препараты | ||
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Бензилпенициллина натриевая соль — Benzylpenicillinum-natrium | Внутримышечно 250 000-500 000 ЕД; внутривенно медленно 1 000 000— 2 000 000 ЕД, капельно 2 000 000-5 000 000 ЕД; эндолюмбально 5000-10 000 ЕД; ингаляционно 100 000-300 000 ЕД; в виде глазных капель, а также капель в нос и в ухо растворы, содержащие в 1 мл 10 000-100 000 ЕД; в полости растворы, содержащие в 1 мл 20 000 ЕД | Флаконы по 250 000; 500 000 и 1 000 000 ЕД |
| Бензилпенициллина калиевая соль — Benzylpenicillinum-kalium | Внутримышечно 250 000-500 000 ЕД; местно в растворах, содержащих в 1 мл 10 000-100 000 ЕД | Флаконы по 250 000; 500 000 и 1 000 000 ЕД |
| Бензилпенициллина новокаиновая соль — Benzylpenicillinum-novocainum | Внутримышечно 300 000 ЕД | Флаконы по 300 000; 600 000 и 1 200 000 ЕД |
| Бициллин-1 — Bicillinum-1 | Внутримышечно 300 000-600 000 ЕД 1 раз в неделю или 1 200 000-2 400 000 ЕД 1 раз в 2 нед | Флаконы по 300 000; 600 000; 1 200 000 и 2 400 000 ЕД |
| Бициллин-5 — Bicillinum-5 | Внутримышечно 1 500 000 ЕД 1 раз в 4 нед | Флаконы по 1 500 000 ЕД |
| Феноксиметилпенициллин — Phenoxymethyl-penicillinum | Внутрь 0,25 г | Таблетки по 0,1 и 0,25 г; драже по 0,1 г |
| Оксациллина натриевая соль — Oxacillinum-natrium | Внутрь, внутримышечно и внутривенно 0,25—0,5 г | Таблетки по 0,25 и 0,5 г; капсулы по 0,25 г; флаконы по 0,25 и 0,5 г |
| Ампициллин — Ampicillinum | Внутрь 0,5 г | Таблетки и капсулы по 0,25 г |
| Карбенициллина динатриевая соль — Саrbenicillinum-dinatricum | Внутримышечно 1 — 1,5 г; внутривенно 4—5 г | Флаконы по 1 г |
| Азлоциллин — Azlocillin | Внутримышечно и внутривенно по 5 г | Флаконы, содержащие порошок для внутримышечного введения, по 0,5; 1 и 2 г; для внутривенного введения по 4; 5 и 10 г |
| Цефалотина натриевая соль — Cefalotinum-natrium | Внутримышечно и внутривенно 4— 5г | Флаконы по 1 г |
| Цефалексин — Cefalexinum | Внутрь 0,25-0,5 г | Капсулы по 0,25 г; таблетки по 0,5 г |
| Цефаклор — Cefaclor | Внутрь по 0,25 г | Капсулы по 0,25 и 0,5 г |
| Цефотаксим — Cefotaxim | Внутримышечно и внутривенно по 0,5-1 г | Флаконы по 0,5; 1 и 2 г |
| Цефокситин — Cefoxitin | Внутривенно и внутримышечно по 1-2 г | Лиофилизированный порошок во флаконах по 1 и 2 г |
| Эритромицин — Erythromycinum | Внутрь 0, 1—0,25 г; наружно в полость конъюнктивы 1% мазь | Таблетки по 0,1 и 0,25 г; мазь, содержащая 0,01 г препарата в 1 г |
| Олеандомицин — Oleandomycinum | Внутрь 0,25 г | Таблетки, покрытые оболочкой, по 0,125 г |
| Рокситромицин — Roxithromycin | Внутрь 0,15 г | Таблетки по 0,15 г |
| Азитромицин — Azithromycin | Внутрь 0,25-0,5 г | Капсулы по 0,125 и 0,25 г; таблетки по 0,5 г |
| Имипенем — Imipenem | Внутривенно 2 г | |
| Азтреонам — Aztreonam | Внутривенно и внутримышечно по 0,5-1 и 2 г | Флаконы по 0,5 и 1 г |
| Тетрациклин — Tetracyclinum | Внутрь 0,2—0,25 г; в полость конъюнктивы 1% мазь | Таблетки, покрытые оболочкой, по 0,05; 0,1 и 0,25 г; глазная мазь, содержащая 0,01 г препарата в 1 г |
| Метациклина гидрохлорид — Methacyclini hydrochloridum | Внутрь 0,3 г | Капсулы по 0,15 и 0,3 г |
| Левомицетин — Laevomycetinum | Внутрь 0,25-0,5 г; наружно 1-10% линимент; в полость конъюнктивы 0,25% раствор и 1% линимент | Таблетки по 0,25 и 0,5 г; двухслойные таблетки продленного действия по 0,65 г; капсулы по 0,1; 0,25 и 0,5 г; 0,25% раствор во флаконах по 10 мл (глазные капли) |
| Синтомицин — Synthomycinum | Наружно 1 — 10% линимент; интравагинально 0,25 г | 1—5% и 10% линимент; суппозитории вагинальные по 0,25 г |
| Стрептомицина сульфат — Streptomycini sulfas | Внутримышечно 0,5 г | Флаконы по 0,25; 0,5 и 1 г |
| Неомицина сульфат — Neomycini sulfas | Внутрь 0,1—0,2 г; наружно 0,5% раствор; 0,5% и 2% мазь | Таблетки по 0,1 и 0,25 г; флаконы по 0,5 г; 0,5% и 2% мазь (в тубах по 15 и 30 г) |
| Амикацина сульфат — Amicacini sulfas | Внутримышечно и внутривенно 0,5 г | Флаконы по 0,1; 0,25 и 0,5 г |
| Гентамицина сульфат— Gentamycini sulfas | Внутримышечно и внутривенно 0,0004 г/кг; накожно мазь или крем 0,1%; в глаз 0,3% раствор | Порошок по 0,08 г во флаконах; в ампулах 4% раствор по 1—2 мл; 0,1% мазь в тубах по 10 и 15 г; 0,3% раствор (глазные капли) |
| Полимиксина М сульфат — Polymyxini M sulfas | Внутрь 500 000 ЕД; наружно линимент, содержащий 10 000 ЕД в 1 г; раствор, содержащий 10 000-20 000 ЕД в 1 мл | Флаконы по 500 000 и 1 000 000 ЕД; таблетки по 500 000 ЕД; линимент в тубах по 30 г, содержащий 10 000 ЕД полимиксина в 1 г |
29.2. СУЛЬФАНИЛАМИДНЫЕ ПРЕПАРАТЫ
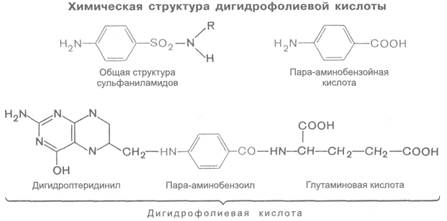
Сульфаниламиды были первыми химиотерапевтическими антибактериальными средствами широкого спектра действия, которые нашли применение в практической медицине. Химически они являются производными сульфаниламида (амида сульфаниловой кислоты).
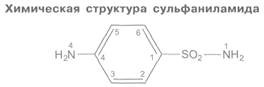
Создание наиболее эффективных, продолжительно действующих и менее токсичных сульфаниламидов основано на замещении атома водорода в амидной группе (у N1). Наличие свободной аминогруппы (—N4H2) в пара-положении обязательно для противомикробного действия. В связи с этим к замещению атомов водорода у N4 прибегают крайне редко; это допускается только в том случае, если в организме радикал отщепляется и аминогруппа высвобождается (например, у фталазола). Введение дополнительных радикалов в бензольный цикл снижает активность соединений.
Сульфаниламиды могут быть представлены следующими группами.
Препараты, применяемые для резорбтивного действия (хорошо всасывающиеся из желудочно-кишечного тракта)
 A. Непродолжительного действия
A. Непродолжительного действия
Сульфадимезин
Этазол
Сульфазин
Уросульфан
Б. Длительного действия
Сульфапиридазин
Сульфадиметоксин
B. Сверхдлительного действия
Сульфален
Препараты, действующие в просвете кишечника (плохо всасывающиеся из желудочно-кишечного тракта)
Фталазол
Препараты для местного применения
Сульфацил-натрий
Сульфазина серебряная соль
Спектр действия сульфаниламидов довольно широк. Он включает в основном следующие возбудители инфекций:
а) бактерии — патогенные кокки (грамположительные и грамотрицательные), кишечная палочка, возбудители дизентерии (шигеллы), холерный вибрион, возбудители газовой гангрены (клостридии), возбудители сибирской язвы, дифтерии, катаральной пневмонии, инфлюэнцы;
б) хламидии — возбудители трахомы, орнитоза, паховой лимфогранулемы;
в) актиномицеты;
г) простейшие — возбудитель токсоплазмоза, плазмодии малярии.
Особенно активны сульфаниламиды в отношении пневмококков, менингококков, гонококков, некоторых типов гемолитических стрептококков, а также возбудителей бактериальной дизентерии.
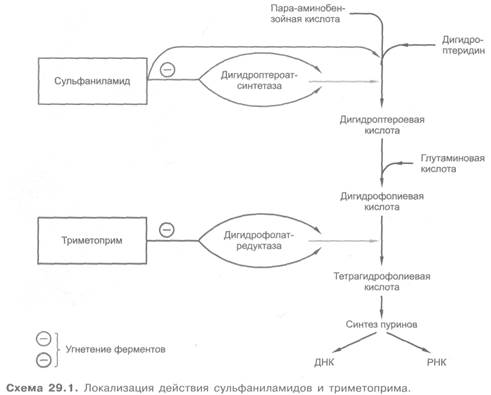
Механизм противомикробного действия сульфаниламидов связан с их конкурентным антагонизмом с пара-аминобензойной кислотой. Последняя включается в структуру дигидрофолиевой кислоты, которую синтезируют многие микроорганизмы. В тканях человека этого не происходит, так как эти ткани утилизируют уже готовую дигидрофолиевую кислоту, чем, по-видимому, и объясняется избирательность противомикробного действия сульфаниламидов. Благодаря химическому сходству с пара-аминобензойной кислотой сульфаниламиды препятствуют ее включению в дигидрофолиевую кислоту. Кроме того, они конкурентно угнетают дигидроптероатсинтетазу. Нарушение синтеза дигидрофолиевой кислоты уменьшает образование из нее тетрагидрофолиевой кислоты, которая необходима для синтеза пуриновых и пиримидиновых оснований (схема 29.1). В результате угнетается синтез нуклеиновых кислот, вследствие чего рост и размножение микроорганизмов подавляются (бактериостатический эффект). При длительном применении сульфаниламидов к ним постепенно развивается устойчивость микроорганизмов. Высказывается предположение, что это может быть связано с повышением интенсивности синтеза микроорганизмами дигидрофолиевой кислоты. Следует учитывать, что устойчивость возникает ко всем сульфаниламидам (т.е. перекрестная устойчивость).
29.2.1. СУЛЬФАНИЛАМИДЫ ДЛЯ РЕЗОРБТИВНОГО ДЕЙСТВИЯ
Препараты этой группы быстро и полно всасываются из желудочно-кишечного тракта. Сульфаниламиды частично связываются с альбуминами плазмы. Распределяются по всем тканям, в том числе проходят через гематоэнцефалический барьер, плаценту, накапливаются в серозных полостях тела. Основной путь превращения сульфаниламидов в организме — ацетилирование (по N4), которое происходит в печени. Образующиеся при этом соединения лишены антибактериальной активности. Некоторые ацетилированные производные хуже растворяются, чем исходные сульфаниламиды, и могут быть причиной образования в моче кристаллов (кристаллурии). Степень ацетилирования разных препаратов неодинакова. Меньше всего ацетилируются уросульфан, сульфацил-натрий, этазол. Выделяются сульфаниламиды и их метаболиты главным образом почками путем фильтрации. Часть сульфаниламидов подвергается реабсорбции. Небольшие количества веществ выводятся кишечником, потовыми и слюнными железами.
Сульфаниламиды, предназначенные для резорбтивного действия, различаются преимущественно по длительности антибактериального эффекта. Препараты непродолжительного действия хорошо всасываются и относительно быстро выделяются. При их энтеральном введении максимальные концентрации в плазме создаются через 2-3 ч. Для поддержания бактериостатических концентраций их назначают через 4-6 ч.
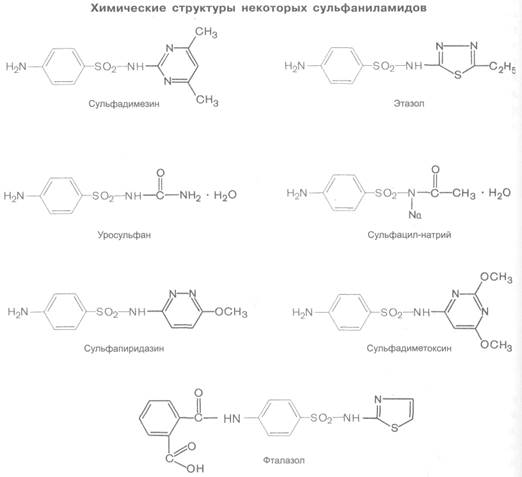
Из сульфаниламидов непродолжительного действия наиболее часто используют сульфадимезин (сульфаметазин), этазол (сульфаэтилтиадиазол), сульфазин (сульфадиазин), уросульфан (сульфакарбамид). К этой же группе относится стрептоцид (стрептоцид белый, сульфаниламид). Однако в настоящее время стрептоцид практически не применяют, так как он менее активен и чаще, чем другие сульфаниламиды, вызывает побочные эффекты.
К препаратам длительного действия относятся сульфапиридазин (сульфаметоксипиридазин, спофадазин) и сульфадиметоксин (мадрибон, мадроксин). Они хорошо всасываются из желудочно-кишечного тракта, но медленно выводятся. Максимальные концентрации их в плазме крови определяются через 3-6 ч.
Длительное сохранение в организме бактериостатических концентраций препаратов, по-видимому, зависит от их эффективной реабсорбции в почках. Может иметь значение и выраженная степень связывания с белками плазмы крови (например, для сульфапиридазина она соответствует примерно 85%).
Таким образом, при использовании препаратов длительного действия в организме создаются стабильные концентрации вещества. Это является несомненным преимуществом препаратов при антибактериальной терапии. Однако если возникают побочные явления, продолжительный эффект играет отрицательную роль, так как при вынужденной отмене вещества должно пройти несколько дней, прежде чем закончится его действие.
Следует учитывать также, что концентрация сулфапиридазина и сульфадиметоксина в спинномозговой жидкости невелика (5-10% от концентрации в плазме крови). Этим они отличаются от сульфаниламидов непродолжительного действия, которые накапливаются в ликворе в довольно больших количествах (50-80% от концентрации в плазме).
Назначают сульфапиридазин и сульфадиметоксин 1-2 раза в сутки.
Препаратом сверхдлительного действия является сульфален (келфизин, сульфаметоксипиразин), который в бактериостатических концентрациях задерживается в организме до 1 нед.
По противомикробной активности сульфаниламиды значительно уступают антибиотикам, поэтому сфера их применения довольно ограничена. Их назначают главным образом при непереносимости антибиотиков или развитии привыкания к ним. Нередко сульфаниламиды комибинируют с некоторыми антибиотиками.
Сульфаниламиды для резорбтивного действия применяют при кокковых инфекциях, особенно при менингококковом менингите, заболеваниях органов дыхания, при инфекции мочевыводящих и желчевыводящих путей и др.
Для лечения инфекций мочевых путей (при пиелонефрите, пиелите, цистите) особенно показан уросульфан, который быстро выделяется почками, преимущественно в неизмененном виде (т.е. в активной форме), при этом в моче создаются высокие его концентрации. Отрицательного влияния на функцию почек уросульфан практически не оказывает.
Препараты длительного действия наиболее целесообразно использовать при хронических инфекциях и для профилактики инфекций (например, в послеоперационном периоде).
При резорбтивном действии сульфаниламиды вызывают много побочных эффектов. При их применении могут наблюдаться диспепсические явления (тошнота, рвота), головная боль, слабость, нарушения со стороны ЦНС, поражения системы крови (гемолитическая анемия, тромбоцитопения, метгемоглобинообразование). Возможна кристаллурия. Вероятность выпадения кристаллов в почках можно уменьшить путем введения больших объемов жидкостей, особенно щелочных (так как кислая среда благоприятствует выпадению в осадок сульфаниламидов и их ацетилированных производных).
Аллергические реакции относительно редки, но тем не менее они иногда возникают и выраженность их может быть различной. Наблюдаются кожная сыпь, лихорадка, иногда гепатит, агранулоцитоз, апластическая анемия. Наличие в анамнезе аллергических реакций на сульфаниламиды является противопоказанием к их повторному применению.
29.2.2. СУЛЬФАНИЛАМИДЫ, ДЕЙСТВУЮЩИЕ В ПРОСВЕТЕ КИШЕЧНИКА
Основным отличием этих препаратов является их плохая всасываемость из желудочно-кишечного тракта, поэтому в просвете кишечника создаются высокие их концентрации. Наиболее часто используют фталазол (фталилсульфатиазол, талисульфазол). Из кишечника препарат всасывается в незначительной степени. В моче обнаруживается лишь 5% от введенного вещества. Противомикробное действие фталазола развивается после отщепления фталевой кислоты (от N4) и высвобождения аминогруппы. В итоге действует выделяющийся при этом норсульфазол.
Применяют фталазол при лечении кишечных инфекций — бациллярной дизентерии, энтероколита, колита, для профилактики кишечной инфекции в послеоперационном периоде. Учитывая, что микроорганизмы при этих заболеваниях локализуются не только в просвете, но и в стенке кишечника, фталазол целесообразно сочетать с хорошо всасывающимися сульфаниламидами (сульфадимезином, этазолом и др.). Часто фталазол комбинируют с антибиотиками (например, с тетрациклинами). Принимают его через каждые 4-6 ч. Переносится фталазол хорошо. Токсичность у него низкая. Применение фталазола желательно сочетать с витаминами группы В. Это целесообразно в связи с подавлением фталазолом роста и размножения кишечной палочки, участвующей в синтезе этих витаминов.
Для лечения кишечных инфекций используют и ряд других плохо всасывающихся препаратов — сульгин (сульфагуанидин), фтазин.
29.2.3. СУЛЬФАНИЛАМИДЫ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ
Местно сульфаниламиды применяют для лечения и профилактики инфекций глаз. С этой целью чаще всего используют растворимый в воде сульфацил-натрий. Он достаточно эффективен и не оказывает раздражающего действия. Его применяют для лечения и профилактики гонорейного поражения глаз у новорожденных и взрослых, при конъюнктивите, блефарите, язвах роговицы и др.
Сульфаниламиды могут быть использованы при раневой инфекции (обычно путем припудривания ран). При этом следует учитывать, что в присутствии гноя, раневого отделяемого, некротических масс, содержащих большие количества пара-аминобензойной кислоты, сульфаниламиды мало или совсем неэффективны. Их следует применять только после первичной обработки раны или в условиях «чистой» раны.
Синтезирована сульфазина серебряная соль (сульфаргин), имеющая в своей молекуле атом серебра. Препарат применяется только местно при ожоговых ранах. Высвобождающееся из препарата серебро усиливает противомикробное действие сульфазина и способствует заживлению ран. Входит в состав мази «Сульфаргин».
29.2.4. КОМБИНИРОВАННЫЕ ПРЕПАРАТЫ СУЛЬФАНИЛАМИДОВ С ТРИМЕТОПРИМОМ
Представляет интерес сочетание сульфаниламидов с препаратами, которые, угнетая дигидрофолатредуктазу, блокируют переход дигидрофолиевой кислоты в тетрагидрофолиевую. К таким веществам относится триметоприм.
Угнетающее действие подобной комбинации, проявляющееся на двух разных этапах биосинтеза прекурзоров нуклеиновых кислот, существенно повышает противомикробную активность — эффект становится бактерицидным.
Направленность действия сульфаниламидов и триметоприма см. на схеме 29.1.
Выпускается препарат бактрим (бисептол, котримоксазол, септрин), содержащий триметоприм и сульфаметоксазол. Он обладает высокой антибактериальной активностью. Оказывает бактерицидное действие. Хорошо всасывается из желудочно-кишечного тракта. Максимальная концентрация в плазме крови определяется через 3 ч. Продолжительность эффекта 6-8 ч. Выделяются оба компонента бактрима в основном почками. При использовании бактрима наблюдаются различные побочные эффекты. Наиболее часты диспепсические явления (тошнота, рвота, анорексия, диарея) и аллергические реакции со стороны кожи (эритематозная сыпь, крапивница, зуд). Возможно угнетение кроветворения (лейкопения, агранулоцитоз, тромбоцитопения, мегалобластическая анемия и др.). Иногда возникают нарушения функции печени, почек.
Описаны случаи суперинфекции (кандидамикоз полости рта). При длительном применении бактрима необходимо контролировать состав периферической крови.
Бактрим противопоказан при выраженных нарушениях функции печени, почек и кроветворения. Не следует назначать его детям до 6 лет и при беременности.
Аналогичными препаратами являются лидаприм (сульфаметрол + триметоприм), сульфатен (содержит сульфамонометоксин и триметоприм), а также потесептил (сульфадимезин + триметоприм). Показания, побочные эффекты и противопоказания для обоих препаратов такие же, как для бактрима.
| Препараты | ||
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Сульфадимезин — Sulfadimezinum | Внутрь 1 г | Порошок; таблетки по 0,25 и 0,5 г |
| Этазол — Aethazolum | Внутрь 1 г | Порошок; таблетки по 0,25 и 0,5 г |
| Уросульфан — Urosulfanum | Внутрь 0,5—1 г | Порошок; таблетки по 0,5 г |
| Сульфапиридазин — Sulfapyridazinum | Внутрь 0,5—1 г | Порошок; таблетки по 0,5 г |
| Сульфадиметоксин — Sulfadimethoxinum | Внутрь 0,5—1 г | Порошок; таблетки по 0,2 и 0,5 г |
| Фталазол — Phthalazolum | Внутрь 1 г | Порошок; таблетки по 0,5 г |
| Сульфацил-натрий — Sulfacylum-natrium | Внутрь 0,5—1 г; внутривенно (медленно) 0,9—1,5 г; в полость конъюнктивы 1—2 капли 10—30% раствора или 10—30% мазь | Порошок; ампулы по 5 мл 30% раствора; флаконы по 5и 10 мл 30% раствора; 20% раствор (глазные капли) в тюбиках-капельницах по 1,5 мл; 30% мазь в упаковке по 10 г |
| Бактрим — Bactrimum | 2 таблетки | Таблетки (в 1 таблетке 0,4 г сульфаметоксазола и 0,08 г триметоприма) |
29.3. ПРОИЗВОДНЫЕ ХИНОЛОНА
К числу первых производных хинолона, получивших практическое применение, относится кислота налидиксовая (невиграмон, неграм). Основной спектр ее действия включает грамотрицательные бактерии (отсюда одно из названий — «неграм»). Она эффективна в отношении кишечной палочки, протея, капсульных бактерий (клебсиелл), шигелл, сальмонелл. Синегнойная палочка устойчива к кислоте налидиксовой. Механизм ее противомикробного действия связывают с угнетением синтеза ДНК. Устойчивость бактерий к препарату развивается довольно быстро (иногда через несколько дней после начала лечения).
Из желудочно-кишечного тракта препарат всасывается хорошо. Химическим превращениям подвергается примерно 20% от введенной дозы вещества. Выводится кислота налидиксовая (и ее метаболиты) главным образом почками, вследствие чего в моче создаются достаточно высокие концентрации вещества.
Основное применение — инфекции мочевыводящих путей, вызванные кишечной палочкой, протеем и другими микроорганизмами, чувствительными к кислоте налидиксовой. Ценным качеством препарата является его активность в отношении штаммов, устойчивых к антибиотикам и сульфаниламидным препаратам.
Из побочных эффектов возможны диспепсические нарушения, аллергические реакции, фотодерматозы, скоропреходящие нарушения зрения (снижение остроты зрения, светобоязнь), головная боль.
Противопоказанием служат заболевания с выраженным нарушением функции печени и почек. Не следует назначать препарат женщинам в первые 3 мес беременности и детям в возрасте до 2 лет.
За последние годы большое внимание привлекли фторхинолоны — производные хинолона, содержащие в структуре атомы фтора. Синтезировано значительное количество таких препаратов: ципрофлоксацин (ципробай), норфлоксацин, пефлоксацин, ломефлоксацин, офлоксацин (таривид) и др. Они являются высокоактивными антибактериальными средствами широкого спектра действия. Оказывают бактерицидное действие на грамотрицательные бактерии, в том числе на гонококки, кишечную палочку, шигеллы, сальмонеллы, Klebsiella pneumoniae, Enterobacter, Haemophilus influenzae, синегнойную палочку, микоплазмы, хламидии и др. В отношении грамположительных бактерий менее активны.
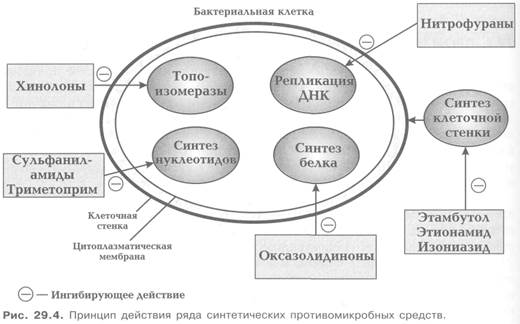
Механизм антибактериального действия фторхинолонов (рис. 29.4) заключается в ингибировании бактериальных ферментов топоизомераз II и IV (в том числе ДНК-гиразы — топоизомеразы II), что нарушает репликацию ДНК и соответственно образование РНК. Все это препятствует росту и размножению бактерий.
Фторхинолоны хорошо всасываются из пищеварительного тракта. Проникают в большинство тканей. Через гематоэнцефалический барьер проникают в необходимых концентрациях только отдельные препараты (офлоксацин, пефлоксацин, ципрофлоксацин), да и то при воспалении оболочек мозга. В умеренной степени связываются с белками плазмы. Выделяются в основном почками (путем фильтрации и активной секреции). Сравнительная фармакокинетика ряда фторхинолонов приведена в табл. 29.9.
Применяются они при инфекциях мочевыводящих, дыхательных путей, желудочно-кишечного тракта, вызванных микроорганизмами, чувствительными к фторхинолонам.
| Таблица 29.9. Фармакокинетика фторхинолонов | |||||||
| Препарат | Путь введения | Биодоступность, % | Связывание с белками плазмы, % | t1/2 ч | Проникновение через ГЭБ | Путь выведения | Кратность приема в сутки |
| Ципрофлоксацин | Внутрь, внутривенно | 50-80 | 20-40 | 3-4,5 | + | Почки | |
| Норфлоксацин | Внутрь | 30-40 | 10-35 | 4-5 | ± | Почки | |
| Офлоксацин | Внутрь | >90 | 8-32 | 5-7 | + | Почки | |
| Пефлоксацин | Внутрь, внутривенно | + | |||||
| Ломефлоксацин | Внутрь | ≥95 | ± | Почки | 1-2 | ||
| Эноксацин | Внутрь | 80-90 | 3-6 | Почки | |||
| Руфлоксацин | Внутрь | ||||||
| Гатифлоксацин | Внутрь | Почки | |||||
| Гемифлоксацин | Внутрь | ||||||
| Левофлоксацин | Внутрь | 6,9 | Почки | ||||
| Моксифлоксацин | Внутрь | 12,1 | Почки, кишечник | ||||
| Примечание: ГЭБ — гематоэнцефалический барьер. Плюс — проникает хорошо только при воспалении. (±) — проникает плохо (в том числе при воспалении). |
Привыкание микроорганизмов к фторхинолонам развивается относительно медленно. Из побочных эффектов отмечаются диспепсические нарушения, кожные высыпания и другие аллергические реакции, головная боль, головокружение, бессонница, фотосенсибилизация. Возможна суперинфекция. Однако в целом фторхинолоны переносятся хорошо.
Противопоказаны беременным и кормящим женщинам, а также пациентам в возрасте до 18 лет.
Одно из важных направлений в создании новых фторхинолонов — повышение противомикробного действия соединений на грамположительные бактерии, в частности на Streptococcus pneumoniae и другие стрептококки, атипичные и анаэробные возбудители. К числу таких препаратов относится моксифлоксацин (авелокс), отличающийся высокой бактерицидной активностью в отношении стрептококков, стафилококков, листерий, коринебактерий и в меньшей степени — энтерококков. Так, например, по влиянию на пневмококки (и бактероиды) in vitro моксифлоксацин в 4-16 раз активнее ципрофлоксацина и офлоксацина. Следует отметить, что моксифлоксацин эффективен при инфицировании грамположительными бактериями, устойчивыми ко многим другим антибактериальным средствам. Кроме того, моксифлоксацин характеризуется высокой активностью в отношении хламидий, микоплазм, уреаплазм и анаэробных возбудителей. Активность моксифлоксацина в отношении анаэробов находится на уровне метронидазола, клиндамицина и имипенема.
Препарат хорошо всасывается из кишечника. Биодоступность около 90%. Порядка 48% связывается с белками плазмы крови. 50% вещества метаболизируется в печени. Выделяются моксифлоксацин и его метаболиты почками и с желчью в кишечник. Назначают препарат 1 раз в сутки.
Переносится моксифлоксацин хорошо. Побочные эффекты в основном аналогичны таковым других фторхинолонов (отсутствует фотосенсибилизирующее действие). Нередко отмечаются тошнота, диарея, головокружение.
К новым фторхинолонам относятся также гатифлоксацин, гемифлоксацин, левофлоксацин. Все они эффективны при энтеральном введении, обладают высокой
Date: 2015-07-01; view: 1232; Нарушение авторских прав