
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Никотинамид- 6 page
|
|
Весьма перспективны также вещества, блокирующие глутаматергические влияния. К числу таких препаратов относятся антагонисты NMDA-рецепторов, устраняющие стимулирующие эффекты глутаматергических нейронов на базальные ядра и задерживающие дегенеративные изменения дофаминергических нейронов.
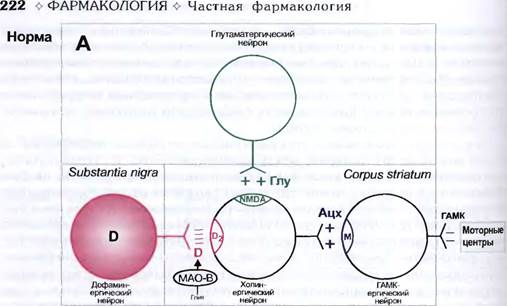
В функции ядер экстрапирамидной системы принимают участие также холинергические нейроны. При недостатке дофамина преобладают стимулирующие холинергические влияния. Для устранения создавшегося при этом дисбаланса между дофаминергическими и холинергическими влияниями можно использовать центральные холиноблокаторы. Препараты этой группы восстанавливают нарушенное равновесие за счет подавления холинергической передачи (рис. 10.1).
Исходя из принципов действия противопаркинсонических веществ, их подразделяют на следующие основные группы.
Болезнь Паркин- Б сона
Substantia nigra
(с*
ГАМК
'_/~ Моторные! ~ центры J
Леводопа
Селегилин
Бромокриптин
Циклодол
Глу - глутамат; D - дофамин;
Ацх - ацетилхолин; ГАМК - у-аминомасляная кислота;
NMDA - глутаматные NMDA-рецепторы; МАО-В - моноаминоксидаэа В
М - м-холинорецептор; D2 - дофаминовый 02-рецептор
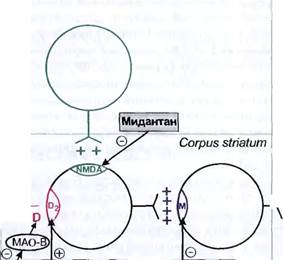
Рис. 10.1. Основная направленность действия противопаркинсонических средств (схема).
/. Вещества, активирующие дофаминергические влияния
1. Предшественник дофамина Леводопа
2. Средства, стимулирующие дофаминовые рецепторы (дофаминомиметики)
Бромокриптин Ропинирол
Глава 10 > Противопаркинсонические средства
3. Ингибиторы моноаминоксидазы В Селегилин
//. Вещества, угнетающие глутаматергические влияния Мидантан
///. Вещества, угнетающие холинергические влияния Циклодол
См. химические структуры
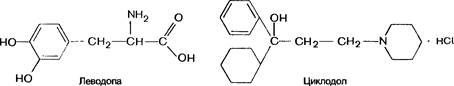
Леводопа (L-ДОФА, леводофа) представляет собой левовращающий изомер диоксифенилаланина, который является предшественником дофамина. Проникает через гематоэнцефалический барьер и затем в нейроны, где леводопа превращается в дофамин. Накапливаясь в базальных ганглиях, дофамин устраняет или ослабляет проявления паркинсонизма (см. рис. 10.1). Особенно выражение влияет леводопа на гипокинезию, менее — на ригидность, еще меньше — на тремор.
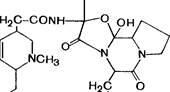
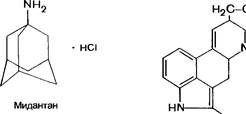
Химические структуры некоторых средств, применяемых для лечения паркинсонизма
Противопаркинсонические средства
СН(СН3)2
Вг
СН(СН3)2
Бромокриптин
СНз
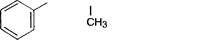
СН2 — СН — N — СН2 — С = СН
Селегилин
Ингибиторы ДОФА-декарбоксилазы
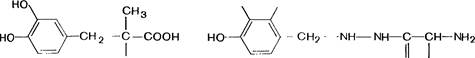
НО
ОН
NH—NH2
О СН2ОН
Карбидопа
Бенсеразид
224 ФАРМАКОЛОГИЯ О- Частная фармакология
цнс
ДОФА-
декарбоксилаза
ЛЕВОДОПА
I
ДОФАМИН
ГЭБ
рЛЕВ ОД ОПА~| --у ->■ ДОФАМИН
t
ДОФА-
декарбоксилаза
Периферические ткани
ЦНС ДОФА-
декарбоксилаза
ЛЕВОДОПА f--^*" ДОФАМИН
1_--
ГЭБ
^декарбоксилаз^
Периферические ткани
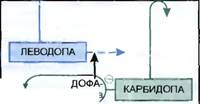
Рис. 10.2. Действие леводопы (а) и леводопы в сочетании с карбидопой (б) (схема). ГЭБ - гематоэнцефалический барьер; минус - угнетающее действие. Интенсивность красного! цвета условно отражает концентрацию дофамина в ЦНС и периферических тканях.
Леводопа относится к наиболее эффективным средствам, применяемым при лечении болезни Паркинсона и симптоматического паркинсонизма (исключая паркинсонизм, вызванный некоторыми лекарственными препаратами, в частности антипсихотическими средствами). Действие леводопы развивается через 1 нед и более и достигает максимума примерно через 1 мес. Дозу увеличивают постепенно. Назначают препарат только после еды. Лечение проводят длительно, так как это по существу заместительная терапия (восполняется недостаток дофамина).
Из желудочно-кишечного тракта препарат всасывается быстро. Однако значительная его часть (70—90%) метаболизируется в слизистой оболочке кишечника. В организме превращается в дофамин и другие метаболиты. Это происходит под влиянием ДОФА-декарбоксилазы, КОМТ и МАО. В итоге в ЦНС поступает около 1% от введенной дозы леводопы. Метаболиты и незначительные количества неизмененной леводопы выделяются почками.
Довольно часто наблюдаются побочные эффекты: нарушение аппетита, тошнота, рвота, ортостатическая гипотензия, сердечные аритмии, психические расстройства, двигательные нарушения (у ряда больных возникают хореиформные движения).
Все эти осложнения обратимы и могут быть нивелированы снижением дозы леводопы. Многие побочные эффекты связаны с образованием дофамина из леводопы в периферических тканях. Последнее можно уменьшить, комбинируя леводопу с ингибиторами периферической ДОФА-декарбоксилазы, не проникающими через гематоэнцефалический барьер (например, с карбидопой или бен-серазидом; рис. 10.2). Выпускают препараты, содержащие леводопу с карбидопой (синемет, наком) и леводопу с бенсеразидом (мадопар). Такие сочетания повышают количество леводопы, поступающей в ЦНС. Это связано с тем, что ингибируется декарбоксилирование леводопы в кишечнике и печени (повышается ее поступление в системное кровообращение), в периферических тканях, например в почках (что способствует поддержанию высоких концентраций ве-
Глава 10 > Противопаркинсонические средства <• 225
1 Применение аналогичного препарата тол кап она ограничено, так как у него выявлена выра-
щества в крови), а также в эндотелии капилляров мозга (устраняется энзимати-ческий барьер для проникновения леводопы в мозг).
Для повышения эффективности леводопы, устранения или уменьшения ее побочных эффектов, помимо использования ингибиторов периферической ДОФА-декарбоксилазы, применяют также ингибиторы КОМТ, например энта-капон (комтан1). Кроме того, при тошноте и рвоте назначают блокаторы дофаминовых рецепторов периферических тканей и пусковой зоны рвотного центра (например, домперидон; не проникает через гематоэнцефалический барьер). При развитии психозов используют блокатор дофаминовых рецепторов головного мозга клозапин (в 10 раз активнее в отношении D4-, чем Dj-рецепторов).
Нельзя сочетать леводопу с неизбирательными ингибиторами МАО (последняя инактивирует норадреналин, дофамин; при угнетении МАО может возникнуть резкая гипертензия), а также с пиридоксином (витамином В6), который снижает активность леводопы.
Наиболее эффективна леводопа в течение 2—5 лет. Постепенно развивается привыкание, возникают дискинезия и другие побочные эффекты.
Препарат противопоказан при тяжелых заболеваниях сердечно-сосудистой системы, печени, почек, при психозах.
К стимуляторам дофаминовых рецепторов, используемым при лечении паркинсонизма, относится бромокриптин (парлодел). По химическому строению это полусинтетическое производное алкалоида спорыньи эргокрипти-на (производное лизергиновой кислоты). Является агонистом дофаминовых Dj-рецепторов. Обладает отчетливой противопаркинсонической активностью. К типичным эффектам бромокриптина относится также торможение продукции пролактина и гормона роста (см. главу 20; 20.1). Принимается внутрь. Из желудочно-кишечного тракта всасывается около 30%. Большая часть инакти-вируется при первом прохождении печеночного барьера. Максимальная концентрация в плазме накапливается через 1,5—3 ч; t =3—6 ч. Значительная часть бромокриптина подвергается биотрансформации. Основной путь выведения — с желчью в кишечник. Бромокриптин, как правило, применяют в комбинации с леводопой.
Побочные эффекты на начальных стадиях лечения: тошнота, рвота, ортоста-тическая гипотензия. При длительном применении возможны психические нарушения, дискинезия, непереносимость этилового спирта, запор и др.
Одним из агонистов D2- и Dj-дофаминовых рецепторов является ропинирол (реквип). Противопаркинсонический эффект связывают с его влиянием на постсинаптические Dj-дофаминовые рецепторы в неостриатуме. Угнетает секрецию пролактина. По эффективности при паркинсонизме ропинирол превосходит бромокриптин.
Как отмечалось, один из путей усиления дофаминергических влияний заключается в подавлении процессов инактивации дофамина. По такому принципу действуют ингибиторы МАО-В. К избирательным необратимо действующим ингибиторам этого фермента относится селегилин (депренил). Обычно его применяют в сочетании с леводопой. Отличается от ингибиторов МАО неизбирательного действия тем, что при взаимодействии с симпатомиметиками не вызывает выраженных гипертензивных реакций (см. главу 11.2).
226 О ФАРМАКОЛОГИЯ ❖ Частная фармакология
1 Первоначально был предложен как противовирусное средство для профилактики гриппа типа А2 под названием амантадин (см. главу 28).
В эксперименте обнаружено, что, помимо ингибирования МАО-В, селегилин обладает нейропротекторным эффектом, уменьшая повреждение нейронов при ишемии и при воздействии ряда нейротоксических веществ. Частично это может быть связано с индукцией фактора роста нервов, продуцируемого глиальными астроцитами. Имеются предварительные клинические данные о благоприятном влиянии селегилина на состояние пациентов при таком нейродегенеративном заболевании, как болезнь Альцгеймера. Не исключено, что подобный эффект может проявляться и в отношении болезни Паркинсона, но это требует специального исследования.
К противопаркинсоническим веществам, устраняющим глутаматергические влияния, относится м идантан1 (амантадина гидрохлорид, симметрел). Согласно современным представлениям, мидантан блокирует глутаматные NMDA-рецеп-торы и тем самым снижает стимулирующее влияние кортикальных глутаматных нейронов на неостриатум, превалирующее на фоне недостаточности дофамина. Это уменьшает клинические проявления болезни Паркинсона — ригидность, тремор и гипокинезию. Кроме того, отмечено, что мидантан обладает нейропротекторным эффектом в отношении нейронов черной субстанции. Связывают это также с угнетением NMDA-рецепторов указанных нейронов и уменьшением поступления в клетки ионов кальция, что снижает возможность деструкции нейронов и замедляет прогрессирование заболевания. Мидантан обладает и некоторым м-холиноблокирующим эффектом.
Применяют мидантан при лечении болезни Паркинсона и симптоматическом паркинсонизме (постэнцефалитическом или цереброваскулярном), особенно в случаях, когда леводопа противопоказана. Мидантан устраняет или уменьшает гипокинезию, в меньшей степени — ригидность и тремор. Улучшение наступает через 1—2 сут и более; максимальный эффект наблюдается через несколько дней, иногда недель.
Переносится мидантан в большинстве случаев хорошо. Из побочных эффектов иногда наблюдаются бессонница, галлюцинации, ортостатическая гипотен-зия, диспепсические расстройства, головная боль.
Препарат следует с осторожностью применять при ряде заболеваний ЦНС, сопровождающихся галлюцинациями, эпилептиформными судорогами, а также при тяжелых заболеваниях печени и почек.
Весьма целесообразно комбинированное применение с леводопой, что позволяет уменьшить ее дозу.
Последняя группа противопаркинсонических средств представлена так называемыми центральными холиноблокаторами. Они подавляют стимулирующие холинергические влияния на базальные ганглии благодаря угнетению центральных холинорецепторов. На синтез, высвобождение и гидролиз ацетилхолина, по имеющимся данным, они не влияют. Из таких препаратов широкое применение получил циклодол (артан, тригексифенидила гидрохлорид). Он оказывает как центральное, так и периферическое м-холиноблокирующее действие. Влияние на ЦНС способствует уменьшению или устранению двигательных нарушений, связанных с поражением экстрапирамидной системы. Циклодол наиболее эффективно уменьшает тремор и в меньшей степени — ригидность, мало влияя на гипокинезию.
Глава 11 ■> Психотропные средства -о 227
Препараты
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Леводопа — Levodopa | Внутрь 0,25—1 г | Капсулы и таблетки по 0,25—0,5 г |
| Мидантан — Midantanum | Внутрь 0,05-0,1 г | Таблетки, покрытые оболочкой, по 0,1 г |
| Циклодол — Cyclodolum | Внутрь 0,001-0,005 г | Таблетки по 0,001; 0,002 и 0,005 г |
| Селегилин — Selegiline | Внутрь 0,005-0,01 г | Таблетки по 0,005 и 0,01 г |
| Бромокриптин — Bromocriptine | Внутрь 0,03-0,04 г | Таблетки по 0,0025 г; капсулы по 0,005 и 0,01 г |
Гл а в а 11
ПСИХОТРОПНЫЕ СРЕДСТВА
Препараты этой группы применяют при нарушениях психической деятельности. Их используют при лечении психозов, а также при невротических и неврозо-подобных расстройствах, сопровождающихся состоянием напряжения, беспокойства, страха, тревоги и другими симптомами.
Механизмы действия психотропных веществ изучены лишь в небольшой степени, хотя масштабы таких исследований велики. Наиболее интересны сведения о влиянии этих веществ на межнейронную передачу, обмен биогенных аминов, на холинергические системы головного мозга, взаимодействие с пептидами, аминокислотами, оказывающими стимулирующее и тормозное влияние на нейроны.
Применяют циклодол при болезни Паркинсона, паркинсонизме и других патологических состояниях, связанных с поражением экстрапирамидной системы. Циклодол эффективен также при явлениях паркинсонизма, вызванных антипсихотическими средствами. Назначают препарат внутрь. Он хорошо всасывается из тонкой кишки и быстро выводится. Кумуляции не наблюдается. При длительном применении развивается привыкание.
Угнетение периферических м-холинорецепторов является причиной ряда нежелательных эффектов (сухость слизистой оболочки полости рта, тахикардия, нарушение аккомодации, снижение тонуса мышц кишечника и др.). Спазмолитическое действие циклодола связано как с атропиноподобным, так и с прямым миотропным (папавериноподобным) действием. При передозировке циклодола могут возникать нарушения со стороны ЦНС (возбуждение, галлюцинации).
Циклодол противопоказан или его следует применять с осторожностью при глаукоме, нарушении мочеотделения, вызванном гипертрофией предстательной железы, при заболеваниях сердца, печени, почек. Не следует назначать циклодол пожилым людям (ухудшается память, нарушается мышление).
При лечении паркинсонизма иногда используют и другие центральные холи-ноблокаторы: тропацин (дифенилтропина гидрохлорид), бензтропина мези-лат (когентин) и др.
Все перечисленные противопаркинсонические препараты не относятся к средствам этиотропной терапии. Они лишь устраняют или ослабляют синдром паркинсонизма, и поэтому лечебный эффект сохраняется только во время их применения.
228 -> ФАРМАКОЛОГИЯ - Частная фармакология
Таблица 11.1. Психотропные средства
| Группа | Средства, применяемые преимущественно при психозах | Средства, применяемые преимущественно при психических нарушениях непсихотического характера (или так называемых пограничных состояниях) |
| Вещества с психоседативным действием | Антипсихотические средства | Анксиолитики Седативные средства |
| Вещества с психостимулирующим действием | Психостимуляторы | |
| Вещества, не оказывающие на здоровых людей ни психосе-дативного, ни психостимулирующего действия | Средства для лечения маний (соли лития) |
и др. Однако механизмы антипсихотического и антиневротического действия препаратов остаются недостаточно ясными, и прежде всего потому, что причины возникновения большинства психических заболеваний и психопатологических состояний неизвестны. Значительные трудности возникают при поиске и доклинической оценке потенциальных психотропных препаратов. К сожалению, не существует адекватных экспериментальных моделей психических расстройств, наблюдаемых у человека. В связи с этим приходится использовать комплекс разнообразных методик, позволяющих оценить влияние вещества на высшую нервную деятельность животных и на этом основании прогнозировать возможности их клинического применения. При исследовании психотропного действия веществ широко используют разнообразные варианты метода условных рефлексов, изучают их влияние на поведенческие реакции, эмоции, мотивации, двигательную активность, экспериментальные психозы и неврозы. Благодаря накопленному опыту в области психофармакологии можно, хотя и в общих чертах, предсказать сферу предполагаемого применения нового соединения, основываясь на некоторых имеющихся корреляциях между экспериментальными и клиническими данными. Однако решающее суждение о пригодности препарата для лечения или профилактики определенных психопатологических состояний можно высказать только после клинических исследований.
Широкое внедрение в медицинскую практику психотропных средств началось с середины XX в. За прошедший период появилось множество препаратов, эффективных при различных психических расстройствах (табл. 11.1). Так, при психозах с успехом используют антипсихотические средства (аминазин, галопери-дол и др.), антидепрессанты (имизин, флуоксетин), соли лития. Для большинства антипсихотических средств, помимо специфического антипсихотического эффекта, характерно успокаивающее (седативное) действие. Основным свойством антидепрессантов является их способность устранять депрессии. Кроме того, антидепрессанты из группы неизбирательных ингибиторов МАО (пиаламид) обладают психостимулирующим эффектом. У трициклических антидепрессантов (например, у имизина) наряду с антидепрессивной активностью может проявляться как психостимулирующее, так и седативное действие. Соли лития применяют для лечения и профилактики маниакальных состояний; ни стимулирующего, ни седативного действия на психическую сферу здорового человека они не оказывают.
Глава 11 Психотропные средства -"- 229
1 От греч. neuron — нерв, leptos — нежный, тонкий.
При психических расстройствах непсихотического (невротического) характера назначают анксиолитики (диазепам и др.), седативные средства (бромиды, препараты валерианы) и психостимуляторы (сиднокарб). К психотропным веществам относятся и так называемые галлюциногены, или психотомиметики (ЛСД-25, мес-калин и др.). Эти вещества вызывают кратковременные остро развивающиеся психозы. Лечебного значения галлюциногены не имеют, однако в социальном аспекте они требуют внимания, так как относятся к средствам, приводящим к развитию психической зависимости. Для фундаментальной медицины они представляют интерес в качестве веществ, вызывающих экспериментальные психозы.
Открытие и внедрение в практику активных психотропных средств является одним из наиболее крупных достижений медицины. Прежде всего это принципиально изменило ситуацию в терапии психических заболеваний. До появления этих препаратов возможности лечения такого контингента больных были более чем ограничены (в основном использовали электрошок и инсулиновую кому). Кроме того, психотропные препараты существенно пополнили арсенал лекарственных средств, применяемых в других областях медицины — терапии, анестезиологии, неврологии и др. Важно и то, что успехи в создании психотропных средств в значительной степени стимулировали фундаментальные исследования (фармакологические, физиологические, биохимические, патофизиологические) по столь важной и вместе с тем сложной для познания проблеме, как механизмы разных проявлений высшей нервной деятельности, а также в выяснении этиологии и патогенеза психических нарушений и принципов их лечения.
11.1. АНТИПСИХОТИЧЕСКИЕ СРЕДСТВА (НЕЙРОЛЕПТИКИ)'
Препараты этой группы оказывают антипсихотическое и в той или иной степени выраженное седативное (успокаивающее) действие. Антипсихотический эффект проявляется в устранении продуктивной симптоматики психозов (бреда, галлюцинаций) и задержке дальнейшего развития заболевания. Психоседативное действие характеризуется общим успокоением, сопровождающимся устранением аффективной напряженности, снижением беспокойства, тревоги, понижением двигательной активности.
Механизм антипсихотического действия недостаточно выяснен. Высказывается предположение, что для большинства препаратов данной группы этот эффект связан с блоком постсинаптических дофаминовых Dj-рецепторов лимби-ческой системы. Блокирующее влияние на дофаминовые рецепторы проявляется антагонизмом с дофамином и дофаминомиметиками (апоморфином, фенамином) как по поведенческим реакциям, так и на уровне отдельных нейронов.
Влиянием на дофаминергическую систему объясняется также способность антипсихотических средств вызывать столь типичный для них побочный эффект, как экстрапирамидные нарушения. В этом случае все события разыгрываются в неостриатуме, где локализуется значительное число рецепторов, чувствительных к дофамину, которые блокируют антипсихотические средства.
Антагонизм между антипсихотическими средствами и дофамином подтверждается, в частности, экспериментами с ионофоретической инъекцией дофамина в область хвостатого ядра. Предварительное введение в этих условиях опыта антипсихотического средства аминазина устраняет угнетающее влияние дофамина
230 о ФАРМАКОЛОГИЯ о Частная фармакология


на нейроны хвостатого ядра. Благодаря подавлению нигростриатной передачи и снижению тормозной функции черной субстанции в отношении неостриатума (см. рис. 10.1) изменяется участие последнего в регуляции двигательной активности. Проявляется это усилением активности а-мотонейронов спинного мозга, повышением тонуса мышц и развитием лекарственного паркинсонизма (возникают гипокинезия, ригидность, тремор). Предполагается, что изменение функционального состояния неостриатума может иметь значение и в развитии антипсихотического действия препаратов.
С блокадой дофаминовых рецепторов связан также ряд других эффектов антипсихотических средств (табл. 11.2).
Седативное действие антипсихотических средств, по-видимому, частично связано с их влиянием на восходящую ретикулярную формацию ствола головного мозга. Антипсихотические средства устраняют реакцию активации ЭЭГ на внешние раздражения, мало влияя на возбудимость нейронов ретикулярной формации при их прямом электрическом раздражении. Показано, что при ионофоретическом нанесении ряда антипсихотических средств на нейроны ретикулярной формации ствола головного мозга уменьшается или утрачивается их чувствительность к возбуждающему действию норадреналина. Очевидно, блокируя адренорецепторы, антипсихотические средства угнетают передачу нервных импульсов с коллатералей специфических афферентных путей на нейроны ретикулярной формации. По-видимому, в седативном эффекте важную роль играет также их влияние на лимбическую систему и гипоталамус.
На ЭЭГ седативное действие антипсихотических средств проявляется возник новением высоковольтных медленных колебаний (результат синхронизации ЭЭГ).
Помимо блокирования рецепторов, чувствительных к дофамину и норадрена лину, антипсихотические средства, по-видимому, в какой-то степени наруша высвобождение этих биогенных аминов и их обратный нейрональный захват.
Для некоторых антипсихотических средств (например, производных фенотиа-зина) в развитии психотропных эффектов может иметь значение их блокирующее влияние на серотониновые рецепторы и м-холинорецепторы головного мозга.
ИВАН ПЕТРОВИЧ ПАВЛОВ (1849-1936).
Основоположник физиологии и фар макологии высшей нервной деятель ности.
IK-Г). га-
Таблица 11.2. Некоторые эффекты, связанные с блокирующим действием антипсихотичес-. ких средств на дофаминовые рецепторы головного мозга
| Локализация дофаминовых рецепторов | Основные эффекты |
| Мезолимбическая и мезокортикальная системы | Антипсихотический эффект. Эмоциональная индифферентность. Депрессия |
| Гипоталамус—гипофиз | Снижение температуры тела. Галакторея (повышается выделение пролактина) |
| Экстрапирамидная система | Явления паркинсонизма; поздняя дискинезия |
| Пусковая («триггер») зона рвотного центра | Противорвотный эффект |
Глава 11 <• Психотропные средства -о 231
Антипсихотические препараты принято подразделять на так называемые «типичные» и «атипичные». Основное различие заключается в том, что для «типичных» препаратов характерен такой побочный эффект, как нарушение функции экстрапирамидной системы (возникают паркинсонизм и другие двигательные нарушения). Для «атипичных» антипсихотических средств этот крайне отрицательный эффект наблюдается относительно редко и выражен в небольшой степени. Основой этих различий является несколько иной спектр рецепторного действия, в частности, в отношении разных подтипов дофаминовых рецепторов. К указанным группам относятся следующие препараты.
А. «Типичные» антипсихотические средства
Производные фенотиазина
Аминазин Трифтазин Фторфеназин
Производные тиоксантена
Хлорпротиксен
Производные бутирофенона
Галоперидол
Б. «Атипичные» антипсихотические средства
Бензамиды
Сульпирид
Производные бензодиазепина Клозапин
Наибольшее количество препаратов относится к фенотиазиновым производным, которые в зависимости от радикалов у N10 подразделяют на ряд подгрупп:
1. Алифатические производные (аминазин).
2. Пиперазиновые производные (трифтазин, фторфеназин).
Типичным представителем производных фенотиазина является аминазин (хлорпромазина гидрохлорид, ларгактил).
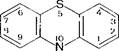
Фенотиазин
Аминазин имеет широкий спектр действия. Препарат оказывает выраженное влияние на ЦНС, а также на периферическую иннервацию, исполнительные органы и обмен веществ.
Влияние на ЦНС проявляется рядом эффектов. Так, для аминазина характерны антипсихотическое и седативное действие, а также способность вызывать экстрапирамидные расстройства (при длительном применении). В больших дозах он вызывает гипнотический эффект: наступает поверхностный сон, легко прерываемый внешним раздражением.
Характерным для аминазина является миорелаксирующее действие, проявляющееся снижением двигательной активности. Связано это с угнетением супра-спинальной регуляции мышечного тонуса в основном за счет воздействия на ба-зальные ядра. Аминазин также уменьшает или полностью устраняет нисходящие облегчающие влияния ретикулярной формации наспинальные рефлексы. Непосредственно на спинной мозг препарат не действует.
Аминазин угнетает центр теплорегуляции. Конечный эффект зависит от температуры окружающей среды. Чаще всего наблюдается незначительная гипотер
232 ■<> ФАРМАКОЛОГИЯ Частная фармакология
мия (за счет увеличения теплоотдачи). В то же время при сочетании аминазина с физическим охлаждением возникает выраженное снижение температуры тела.
Аминазин обладает отчетливым противорвотным эффектом, который связан с блокированием дофаминовых рецепторов пусковой зоны (trigger zone), расположенной на дне IV желудочка. Благодаря этому аминазин предупреждает рвоту, вызываемую апоморфином, морфином, многими противобластомными средствами (см. главу 32; 32.1).
Одним из проявлений влияния аминазина на ЦНС является его способность потенцировать действие ряда нейротропных препаратов — средств для наркоза, снотворных наркотического типа, опиоидных анальгетиков. Усиление их эффектов частично связано с угнетением аминазином процессов биотрансформации этих препаратов.
Аминазин оказывает влияние и на периферическую иннервацию. Наиболее выражено у него а-адреноблокируюшее действие. Так, на фоне аминазина прессор-ная реакция на адреналин резко снижается или наступает «извращение» эффекта адреналина и артериальное давление падает (см. главу 4; 4.2). Кроме того, аминазину присущи некоторые м-холиноблокирующие (атропиноподобные) свойства. Это проявляется небольшим снижением секреции слюнных, бронхиальных и пищеварительных желез. Передачу возбуждения в вегетативных ганглиях он не нарушает.
Аминазин влияет не только на эфферентную, но и на афферентную иннервацию. При местном действии он вызывает выраженное раздражение, которое сменяется анестезией. У аминазина имеется отчетливая противогистаминная активность (блокирует гистаминовые Н,-рецепторы; см. главу 25). Он является также спазмолитиком миотропного действия.
Date: 2015-07-01; view: 538; Нарушение авторских прав