
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Никотинамид- 3 page
|
|
Глава 7 • Снотворные средства v 191
Препараты
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Нитразепам — Nitrazepam | Внутрь 0,005-0,01 г | Таблетки по 0,005 и 0,01 г |
| Золпидем — Zolpidem | Внутрь 0,01 г | Таблетки по 0,01 г |
| Этаминал-натрий — Aethaminalum natrium | Внутрь 0,1—0,2 г; ректально 0,2 г | Порошок; таблетки по 0,1 г |
| Хлоралгидрат — Chlorali hydras | Внутрь и ректально (в клизмах) 0,5—1 г | Порошок |
никает синдром абстиненции. В связи с этим при лечении хронических отравлений дозу барбитурата снижают постепенно до полной его отмены. Одновременно проводят симптоматическое лечение и психотерапию.
Ряд снотворных средств относится к алифатическим соединениям. Одним из них является хлоралгидрат. Это первое синтетическое снотворное, использованное в практической медицине. Оказывает выраженный снотворный эффект. Способствует развитию сна продолжительностью до 8 ч. От барбитуратов отличается тем, что практически не нарушает структуру сна. В больших дозах вызывает наркоз. Наркотическая широта у хлоралгидрата небольшая (быстро наступает угнетение центров продолговатого мозга).
Всасывается из кишечника быстро. Свободно проходит через тканевые барьеры. В организме превращается в трихлорэтанол (но свойствам аналогичен хлоралгидрату). Хлоралгидрат в небольшой степени стимулирует синтез микросомальных ферментов печени. Метаболиты и конъюгаты хлоралгидрата выделяются почками.
При повторном введении хлоралгидрата к нему развивается привыкание, возможна лекарственная зависимость (психическая и физическая). Кумуляция практически не возникает.
Применяют препарат внутрь или ректально (в клизмах) в качестве снотворного (за 15— 30 мин до сна), седативного или противосудорожного средства.
Хлоралгидрат обладает рядом отрицательных свойств. К ним относится возможное неблагоприятное влияние на паренхиматозные органы: печень, почки, сердце. Проявляются данные токсические эффекты главным образом на фоне патологических изменений этих органов, а также при передозировке. Кроме того, хлоралгидрат оказывает выраженное раздражающее действие, поэтому его обычно назначают в сочетании со слизями. Наиболее целесообразно кратковременное применение хлоралгидрата (1—3 дня).
Применяют снотворные средства достаточно широко. При назначении этих препаратов следует учитывать возможность развития привыкания к ним и лекарственной зависимости. Поэтому целесообразно назначать их в минимальной эффективной дозе и не дольше 1 мес либо делать интервалы между приемами 2—3 дня. Необходимо ориентировать пациентов в способности препаратов вызывать последействие, что может отрицательно влиять на их профессиональную деятельность. Важно также иметь в виду взаимодействие с другими лекарственными веществами и этиловым спиртом. Нельзя не учитывать и изменение фармакокине-тики снотворных средств при патологии печени и почек. Отменять препараты следует постепенно, чтобы не развился синдром «отдачи» (а при физической лекарственной зависимости — абстинентный синдром).
Несмотря на значительное число снотворных средств, создание новых, более совершенных препаратов, способствующих нормализации сна, по-прежнему остается одной из важных задач фармакологии. Необходимо, чтобы наряду с высокой активностью, отсутствием побочных эффектов и большой терапевтической широтой новые снотворные средства не приводили бы к нарушению соотношения фаз сна, не вызывали кумуляции, привыкания и лекарственной зависимости.
192 <. ФАРМАКОЛОГИЯ ■■> Частная фармакология
1 Хроническими болями страдают 8-30% взрослого населения.
2 От лат. посео - повреждаю.
' К ним относятся ядра среднего мозга (околоводопроводное серое вещество — periaqueductal gray), продолговатого мозга (большое ядро шва — nucleus raphe magnus; большеклеточное, гигантоклеточ-ное, парагигантоклеточное и латеральное ретикулярные ядра — nuclei reticulares magnocellularis, gigantoeellularis et lateralis; голубое пятно — locus coeruleus) и др.
Глава 8
БОЛЕУТОЛЯЮЩИЕ (АНАЛЬГЕЗИРУЮЩИЕ) СРЕДСТВА
Причиной острых и хронических болевых ощущений могут быть как органические, так и психогенные нарушения. Боль возникает при повреждающих воздействиях на кожу, слизистые оболочки, связки, мышцы, суставы, внутренние органы. Нередко боль обусловлена нарушением функции самой нервной системы. Это так называемые нейропатические боли, связанные с прямой травмой периферических нервов или мозговой ткани, с ишемией, инфекцией, разрастанием опухолей и т.д.
С учетом очень большой распространенности патологических процессов, сопровождающихся болями1, которые могут сохраняться месяцами и годами, значимость болеутоляющих средств трудно переоценить. Устранение или облегчение боли анальгетиками улучшает физическое и психическое состояние пациента, что благоприятно сказывается на его профессиональной и социальной жизни.
Болевые ощущения воспринимаются специальными рецепторами, которые получили название «ноцицепторы»2. Они представляют собой окончания древовидно-разветвленных афферентных волокон, расположенных в коже, мышцах, суставных капсулах, надкостнице, внутренних органах и т.д. Повреждающими (ноцицептивными) раздражителями могут быть механические, термические и химические воздействия. Причиной боли нередко является патологический процесс (например, воспаление). Известны эндогенные вещества, которые, воздействуя на ноцицепторы, способны вызывать болевые ощущения (брадикинин, гистамин, серотонин, ионы калия и др.). Простагландины (например, Е2) повышают чувствительность ноцицепторов к химическому (и термическому) раздражению.
Вызванные болевым раздражением импульсы распространяются по С- и Ав-волокнам и поступают в задние рога спинного мозга (рис. 8.1). Здесь происходит первое переключение с афферентных волокон на вставочные нейроны. Отсюда возбуждение распространяется по ряду путей. Один из них — восходящие афферентные тракты. Они проводят возбуждение к вышележащим отделам — ретикулярной формации, таламусу, гипоталамусу, к базальным ганглиям, лимбической системе и коре большого мозга. Сочетанное взаимодействие этих структур приводит к восприятию и оценке боли с последующими поведенческими и вегетативными реакциями. Второй путь — передача импульсов на мотонейроны спинного мозга, что проявляется двигательным рефлексом. Третий путь осуществляется за счет возбуждения нейронов боковых рогов, в результате чего активируется ад-ренергическая (симпатическая) иннервация.
Функционирование нейронов задних рогов спинного мозга регулируется супраспинальной антиноцицептивной системой. Последняя представлена комплексом структур3, оказывающих нисходящее тормозное влияние на передачу болевых стимулов с первичных афферентных волокон на вставочные нейроны. Например, показано, что электрическое раздражение околоводопроводного серого вещества или парагигантоклеточного ретикулярного ядра либо микроинъекция в
Глава 8 ❖ Болеутоляющие (анальгезируюшие) средства ❖ 193
Кора
большого мозга
Лимбическая система
Таламус
Гипоталамус
Продолговатый мозг
Ноцицепторы
Восходящие
афферентные
пути
Спинной мозг
- Скелетная мышца
-Кровеносный сосуд
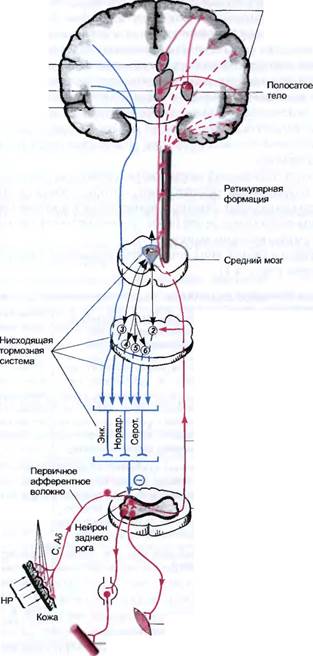
Рис. 8.1. Пути проведения боли.
HP - ноцицептивное раздражение; Серот. - серотонинергические волокна; Норадр. - норадре-нергические волокна; Энк. - энкефалинергические волокна; минус - тормозной эффект." 1 - околоводопроводное серое вещество; 2 - большое ядро шва; 3 - голубое пятно; 4 - боль-шеклеточное ретикулярное ядро; 5 - гигантоклеточное ретикулярное ядро; 6 - парагиганток-леточное ядро.
них энкефалинов вызывает снижение болевой чувствительности. Осуществляется нисходящее торможение за счет серотонинергических, норадренергических и, очевидно, пептидергических (энкефалинергических и др.) нейронов.
194 -с- ФАРМАКОЛОГИЯ ❖ Частная фармакология
Таблица 8.1. Типы опиоидных рецепторов: эндогенные лиганды, локализация, эффекты
| Тип опиоидных рецепторов' | Эндогенные лиганды | Локализация в ЦНС рецепторов, принимающих участие в регуляции ноцицепции | Некоторые эффекты, связанные с активацией центральных и периферических опиоидных рецепторов |
| И (мю) | Эндоморфины | Неостриатум, кора головного мозга, таламус, п. accumbens, гип-покамп, миндалевидное тело, поверхностный слой серого вещества задних рогов спинного мозга, большое ядро шва, околоводопроводное серое вещество | Анальгезия, седативный эффект, эйфория, физическая зависимость, угнетение дыхания, снижение моторики желудочно-кишечного тракта, брадикардия, миоз |
| (дельта) | Энкефалины | Обонятельная луковица, кора головного мозга, неостриатум, п. accumbens, таламус, гипоталамус, ствол головного мозга, поверхностный слой серого вещества задних рогов спинного мозга | Анальгезия, угнетение дыхания, снижение моторики желудочно-кишечного тракта |
| к (каппа) | Динорфины | Кора головного мозга, п. accumbens, перегородка, межножковое ядро | Анальгезия, седативный эффект, дисфория, миоз, небольшое снижение моторики желудочно-кишечного тракта, возможна физическая зависимость |
' Комитетом Международного союза фармакологов предложена новая номенклатура опиоидных рецепторов: ОР, (6), ОР2 (к) и ОР3 (ц).
Выделен и ряд подтипов опиоидных рецепторов, имеющих определенную функциональную значимость. Так, супраспинальную анальгезию связывают с р,-, к3-, 5,- и 52-подтипами, а спинальную — с р2-, 52-и к,-подтипами.
1 Algesis (греч.) — ощущение боли.
2 ORLI — опиоидоподобный рецептор (opioid receptor like protein). Его обозначают также N/OFQ (nociceptin/orfanin FQ) рецептор или ОР4.
3 О ваниллоидных (капсаициновых) рецепторах и их лигандах см. на с. 165.
Следует учитывать и наличие значительного числа различных эндогенных пептидов, в том числе с анальгетической активностью (энкефалины, fi-эндорфин, динорфины, эндоморфины), а также альгетическими1 свойствами (например, субстанция Р). Последние вызывают или усиливают болевые ощущения. Кроме того, недавно выделен эндогенный пептид, названный ноцицептином. Он специфически взаимодействует со специальными рецепторами, отличающимися от опиоидных рецепторов2, и принимает участие в регуляции ноцицепции. Обладают антино-цицептивным действием. В тканях мозга образуются и многие другие биологически активные вещества, которые могут играть роль не только медиаторов, но и модуляторов передачи болевых стимулов3. В качестве последних выступают и некоторые нейрогормоны.
Пептиды с анальгетической активностью (опиоиды) взаимодействуют со специфическими опиоидными рецепторами, которые обнаружены в большинстве образований, принимающих участие в проведении и восприятии боли. Выявлено несколько типов опиоидных рецепторов, различающихся по чувствительности к эндогенным и синтетическим опиоидам.
С возбуждением каждого типа рецепторов связывают определенные физиологические эффекты (табл. 8.1).
Глава 8 Болеутоляющие (анальгезирующие) средства -С- 195
1 Происхождение термина «анальгетик» см. в главе 5.
Таким образом, в организме функционирует сложная нейрогуморальная анти-ноцицептивная система. В случае ее недостаточности (при чрезмерно выраженном или длительном повреждающем воздействии) болевые ощущения приходится подавлять с помощью болеутоляющих средств.
Анальгетики1 — препараты, которые при резорбтивном действии избирательно подавляют болевую чувствительность. Они не выключают сознание и не угнетают другие виды чувствительности. Исходя из фармакодинамики соответствующих препаратов, их подразделяют на следующие группы.
I. Средства преимущественно центрального действия А. Опиоидные (наркотические) анальгетики
1. Агониеты
2. Агонисты-антагонисты и частичные агониеты
Б. Неопиоидные препараты с анальгетической активностью
1. Неопиоидные (ненаркотические) анальгетики (производные параами-нофенола)
2. Препараты из различных фармакологических групп с анальгетическим компонентом действия
II. Средства преимущественно периферического действия
Неопиоидные (ненаркотические) анальгетики (производные салициловой кислоты, пиразолона и др.; см. в главе 24 в разделе «Нестероидные противовоспалительные средства»). В этой главе будут рассмотрены анальгетики, действующие преимущественно на ЦНС.
8.1. ОПИОИДНЫЕ (НАРКОТИЧЕСКИЕ) АНАЛЬГЕТИКИ И ИХ АНТАГОНИСТЫ
Фармакологические эффекты опиоидных анальгетиков и их антагонистов обусловлены взаимодействием с опиоидными рецепторами, которые обнаружены как в ЦНС, так и в периферических тканях.
Исходя из принципа взаимодействия анальгетиков этой группы с опиоидными рецепторами, их можно представить в виде следующих групп.
Агониеты
Морфин Промедол Фентанил Суфентанил Агонисты-антагонисты и частичные агониеты Пентазоцин Налбуфин Буторфанол Бупренорфин
Многие опиоидные анальгетики относятся к первой группе веществ. Однако в этом качестве могут быть использованы и агонисты-антагонисты, если у них доминируют свойства агонистов (например, пентазоцин), а также частичные агониеты. В связи с тем, что эти анальгетики взаимодействуют с опиоидными рецепторами, их называют опиоидами.
Опиоидные анальгетики оказывают выраженное угнетающее влияние на ЦНС. Оно проявляется анальгетическим, снотворным, противокашлевым действием. Кроме того, большинство из них изменяют настроение (возникает эйфория) и вызывают лекарственную зависимость (психическую и физическую).
К группе опиоидных анальгетиков относится ряд препаратов, получаемых как из растительного сырья, так и синтетическим путем.
196 ❖ ФАРМАКОЛОГИЯ ❖ Частная фармакология Агониеты опиоидных рецепторов
Широкое распространение в медицинской практике получил алкалоид1 морфин. Выделяют его из опия2, который является застывшим млечным соком, вытекающим из надрезов головок снотворного мака — Papaver somniferum (рис. 8.2). В опии, предназначенном для медицинских целей, должно быть не менее 10% морфина. Всего опий содержит более 20 алкалоидов.
По химической структуре одни алкалоиды опия относятся к производным фе-нантрена, другие — к производным изохинолина.

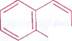
Фенантрен
Изохинолин
Для производных фенантрена (морфин, кодеин и др.) характерно в основ- J ном угнетающее действие на ЦНС (анальгетическое, противокашлевое), а для алкалоидов изохинолинового ряда (папаверин и др.) — прямое спазмолитическое действие на гладкие мышцы.
В настоящем разделе из алкалоидов опия будет рассмотрен только морфин как типичный представитель опиоидных (наркотических) анальгетиков.
Основным для морфина является болеутоляющий эффект. Морфин обладает I достаточно выраженной избирательностью болеутоляющего действия. Другие виды чувствительности (тактильную, температурную чувствительность, слух, зрение) в терапевтических дозах он не подавляет.
Механизм болеутоляющего действия морфина выяснен не полностью. Тем не менее есть все основания считать, что он складывается из следующих основных компонентов: 1) угнетения процесса межнейронной передачи болевых импульсов в центральной части афферентного пути и 2) нарушения субъективно-эмоционального восприятия, оценки боли и реакции на нее3.
Механизм болеутоляющего действия морфина обусловлен его взаимодействием с опиоидными рецепторами (р > к» 8), агонистом которых он является. Стимуляция морфином опиоидных рецепторов проявляется активацией эндогенной антиноцицептивной системы и нарушением межнейронной передачи Рис. 8.2. Снотворный мак - Papaver KJ
somniferum L. (содержит алкалоиды болевых стимулов на разных уровнях ЦНС. морфин, кодеин, папаверин и др.). Так, существенное значение имеет прямое

' Значение термина «алкалоид» см в разделе 1.3.
2 От греч. opos — сок. Получают опий вручную, надрезая незрелые маковые головки и затем собирая высохший на воздухе млечный сок.
3 За последние годы появились данные о наличии у опиоидов периферического компонента аналь-гетического действия. Так, было показано, что в эксперименте в условиях воспаления опиоиды снижают болевую чувствительность к механическому воздействию. Очевидно, опиоидергические процессы принимают участие в модуляции боли в воспаленных тканях.
Глава 8 ❖ Болеутоляющие (анальгезирующие) средства ❖ 197

В.А. СЕРТЮРНЕР (1783-1841). В 1806 г. выделил из снотворного мака алкалоид морфин. Это был первый алкалоид, полученный в очищенном виде.
угнетающее влияние морфина на спиналь-ные нейроны. При этом происходит нарушение межнейронной передачи возбуждения на уровне задних рогов спинного мозга. Важно также действие морфина на супраспинальные ядра, участвующие в нисходящем контроле активности нейронов задних рогов спинного мозга. В эксперименте показано, что введение морфина в некоторые из этих ядер (например, в околоводопроводное серое вещество, в ретикулярные парагигантоклеточное и гигантоклеточное ядра) вызывает анальгезию. Важность нисходящей системы доказывается также тем, что разрушение большого ядра шва в значительной степени снижает анальгетическое действие морфина. Таким образом, угнетающее влияние морфина на передачу болевых импульсов в спинном мозге с первичных афферентных волокон на вставочные нейроны склады-
вается из усиления нисходящих тормозных влияний и прямого угнетающего действия на межнейронную передачу в спинном мозге. Эти виды действия локализуются как на постсинаптических нейронах, так и на уровне пресинаптических окончаний. В последнем случае морфин, стимулируя пресинаптические опиоидные рецепторы окончаний первичных афферентов, уменьшает высвобождение медиаторов (например, глутамата, субстанции Р), принимающих участие в передаче ноцицептивных стимулов. Торможение постсинаптических нейронов обусловлено их гиперполяризацией (за счет активации постсинаптических К+-каналов). Нарушение морфином межнейронной передачи в спинном мозге снижает интенсивность импульсации, поступающей в восходящие афферентные пути, а также уменьшает двигательные и вегетативные реакции (рис. 8.3).
Изменение восприятия боли связано, по-видимому, не только с уменьшением поступления болевых импульсов к вышележащим отделам, но также с успокаивающим действием морфина. Последнее, очевидно, сказывается на оценке боли и ее эмоциональной окраске, что имеет важное значение для двигательных и вегетативных проявлений боли. Роль психического состояния для оценки болевых ощущений очень велика. Достаточно отметить, что положительный эффект плацебо при некоторых болях достигает 35—40%.
Успокаивающее действие морфина может быть связано с его влиянием на нейроны коры головного мозга, на активирующую восходящую ретикулярную формацию ствола головного мозга, а также на лимбическую систему и гипоталамус. Например, известно, что морфин угнетает реакцию активации коры головного мозга (подавляет десинхронизацию ЭЭГ на внешние раздражения), а также реакцию лимбической системы и гипоталамуса на афферентные импульсы.
Одно из типичных проявлений психотропного действия морфина — вызываемое им состояние эйфории1, которая заключается в повышенном настроении,
1 От греч. ей — хорошо, phero — переношу.
198 ❖ ФАРМАКОЛОГИЯ ❖ Частная фармакология
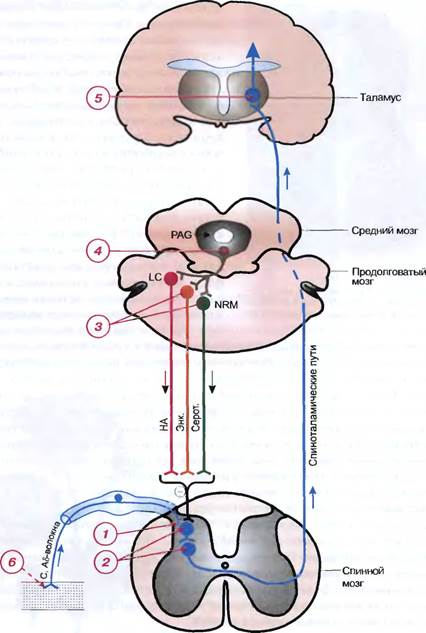
Рис. 8.3. Возможные точки приложения действия морфина.
Анальгетический эффект морфина обусловлен его стимулирующим влиянием на опиоидные рецепторы на разных уровнях ЦНС.
1 - влияние на пресинаптические рецепторы первичных афферентов (приводит к снижению высвобождения медиаторов, например субстанции Р, глутамата); 2 - влияние на постсинаптические рецепторы нейронов заднего рога спинного мозга, приводящее к угнетению их активности; 3,4 - активация антиноцицептивной системы среднего и продолговатого мозга (центральное серое вещество, ядра шва) усиливает нисходящее тормозное влияние на проведение болевых импульсов в задних рогах спинного мозга; 5 - угнетение межнейронной передачи болевых импульсов на уровне таламуса; 6 - при воспалении снижение чувствительности окончаний афферентных нервов. PAG - околоводопроводное серое вещество; LC - голубое пятно; NRM - большое ядро шва; НА - адренергические волокна; Энк. - энкефалин-ергические волокна; Се-рот. - серотонинергические волокна; минус - тормозное влияние.
Глава 8 ■> Болеутоляющие (анальгезирующие) средства -с- 199
1 От греч. dys — отрицание, phero — переношу.
2 Морфин получил свое название благодаря снотворному действию (в честь греческого бога сновидений Морфея).
ощущении душевного комфорта, положительном восприятии окружающей обстановки и жизненных перспектив независимо от реальной действительности. Особенно выражена эйфория при повторном применении морфина. Однако у некоторых людей отмечается обратное явление: плохое самочувствие, отрицательные эмоции (дисфория1).
В терапевтических дозах морфин вызывает сонливость, а при благоприятных условиях способствует развитию сна2. Сон, вызванный морфином, обычно поверхностный и легко прерывается внешними раздражителями.
Одним из проявлений центрального действия морфина служит снижение температуры тела, связанное с угнетением центра теплорегуляции, расположенного в гипоталамусе. Однако отчетливая гипотермия наблюдается только при введении больших доз морфина. Вместе с тем морфин может оказывать стимулирующее влияние па определенные центры гипоталамуса. В частности, это приводит к повышению выделения антидиуретического гормона (вазопрессина) и уменьшению диуреза.
Наблюдаемое при введении морфина (особенно в токсических дозах) сужение зрачков (миоз) также имеет центральный генез и связано с возбуждением центров глазодвигательного нерва. Последнее является, по-видимому, вторичным и возникает в результате воздействия морфина на вышележащие отделы ЦНС. Такое предположение основывается на том, что у декортицированных собак морфин не вызывает миоза.
Существенное место в фармакодинамике морфина занимает его действие на продолговатый мозг, и в первую очередь на центр дыхания. Морфин (начиная с терапевтических доз) угнетает центр дыхания, снижая его возбудимость к углекислоте и рефлекторным воздействиям. Сначала наступает урежение частоты дыханий, которое компенсируется увеличением их амплитуды. При повышении дозы до субтоксической ритм дыхания снижается еще больше, падают амплитуда одиночных дыханий и минутный объем. Нередко отмечается неправильный дыхательный ритм, возможно периодическое дыхание (при токсических дозах вещества). При отравлении морфином смерть наступает от паралича центра дыхания.
Морфин угнетает центральные звенья кашлевого рефлекса и обладает выраженной противокашлевой активностью.
На рвотный центр морфин, как правило, действует угнетающе. Однако в части случаев он может вызывать тошноту и рвоту. Связывают это с возбуждающим действием морфина на хеморецепторы пусковой зоны (trigger zone), расположенной на дне IV желудочка и активирующей центр рвоты (см. рис. 15.3). Центр блуждающих нервов морфин возбуждает, особенно в больших дозах. Возникает бра-дикардия. Насосудодвигательный центр практически не влияет. Спинномозговые рефлексы при введении морфина в терапевтических дозах обычно не меняются, в больших дозах — угнетаются.
Таким образом, влияние морфина на ЦНС довольно разнообразно (табл. 8.2).
Морфин оказывает выраженное влияние на многие гладкомышечные органы, содержащие опиоидные рецепторы. В отличие от алкалоидов опия изохинолино-вого ряда (например, папаверина) морфин стимулирует гладкие мышцы, повышая их тонус.
200 <■ ФАРМАКОЛОГИЯ > Частная фармакология
| Таблица 8.2. Основные эффекты морфина | |
| Угнетающие эффекты | Стимулирующие эффекты |
| Центральные | |
| Подавление боли Ссдативный и снотворный эффекты Угнетение центра дыхания Угнетение кашлевого рефлекса Небольшое угнетение центра теплорегуляции Снижение секреции гоналотропных гормонов | Эйфория Стимуляция центров глазодвигательных нервов (миоз) Стимуляция центров блуждающих нервов Повышение продукции пролактина и антидиуретического гормона Возможна стимуляция рецепторов пусковой зоны рвотного центра |
| Периферические | |
| Угнетение моторики желудка и пропуль-сивной перистальтики кишечника Угнетение секреции желез желудка, поджелудочной железы, кишечника | Повышение тонуса сфинктеров желудочно-кишечного тракта Повышение тонуса мышц кишечника Повышение тонуса сфинктера Одди (повышение давления в желчном пузыре/протоках и протоке поджелудочной железы) Повышение тонуса мышц бронхов Повышение тонуса сфинктеров мочеточников и мочевого пузыря |
Со стороны желудочно-кишечного тракта наблюдаются повышение тонуса сфинктеров и кишечника, снижение перистальтики кишечника, способствующей продвижению его содержимого, увеличение сегментации кишечника. Кроме того, уменьшаются секреция поджелудочной железы и выделение желчи. Все это замедляет продвижение химуса по кишечнику. Этому способствуют также более интенсивное всасывание воды из кишечника и уплотнение его содержимого. В итоге развивается запор (обстипация).
Морфин может существенно повышать тонус сфинктера Одди (сфинктер пе-ченочно-поджелудочной ампулы) и желчных протоков, что нарушает процесс поступления в кишечник желчи. Снижается и выделение панкреатического сока.
Морфин повышает тонус и сократительную активность мочеточников. Он также тонизирует сфинктер мочевого пузыря, затрудняя мочеотделение.
Под влиянием морфина повышается тонус бронхиальных мышц, что может быть связано как с его действием на опиоидные рецепторы мыши, так и с высвобождением гистамина.
Непосредственно на сосуды морфин практически не влияет.
В терапевтических дозах он, как правило, не изменяет уровень артериального давления. При увеличении дозы может вызывать небольшую гипотензию, которую относят за счет незначительного угнетения сосудодвигательного центра и высвобождения гистамина. На фоне действия морфина может развиться орто-статическая гипотензия.
Из желудочно-кишечного тракта морфин всасывается недостаточно хорошо. Кроме того, значительная его часть инактивируется в печени при первом про
Глава 8 Болеутоляющие (анальгезируюшие) средства <- 201
хождении через нее. В связи с этим для более быстрого и выраженного эффекта препарат обычно вводят парентерально. Длительность анальгезируюшего действия морфина 4—6 ч. Определяется она довольно быстрой биотрансформацией морфина в печени и выведением его из организма1. Через гематоэнцефалический барьер морфин проникает плохо (в ткани мозга попадает около 1% от введенной дозы). Морфин в неизмененном виде (10%) и его конъюгаты (90%) выделяются преимущественно почками и в небольшом количестве (7—10%) — желудочно-кишечным трактом, куда попадают с желчью.
В качестве одного из заменителей морфина иногда используют ом но по н (пантопон), представляющий собой смесь гидрохлоридов 5 алкалоидов опия как фенантреново-го (морфин, кодеин, тебаин), так и изохинолинового (папаверин, наркотин) ряда. Фар-макодинамика омнопона в целом аналогична таковой морфина. Одно из отличий заключается в том, что омнопон в меньшей степени, чем морфин, повышает тонус гладких мышц.
Помимо морфина, в медицинской практике нашли применение многие синтетические и полусинтетические препараты. Структуры некоторых из них приведены ниже.
К числу таких анальгетиков относятся производные пиперидина, имеющие аналогичный с морфином спектр рецепторного действия (р>к «8; табл. 8.3). Одним из широко распространенных в практике препаратов этого ряда является промедол (тримеперидина гидрохлорид). По обезболивающей активности он уступает морфину в 2—4 раза2. Продолжительность действия 3— 4 ч. Тошноту и рвоту вызывает реже, чем морфин. Несколько меньше угнетает центр дыхания.
Промедол (и сходный с ним по структуре и действию анальгетик меперидин) в организме подвергаются биотрансформации с образованием нейротоксичного N-деметилированного метаболита. Последний стимулирует ЦНС (возможны тремор, подергивания мышц, гиперрефлексия, судороги). Метаболит имеет длительный период «полужизни» (t|, = 15—20 ч). Поэтому промедол (и меперидин) рекомендуется применять только кратковременно (до 48 ч).
Date: 2015-07-01; view: 552; Нарушение авторских прав