
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Перший закон термодинаміки. Внутрішня енергія і засоби її зміни
|
|
Теоретичні відомості
Макросистемою називається система, що складається з великої кількості частинок. Термодинаміка – це розділ фізики, у якому розглядається поведінка макросистем з використанням понять і параметрів, що характеризують систему в цілому. Молекулярна або статистична фізика розглядає стан макросистеми на основі уявлень про молекулярну будівлю речовини. Стан макросистеми характеризують величинами, що називаються термодинамічними параметрами (тиск р, об’єм V, температура Т і інші). Стан системи є рівноважним, якщо всі параметри її мають визначені і сталі значення при незмінних зовнішніх умовах. Будь який реальний процес проходить через послідовність нерівноважних станів. Але якщо такий вплив здійснюється досить повільно, то можна сказати, що процес проходить через послідовність рівноважних станів. Такий процес називають квазістатичним.
Температура – це фізична величина, що характеризує стан термодинамічної рівноваги макросистеми. Якщо при встановленні теплового контакту між тілами одне з тіл передає енергію іншому за допомогою теплопередачі, то вважають, що перше тіло має більшу температуру, ніж друге. Будь який метод виміру температури вимагає встановлення температурної шкали. Для цього використовують деякі особливі точки. За міжнародною угодою температурну шкалу будують по тройній точці води (Ттр). У термодинамічній шкалі температур (шкалі Кельвіна) приймається по визначенню, що Ттр = 273,15 К. При такому значенні Ттр інтервал між точками плавлення льоду і кипіння води практично дорівнює 100 кельвін, і температури цих точок дорівнюють приблизно 273,15 і 373,15 К. При цьому варто враховувати, що 1К=1°С. Температура t по шкалі Цельсія зв'язана з температурою по шкалі Кельвіна співвідношенням:
t = Т – 273,15.
Температуру Т = 0 називають абсолютним нулем, йому відповідає t=–273,15 °С.
Внутрішня енергія – це енергія частинок, з яких складається речовина. Вона містить у собі:
- сумарну кінетичну енергію хаотичного руху молекул у Ц–системі;
- власну потенціальну енергію взаємодії всіх молекул;
- внутрішню енергію молекул, атомів і ядер.
Внутрішня енергія є функцією стану. При зміні стану збільшення внутрішньої енергії визначається тільки кінцевим і початковим станами і не залежить від процесу, при якому система переводиться з одного стану в інший. Способи зміни внутрішньої енергії:
1. виконати над системою роботу;
2. передати системі кількість теплоти Q.
Кількістю теплоти називається міра зміни внутрішньої енергії при теплопередачі.
Теплопередачею називається сукупність мікроскопічних процесів, що приводять до передачі енергії від одного тіла до іншого.
Закон збереження енергії з урахуванням теплових процесів називається першим початком термодинаміки.
Якщо над системою виконали роботу 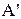 і передали їй кількість теплоти Q, то, відповідно до закону збереження енергії, збільшення внутрішньої енергії буде дорівнює алгебраїчній сумі роботи зовнішніх сил над системою і переданого їй кількості теплоти:
і передали їй кількість теплоти Q, то, відповідно до закону збереження енергії, збільшення внутрішньої енергії буде дорівнює алгебраїчній сумі роботи зовнішніх сил над системою і переданого їй кількості теплоти:
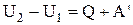 .
.
Якщо система виконує роботу А проти зовнішніх сил, то з урахуванням третього закону Ньютона можна записати: 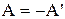 . Тоді останню формулу можна переписати у вигляді:
. Тоді останню формулу можна переписати у вигляді:
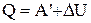 .
.
Отримане вираження є математичним записом першого початку термодинаміки: Кількість теплоти, що передана макросистемі, йде на збільшення її внутрішньої енергії і на здійснення системою роботи над зовнішніми тілами. У диференціальній формі перший закон термодинаміки має вигляд:
 .
.
 Обчислимо елементарну роботу газу
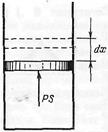
Обчислимо елементарну роботу газу 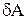 при нескінченно малому квазістатичному розширенні, у якому його об’єм збільшується на dV. Нехай газ знаходиться в циліндрі під поршнем. Сила тиску газу на поршень дорівнює
при нескінченно малому квазістатичному розширенні, у якому його об’єм збільшується на dV. Нехай газ знаходиться в циліндрі під поршнем. Сила тиску газу на поршень дорівнює
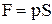 ,
,
де S – площа поршня.
Якщо поршень переміститься на відстань dx, то газ виконає роботу:
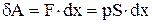
або враховуючи, що 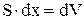 , одержуємо:
, одержуємо:
 .
.
Повна робота при переході системи зі стану 1 у стан 2 визначається з вираження:
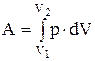 .
.
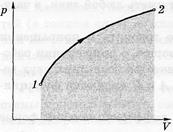
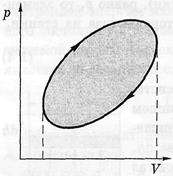 Геометрично роботу можна визначити як площу фігури під графіком у системі pV. З графіка видно, що робота істотно залежить від процесу, при якому система переводиться зі стану 1 у 2, оскільки площа під кривою 1–2 залежить від вигляду кривої, тобто від процесу. Якщо в результаті змін макросистема повертається у вихідний стан, то кажуть, що вона зробила круговий процес або цикл. На діаграмі pV такий процес має вигляд замкнутої кривої. Робота, чинена системою за цикл, чисельно дорівнює площі замкненого циклу. При цьому, якщо точка, що зображує стан системи, описує цикл за годинною стрілкою, то робота системи А > 0. Якщо ж проти руху стрілки, то А < 0.
Геометрично роботу можна визначити як площу фігури під графіком у системі pV. З графіка видно, що робота істотно залежить від процесу, при якому система переводиться зі стану 1 у 2, оскільки площа під кривою 1–2 залежить від вигляду кривої, тобто від процесу. Якщо в результаті змін макросистема повертається у вихідний стан, то кажуть, що вона зробила круговий процес або цикл. На діаграмі pV такий процес має вигляд замкнутої кривої. Робота, чинена системою за цикл, чисельно дорівнює площі замкненого циклу. При цьому, якщо точка, що зображує стан системи, описує цикл за годинною стрілкою, то робота системи А > 0. Якщо ж проти руху стрілки, то А < 0.
Date: 2015-07-01; view: 747; Нарушение авторских прав