Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Диабетическая нефропатия
|
|
Заболевания почек достаточно часто осложняют течение сахарного диабета, диабетическая нефропатия является причиной высокой инвалидизации и смертности. В Мире почечная недостаточность является причиной смертности среди больных СД I и II типов соответственно в 53 и 3 % случаев. Поэтому лабораторный контроль за поражением почек должен быть включен в обследование больных сахарным диабетом. Традиционная классификация диабетической нефрропатии по Mognsen выделяет 5 стадий (таблица 17).
Таблица 17.
| Стадии диабетической нефропатии (по Mognsen) | ||
| Стадия | Клинико-лабораторная характеристика | Сроки развития |
| 1. Гиперфунк-ция почек | n увеличение скорости клубочковой фильтрации (СКФ) (> 140 мл/мин) n увеличение почечного кровотока n гипертрофия почек n нормоальбуминурия (< 30 мг/сутки) | развивается в дебюте сахарного диабета |
| 2. Начальные структурные изменения ткани почек | n утолщение базальных мембран капилляров клубочков n расширение мезангиума n сохраняется высокая СКФ n нормоальбуминурия | 2 - 5 лет от начала диабета |
| 3. Начинаю-щаяся нефропатия | n микроальбуминурия (от 30 до 300 мг/сутки) n СКФ высокая или нормальная n нестойкое повышение артериального давления | 5 - 15 лет от начала диабета |
| 4. Выраженная нефропатия | n протеинурия (более 500 мг/сутки) n СКФ нормальная или умеренно сниженная n артериальная гипертензия | 10 - 25 лет от начала диабета |
| 5. Уремия | n снижение СКФ < 10 мл/мин n артериальная гипертензия n симптомы интоксикации | более 20 лет от начала диабета или 5-7 лет от появления протеинурии |
В настоящее время Минздрав России утвердил более простую, но клинически более отчетливую классификацию, которая включает 3 стадии развития диабетической нефропатии (таблица 18)
Таблица 18.
| Новая классификация стадий диабетической нефропатии |
|
|
|
Длительное время диабетическая нефропатия протекает бессимптомно. В то же время многочисленные работы показывают, что на доклинических стадиях имеет место увеличение объема клубочков почек, видимо за счет увеличения количества мезангиальных клеток и матрикса, изменяются стуктуры подоцитов и их количество. Это сопровождается утолщением базальной мембраны клубочков у больных как СД I типа, так и больных СД II типа.
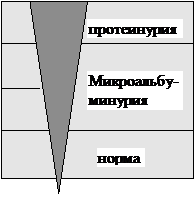
Первым признаком диабетической нефропатии является развитие микроальбуминурии, по мере прогрессирования болезни она сменяется протеинурией. Экскреция альбумина с мочой в норме менее 20 мкг/мин, микроальбуминемия определяется как экскреция альбумина с мочой до 200 мкг/мл, что соответствует содержанию белка от 20 до 300 мг/л утренней мочи или от 30 до 300 мг/сутки. Этот уровень не определяется с помощью тест-полосок «сухая химия». Для выявления микроальбуминурии используются специальные диагностические полоски. При экскреции свыше 200 мкг белка/мин диагностируется протеинурия (рис. 20, таблица 19).
| |||||||
 | |||||||
 | |||||||
| |||||||
Рис. 20. Качественные этапы экскреции альбумина с мочой.
Микроальбуминурия является достаточно ранним признаком нарушения функции клубочков, в этот период по оценкам многих клиницистов болезнь поддается медикаментозному лечению. Уровень экскреции альбумина с мочой определяется в основном структурной и функциональной целостностью гломерулярного фильтра, отделяющего просвет клубочкового капилляра от мочевого пространства, и величиной внутрикапиллярного клубочкового давления.
Таблица 19.
| Классификация альбуминурии | |||
| Уровень альбу | Экскреция альбумина с мочой | Концентрация | |
| минурии | В утренней порции | за сутки | альбумина в моче |
| Нормоальбуминурия | < 20 мкг/мин | < 30 мг | < 20 мг/л |
| Микроальбуминурия | 20 - 200 мкг/мин | 30 - 300 мг | 20 - 200 мг/л |
| Макроальбуминурия | > 200 мкг/мин | > 300 мг | > 200 мг/л |
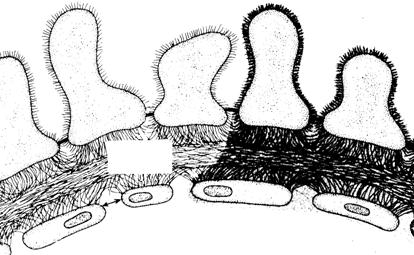
Основой гломерулярного фильтра является клубочковая базальная мембрана (рис. 21). Со стороны просвета капилляра базальная мембрана выстлана слоем эндотелиальных клеток, имеющих естественные отверстия - фенестры - диаметром около 150 Å. Со стороны мочевого пространства базальная мембрана покрыта слоем эпителиальных клеток (подоцитов), имеющих дополнительные отростки - педикулы, располагающиеся с образованием пространства щелевидной формы. Эндотелиальные и эпителиальные клетки выстланы отрицательно заряженным клубочковым полианионом. Гломерулярный фильтр является эффективным препятствием для фильтрации молекул с большой молекулярной массой, в частности, для молекул белка. При диабете происходит гликирование сиалогликопротеинов на гломерулярной базальной мембране клубочкового полианиона, что ведет к нейтрализации общего отрицательного заряда гломерулярного фильтра. Эта потеря заряда способствует более легкому прохождению в ультрафильтрат отрицательно заряженных молекул альбумина. Способствует микроальбуминемии повышение внутриклубочкового давления, которое развивается первично по отношению к увеличению системного АД, так как почки при диабете теряют эффективность работы системы ауторегуляции внутрипочечного давления.
| Рис. 21. При диабете происходит гликирование поверхностных белков мембран эндотелиальных и эпителиальных клеток (подоцитов) с потерей поверхностного заряда. В результате полиэлектролит альбумин проникает через фильтр клубочков почек |
Если в суточной моче концентрация альбумина выше 30 мг и эти значения повторяются несколько раз, то необходимо проводить лечение, так как данные изменения характерны для начинающейся диабетической нефропатии.
По мере прогрессирования поражения почек при диабете развивается выраженная протеинурия. Тщательный контроль за уровнем глюкозы в крови и лечение любых форм гипертонии может приостановить микроальбуминемию и предупредить развитие манифестной почечной недостаточности. Согласно рекомендациям Американской диабетической ассоциации (1997) и Европейской группы по изучению СД (1999) исследование микроальбуминурии входит в перечень обязательных рутинных методов обследования больных СД I и II типов (таблица 20).
Таблица 20.
| Рекомендации для скрининга на микроальбуминурию | |
| Категория больных | Начало скринирования |
| Больные СД 1, заболевшие в раннем детском возрасте | ежегодно с возраста 10-12 лет |
| Больные СД 1, заболевшие в пубертатном возрасте | при постановке диагноза и далее раз в год |
| Больные СД 1, заболевшие в постпубертатном возрасте | спустя 5 лет с дебюта диабета |
| Больные СД 2 | при постановке диагноза и далее раз в год |
Существуют международные программы по диагностике и контролю течения диабетических нефропатий, приводим (рис. 22) алгоритм скрининга и мониторирования диабетической нефропатии, принятый Сент- Винсентской декларацией (1989г.).
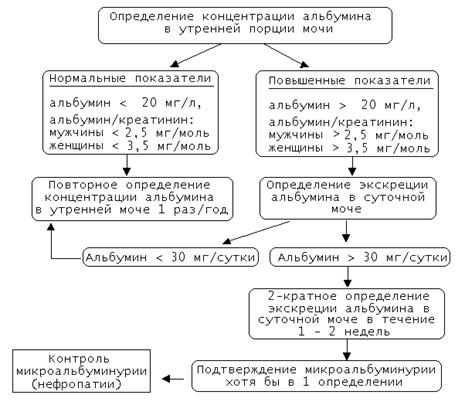
Рис. 22. Программа скрининга и мониторинга диабетической нефропатии (Сент-Винсентская декларация (1989г.).
Скорость клубочковой фильтрации (СКФ) является ранним проявлением влияния гипергликемии на функцию почек. При СД I типа прежде всего возникает гиперфильтрация, то есть СКФ выше 140мл/мин. Гиперфильтрация приводит к дальнейшему повреждению почек, однако может коррегироваться оптимальным гликемическим контролем. С увеличением длительности заболевания СКФ прогрессивно снижается. Скорость ее снижения увеличивается с развитием протеинурии и находится под влиянием артериального давления. Mogensen подсчитал, что при сахарном диабете с нормальной СКФ с началом протеинурии этот показатель снижается со скоростью 11 мл/мин в год. Уровень креатинина в сыворотке начинает повышаться лишь через год после появления протеинурии, когда СКФ снижена на 50 - 75 %.
Наиболее точным методом определения СКФ является радиоизотопное исследование почечной функции с использованием 51Cr-ЭДТА. Несмотря на точность, эта методика требует соответствующего оборудования, больших затрат и времени. Определение клиренса креатинина по пробе Реберга-Тареева (клиренс эндогенного креатинина за сутки) является приемлемой для определения СКФ, особенно при уровне ниже 100 мл/мин/1,73 м2. Надежным сывороточным показателем клубочковой фильтрации является цистатин С - внеклеточный ингибитор протеаз. Этот компонент выводится из организма только путем фильтрации в почках, на его уровень не влияет пол, возраст, масса тела.
Экономические аспекты диагностики диабетической нефропатии. Лечение больных СД с терминальной стадией почечной недостаточности требует колоссальных затрат. В США стоимость лечения 1 больного на гемодиализе составляет 40 – 45 тыс. $ в год. Используя ту же сумму денег, можно провести скрининг на микроальбуминурию у 4000 больных СД I и II типов. В то же время, по данным опроса краевых, областных и городских эндокринологов (диабетологов) различных регионов России, определение микроальбуминурии в России проводится на постоянной основе в 20 % регионов, проводится только в научных целях – в 20 % регионов, не проводится в 60 % регионов.
Date: 2015-07-17; view: 802; Нарушение авторских прав