
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Гипотензивные средства 3 page
|
|
Механизмы эрекции
Белочная оболочка пещеристых и губчатого тел полового члена состоит из сети эластических волокон, на кото-
рой покоятся коллагеновые. Особенности гистологического строения белочной оболочки определяются ее локализаций и функцией. Белочная оболочка пещеристых тел состоит из двух слоев — внутреннего и наружного. Циркулярный внутренний слой поддерживает пещеристое тело снаружи. Кроме того, от него внутрь отходят соединительнотканные тяжи, образующие трабекулы пещеристого тела. Продольный наружный слой проходит от головки к ножкам полового члена и вплетается в надкостницу нижней ветви лобковой кости. На вентральной поверхности (между пятью и семью часами условного циферблата) наружный слой белочной оболочки отсутствует. Между внутренним и наружным слоем белочной оболочки на небольшом расстоянии проходят эмиссарные вены, затем они под острым углом прободают наружный слой. Ветви дорсальной артерии полового члена прободают белочную оболочку прямо перпендикулярно к продольной оси полового члена, заключены в соединительнотканный футляр. Наружный слой белочной оболочки, вероятно, способствует сдавлению вен во время эрекции. В отличие от пещеристых тел у губчатого тела полового члена наружного слоя белочной оболочки нет, поэтому во время эрекции давление в нем почти не повышается.
Основной источник кровоснабжения полового члена — парная внутренняя половая артерия. Ее конечные ветви — артерия луковицы полового члена, дорсальная и глубокая артерии полового члена. Первая кровоснаб-жает губчатое тело, вторая — головку полового члена, третья — пещеристые тела. Эти артерии часто анасто-мозируют между собой. В отдельных случаях большая часть полового члена кровоснабжается добавочными половыми артериями, отходящими от наружной подвздошной или запирательной артерий. Венозный отток от губчатого и пещеристых тел полового члена начинается в подоболочечных венах, которые сливаются в эмиссарные вены. От головки полового члена кровь оттекает в основном по глубокой дорсальной вене полового члена, от губчатого тела — по огибающей и уретральной венам, а также по вене луковицы полового члена. Венозный отток от пещеристых тел сложнее. От дис-тальной и средней частей кровь по глубокой дорсальной вене полового члена оттекает в предстательное венозное сплетение, от проксимальной части — по пещеристым и ножковым венам полового члена в предстательное венозное сплетение и во внутреннюю половую вену. В головке полового члена анастомозирует множество вен разного калибра. Кровь от кожи и подкожной клетчатки оттекает по поверхностным дорсальным венам полового члена, которые впадают в большие подкожные вены ног.
Первые исследования кровоснабжения полового члена были проведены на трупах и с помощью сцинтигра-фии с шХе у добровольцев. При этом было показано, что во время эрекции усиливается артериальный кровоток. Позже в экспериментах с электростимуляцией нервов у собак и обезьян, а также в исследованиях на доброволь-
Глава 47. Нарушения половой функции у мужчин

|
цах, у которых эрекцию вызывали интракавернозными инъекциями папаверина, была окончательно установлена роль пещеристых тел, артерий и вен полового члена в эрекции.
Выделяют несколько фаз эрекции (табл. 47.1, рис. 47.2). В исследованиях со зрительной эротической стимуляцией и в фазе быстрого сна выявлена синергичная активность луковично-губчатых и седалищно-пещеристых мышц. Раздельная электростимуляция нервов пещеристых тел полового члена и полового нерва у животных, а также интракавернозные инъекции папаверина у животных и человека помогли установить роль вегетативных и соматических нервных волокон в эрекции. Вегетативные волокна ответственны за сосудистую фазу эрекции — наполнение пещеристых тел кровью. После наступления полной эрекции импульсация по соматиче-
Таблица 47.1. Фазы эрекции
1. Фаза покоя
Артериальный и венозный кровоток минимален; по газовому составу кровь схожа с венозной. Скорость кровотока 0,5—8 мл/мин
2. Латентная фаза (фаза наполнения)
Приток крови по внутренней половой артерии и в систолу, и в диастолу увеличивается. Давление во внутренней половой артерии уменьшается, а в пещеристых телах не меняется. Половой член несколько удлиняется
3. Фаза набухания
Давление в пещеристых телах увеличивается. Половой член удлиняется и увеличивается в диаметре. По мере повышения давления в пещеристых телах приток артериальной крови уменьшается. Как только давление в пещеристых телах превышает диастолическое АД, кровоток сохраняется только в систолу
4. Фаза полной эрекции
Давление в пещеристых телах может достигать 80—90% систолического АД. Давление во внутренней половой артерии повышается, но остается чуть ниже системного. Приток артериальной крови намного меньше, чем в фазе наполнения, но все же больше, чем в фазе покоя. Хотя большинство вен сдавлено, венозный отток несколько больше, чем в фазе наполнения. Кровь в пещеристых телах по газовому составу почти соответствует артериальной
5. Фаза ригидной эрекции
В результате сокращения седалищно-пещеристых мышц давление в пещеристых телах намного превышает систолическое АД и эрекция становится ригидной. Кровоток во внутренней половой артерии почти прекращается. Однако эта фаза крат-ковременна, поэтому ишемического повреждения тканей не происходит
6. Фаза детумесценции
После эякуляции или прекращения эротической стимуляции импульсация по симпатическим нервным волокнам способствует сокращению гладких мышц вокруг ячеек пещеристых тел и артериол. Артериальный кровоток соответствует таковому в фазе покоя, вены вновь открываются, и большая часть крови выталкивается из ячеек. Длина и диаметр полового члена возвращаются к исходным
Рисунок 47.2. Фазы эрекции (обозначены цифрами) (данные экспериментов со стимуляцией нервов у обезьян).
ским волокнам вызывает сокращение седалищно-пе-щеристых мышц. Они сдавливают проксимальные отделы пещеристых тел, давление в которых становится гораздо выше систолического АД. Наступает фаза ригидной эрекции. В естественных условиях эта фаза достигается при мастурбации или во время полового акта, но возможна и при небольшом сгибании полового члена без сокращения седалищно-пещеристых мышц. Как показали эксперименты на животных, в фазе ригидной эрекции кровоток во внутренней половой артерии значительно уменьшен, но поскольку эта фаза кратковременна, ише-мического повреждения тканей не происходит.
Кровоснабжение головки полового члена меняется по-другому. Как и в пещеристых телах, в ней усиливается артериальный кровоток. Однако из-за отсутствия белочной оболочки венозный отток в фазе полной эрекции сохраняется, поэтому головка полового члена становится своего рода артериовенозным свищом. Давление в головке полового члена и глубокой дорсальной вене полового члена повышается за счет сдавления этой вены между увеличенными пещеристыми телами и глубокой фасцией полового члена, а также между пещеристыми телами и лобковыми костями. Увеличению головки полового члена способствует также то, что в фазе ригидной эрекции большинство вен полностью пережато.
На основании данных аутопсий в середине XX в. появилась гипотеза о том, что в артериях и венах полового члена есть валики. Одновременное сокращение или расслабление этих валиков регулирует сброс крови из артерий в вены и приводит к эрекции или детумесценции. Позже эту гипотезу опровергли, так как эти валики не были обнаружены у новорожденных. Возможно, описанные структуры были не чем иным, как атеросклеро-тическими бляшками. Все вопросы об анатомических изменениях во время эрекции были окончательно сняты в 1980-х гг. после экспериментальных исследований, в которых использовалась электронная микроскопия. В
Глава 47. Нарушения половой функции у мужчин
 покое в пещеристых телах видны спавшиеся ячейки, суженные артерии и артериолы и открытые венулы, дренирующие венозные сплетения под белочной оболочкой. Во время эрекции артериолы, артерии и ячейки пещеристых тел заметно расширены, а подоболо-чечные и эмиссарные вены сдавлены. На основании этих работ, а также исследований, в которых применялись интракавернозные инъекции папаверина, было предположено, что ключевую роль в эрекции, по-видимому, играют гладкие мышцы артериол и трабекул пещеристых тел.
покое в пещеристых телах видны спавшиеся ячейки, суженные артерии и артериолы и открытые венулы, дренирующие венозные сплетения под белочной оболочкой. Во время эрекции артериолы, артерии и ячейки пещеристых тел заметно расширены, а подоболо-чечные и эмиссарные вены сдавлены. На основании этих работ, а также исследований, в которых применялись интракавернозные инъекции папаверина, было предположено, что ключевую роль в эрекции, по-видимому, играют гладкие мышцы артериол и трабекул пещеристых тел.
В покое гладкие мышцы сокращены, что, возможно, объясняется симпатическими влияниями. Высокое сопротивление, которое создают спавшиеся ячейки пещеристых тел вместе с извитыми суженными артериями и артериолами, обеспечивает минимальный кровоток в ячейках. Когда гладкие мышцы артерий, артериол и трабекул расслабляются (например, после введения а-адре-ноблокаторов или вазодилататоров), растяжимость артерий, артериол и ячеек пещеристых тел увеличивается, а сопротивление кровотоку резко уменьшается, в результате ячейки пещеристых тел заполняются кровью и расширяются. Половой член удлиняется и увеличивается в диаметре. Увеличение размеров полового члена ограничивает белочная оболочка. Между наполненными кровью ячейками пещеристых тел и белочной оболочкой сдавливаются подоболочечные вены. Дальнейшее расширение ячеек приводит к сдавлению эмиссарных вен и снижению оттока венозной крови до минимума (рис. 47.3). Поскольку приток артериальной крови к половому члену значительно возрастает только во время эрекции, сброс артериальной крови в покое не нужен. Следова-
тельно, даже если описанные в сосудах валики и существуют, то они бесполезны.
Гормональная регуляция
Для полового развития по мужскому типу необходимы андрогены. Если тестостерон регулирует секрецию гона-дотропных гормонов и сперматогенез, то дигидротесто-стерон обеспечивает все прочие проявления полового развития у мужчин, в том числе оволосение по мужскому типу, развитие скелетных мышц, а также угри и андроге-нетическую алопецию. Андрогены влияют на функцию гипоталамуса — одного из высших центров эрекции. Кроме того, они могут влиять на синаптическую проводимость, в том числе накопление, синтез, обратный захват и высвобождение медиаторов, а также чувствительность рецепторов. У взрослых мужчин при дефиците андрогенов снижается половое влечение и нарушается эмиссия. При этом ночные эрекции возникают реже и уменьшается их выраженность. Однако, как показали исследования, после отмены андрогенов у больных с ги-погонадизмом эрекция при зрительной эротической стимуляции сохраняется. Таким образом, андрогены, вероятно, способствуют эрекции, но необязательны для ее возникновения. В возрасте старше 70 лет отчасти из-за угасания функции яичек, отчасти из-за нарушений в ги-поталамо-гипофизарно-гонадной системе начинает неуклонно снижаться секреция тестостерона. Каковы максимальные уровни андрогенов, при превышении которых половая активность больше не увеличивается, не известно. Однако известно, что введение тестостерона у мужчин с нормальной секрецией андрогенов повышает по-
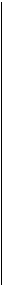

Рисунок 47.3. Механизм эрекции. А. В фазе покоя артерии, артериолы и ячейки пещеристых тел полового члена сужены. Вены между ячейками и под белочной оболочкой раскрыты, кровь свободно оттекает по эмиссарным венам. Б. Во время эрекции гладкие мышцы трабекул и артериол расслабляются, благодаря чему кровь начинает активно поступать в легко растяжимые ячейки. Большая часть вен сдавлена расширенными ячейками и нерастяжимой белочной оболочкой. Это касается даже относительно крупных эмиссарных вен. Отток венозной крови минимален.
Глава 47. Нарушения половой функции у мужчин
ловое влечение. Чтобы определить, существуют ли эти максимальные уровни, и если да, то как они меняются с возрастом, нужны дополнительные исследования.
Нервная регуляция
В нервной регуляции эрекции участвуют адренергиче-ские и холинергические нейроны, а также, как недавно показано, нитрергические нейроны. Норадрена-лин обеспечивает сокращение гладких мышц пещеристых тел, что приводит к детумесценции. Ацетилхолин тормозит симпатические влияния на уровне вставочных нейронов и способствует высвобождению окиси азота (N0) эндотелием (образуется из аргинина под действием NO-синтазы). Все это обеспечивает расслабление гладких мышц пещеристых тел и эрекцию.
Роль нитрергических нейронов была выяснена сравнительно недавно. Оказалось, что при электростимуляции таких нейронов in vitro высвобождается N0, накапливается цГМФ и расслабляются гладкие мышцы пещеристых тел кролика. Было показано также, что раздражение определенных волокон, не содержащих классические вегетативные медиаторы (так называемых неадре-нергических, нехолинергических волокон), приводит к расслаблению гладких мышц пещеристых тел человека; этот эффект подавляется веществами, блокирующими синтез или действие NO. Сходные данные получены и на собаках. NO-синтаза обнаружена в волокнах, иннер-вирующих гладкие мышцы сосудов и внутренних органов; возможно, тормозные влияния таких волокон на эти мышцы также опосредованы NO При иммуноги-стохимическом исследовании биоптатов полового члена человека оказалось, что содержание NO-синтазы в нервах пещеристых тел полового члена после стандартной радикальной простатэктомии заметно снижено. Кроме того, не исключено, что на эрекцию влияют вещества, которые высвобождаются эндотелием в просвет ячеек пещеристых тел, в частности простагландины, NO (ранее назывался эндотелиальным фактором расслабления сосудов) и эндотелины (мощные факторы вазоконстрик-ции, вырабатываемые эндотелием). И нитраты, и N0 активируют гуанилатциклазу в гладких мышцах сосудов и повышают содержание цГМФ в клетках.
Понять физиологию эрекции, усовершенствовать диагностику и тактику лечения помогли интракаверноз-ные инъекции вазодилататоров. Лекарственные средства, вызывающие эрекцию и детумесценцию, приведены в табл. 47.2. Хотя в высоких дозах действие препаратов несколько меняется, большинство веществ, вызывающих эрекцию, расслабляют гладкие мышцы, а вызывающих детумесценцию — их сокращают.
Механизмы сокращения и расслабления гладких мышц
Строение гладкомышечных клеток и поперечнополосатых мышечных волокон сходно. Отличие состоит толь-
ко в том, что в гладкомышечных клетках нити актина и миозина расположены беспорядочно. Легкие цепи миозина обеспечивают связывание миозина с актином. Сокращение гладких мышц регулируется кальцием. Когда уровень свободного кальция в цитоплазме возрастает с ба-зального (120—270 ммоль) до 500—700 ммоль, Са2+-каль-модулиновый комплекс связывается с киназой легких цепей миозина. Активированная киназа фосфорилиру-ет легкую цепь миозина, запускает образование акто-миозиновых мостиков и мышечное сокращение. Как только уровень свободного кальция падает до базально-го, Са2+-кальмодулиновый комплекс распадается, киназа легких цепей миозина инактивируется. Дефосфорилиро-вание легких цепей миозина препятствует образованию актомиозиновых мостиков и способствует расслаблению гладкомышечных клеток.
Механизмы внутриклеточной передачи сигнала
Пептидные гормоны и многие производные аминокислот не могут проникать через мембраны клеток-мишеней, поэтому они связываются с определенными мембранными рецепторами. Именно рецепторы запускают реакции, обеспечивающие преобразование внеклеточного сигнала во внутриклеточный и приводящие к изменению функции клеток-мишеней. Связывание рецептора с лигандом вызывает конформационные изменения в рецепторе, что прямо или косвенно влияет на каскад молекулярных превращений, которые проявляются в виде биологической реакции. Прямая активация происходит, когда рецептор представляет собой фермент или ионный канал. Косвенная активация требует участия дополнительных факторов. Так, для активации некоторых эффекторных молекул (в том числе ферментов и ионных каналов) нужны G-белки. Активированные ферменты образуют внутриклеточные медиаторы (по-
Таблица 47.2. Вещества, вызывающие эрекцию и детумесценцию
Стимуляторы эрекции _______ Стимуляторы детумесценции
Вазоактивный интестиналь- Адреналин
ный полипептид3 Гуанетидин
Верапамил Дофамин
Имипрамин Метараминол
Кальцитониноподобный пеп- Норадреналин
ТИД Фенилэфрин
Моксизилит Эфедрин
Нитроглицерин и доноры NO
Папаверин3
Простагландин Е, и алпроста-
дил
Сидценафил
Феноксибензамин
Фентоламин3
3 В том числе в комбинации с другими веществами.
Глава 47. Нарушения половой функции у мужчин
 средники), которые переносят сигнал в цитоплазму. Основные вторые посредники — цАМФ, цГМФ, инози-тол-1,4,5-трифосфати 1,2-диацилглицерин. Ион кальция считают третьим посредником, так как повышение его концентрации в цитоплазме зависит от инози-тол-1,4,5-трифосфата. В процессе эрекции и детумес-ценции передача сигнала может происходить по любому из перечисленных путей. Например, растворимый цГМФ — второй посредник для NQ цАМФ — второй посредник для простагландина Е,, вазоактивного интести-нального полипептида и кальцитониноподобного пептида. Норадреналин, фенилэфрин и эндотелины, вероятно, активируют фосфолипазу С, которая катализирует образование 1,2-диацилглицерина и инозитол-1,4,5-три-фосфата. Последний, в свою очередь, способствует повышению внутриклеточной концентрации ионов кальция и сокращению гладких мышц. Расслабление гладких мышц вызывают цАМФ и цГМФ, поскольку они активируют ионные каналы и снижают внутриклеточную концентрацию ионов кальция. Под действием фосфо-диэстераз цАМФ и цГМФ превращаются в аденозинмо-нофосфат и гуанозинмонофосфат соответственно. К настоящему времени известны 10 типов фосфодиэстеразы. В половом члене в большом количестве содержится фос-фодиэстераза типа V, которая расщепляет гуанозинмонофосфат. При импотенции с успехом применяется ингибитор фосфодиэстеразы типа V силденафил.
средники), которые переносят сигнал в цитоплазму. Основные вторые посредники — цАМФ, цГМФ, инози-тол-1,4,5-трифосфати 1,2-диацилглицерин. Ион кальция считают третьим посредником, так как повышение его концентрации в цитоплазме зависит от инози-тол-1,4,5-трифосфата. В процессе эрекции и детумес-ценции передача сигнала может происходить по любому из перечисленных путей. Например, растворимый цГМФ — второй посредник для NQ цАМФ — второй посредник для простагландина Е,, вазоактивного интести-нального полипептида и кальцитониноподобного пептида. Норадреналин, фенилэфрин и эндотелины, вероятно, активируют фосфолипазу С, которая катализирует образование 1,2-диацилглицерина и инозитол-1,4,5-три-фосфата. Последний, в свою очередь, способствует повышению внутриклеточной концентрации ионов кальция и сокращению гладких мышц. Расслабление гладких мышц вызывают цАМФ и цГМФ, поскольку они активируют ионные каналы и снижают внутриклеточную концентрацию ионов кальция. Под действием фосфо-диэстераз цАМФ и цГМФ превращаются в аденозинмо-нофосфат и гуанозинмонофосфат соответственно. К настоящему времени известны 10 типов фосфодиэстеразы. В половом члене в большом количестве содержится фос-фодиэстераза типа V, которая расщепляет гуанозинмонофосфат. При импотенции с успехом применяется ингибитор фосфодиэстеразы типа V силденафил.
Ионные каналы
В изолированных гладкомышечных клетках пещеристых тел и в культивированных гладкомышечных клетках обнаружены потенциалзависимые кальциевые каналы L-типа (медленные кальциевые каналы). По некоторым данным, сокращение гладкомышечных клеток под действием фенилэфрина и эндотелинов обусловлено как поступлением ионов кальция в клетку через кальциевые каналы, так и мобилизацией внутриклеточного кальция, а сокращение под действием калия хлорида — только входящим кальциевым током. Уже известны 4 подтипа калиевых каналов в гладкомышечных клетках пещеристых тел: кальций-зависимые, АТФ-зависимые, потенциал-зависимые каналы задержанного выпрямления и каналы быстрого кратковременного тока (1А). Не исключено, что в расслаблении гладких мышц, опосредованном цАМФ, участвуют кальций-зависимые калиевые каналы.
Межклеточные взаимодействия
Щелевые контакты — это водные межклеточные каналы, соединяющие цитоплазму соседних клеток и присутствующие во многих тканях. Миллионы гладкомышечных клеток пещеристых тел иннервированы достаточно скудно, поэтому решающая роль в межклеточных взаимодействиях принадлежит именно щелевым контактам, которые и обеспечивают согласованную работу отдельных клеток. У человека взаимодействие между гладко-
мышечными клетками пещеристых тел, вероятно, регулирует мышечное сокращение, опосредованное <х,-адре-норецепторами и эндотелинами. Возможно, импотенция в ряде случаев может быть обусловлена дефектом белка щелевых контактов коннексина-43.
ИМПОТЕНЦИЯ
Нарушения половой функции у мужчин — это заболевания, делающие половую жизнь невозможной или неполноценной. К ним относят импотенцию, нарушения эмиссии и эякуляции, а также аноргазмию. Импотенция — неспособность достичь или поддержать достаточную для полового акта эрекцию. Об импотенции говорят, когда описанные нарушения наблюдаются более чем в половине попыток полового акта в течение 6 мес.
Эпидемиология
По данным Массачусетского исследования мужского старения, те или иные нарушения эрекции отметили 52% опрошенных мужчин в возрасте 40—70 лет: у 17% нарушения были легкими, у 25% — среднетяжелыми, у 10% — эрекция отсутствовала полностью. Хотя в возрасте 40—70 лет частота легких нарушений эрекции остается стабильной, частота среднетяжелых нарушений за последнее время удвоилась (с 17 до 34%), а частота импотенции утроилась (с 5 до 15%). Факторами риска импотенции являются сахарный диабет, болезни сердца, артериальная гипертония, низкий уровень холестерина липопротеидов высокой плотности, лучевая терапия и хирургическое лечение рака предстательной железы. Мужчины с импотенцией склонны к депрессии и гневу. Помимо высокой частоты импотенции Национальный опрос, посвященный здоровью и социальной жизни, выявил у американцев в возрасте 18—59 лети другие нарушения половой функции: преждевременную эякуляцию (28,5%), снижение полового влечения (15,8%), боязнь неудачи (17%) и отсутствие удовлетворения от половой жизни (8,1%).
Этиология и патогенез
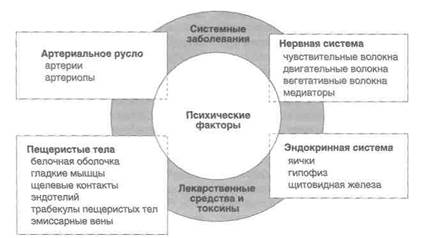
Эрекция зависит от целого ряда психических, нейроген-ных, гормональных, сосудистых и анатомических факторов (рис. 47.4). Разные формы импотенции описаны в соответствующих разделах. Импотенция, возникающая по нескольким или неизвестным причинам, обсуждается в разделе «Другие причины».
Психические расстройства
Первые гипотезы объясняли импотенцию тревожностью. В. Мастере и В. Джонсон ввели понятия «боязни неудачи» и «самонаблюдения». Среди причин психогенной импотенции выделяют строгое воспитание, религиозные убеждения, невроз навязчивых состояний, ангедонию, страх половой жизни, половые извраще-
Глава 47. Нарушения половой функции у мужчин
|
Рисунок 47.4. Факторы, влияющие на эрекцию.
ния, депрессию, синдром вдовца, внешнюю непривлекательность, страх старения и незнание нормальных возрастных изменений, а также патологическое разделение всех женщин на святых и развратниц. В 1950-х гг. импотенцию в 90% случаев считали психогенной. Теперь же большинство авторов признают, что более чем у 50% больных импотенция имеет органическую этиологию. У пожилых этот показатель, возможно, еще выше. Патогенез психогенной импотенции не известен. Предполагается, что в ее развитии играют роль повышение симпатического тонуса и замедленное высвобождение медиаторов.
Нервные болезни
Нейрогенная импотенция возникает в результате органического или функционального поражения головного или спинного мозга, нервов пещеристых тел полового члена и полового нерва, нервных окончаний и рецепторов. Наибольший интерес среди этих нарушений вызывают повреждения спинного мозга. Известно, что эрекция сохраняется у 95% больных с полным разрушением корковых мотонейронов и только у 25% — с разрушением периферических мотонейронов. В первом случае эрекция является рефлекторной, во втором — психогенной. В то же время, если центральные и периферические мотонейроны частично сохранены, эрекция наблюдается более чем у 90% больных. Как полагают, патология головного мозга (опухоли, эпилепсия, инсульт, болезнь Паркинсона, болезнь Альцгеймера) приводит к импотенции из-за подавления полового влечения или чрезмерного торможения спинномозговых центров эрекции. При поражении спинного мозга (позвоночная расщелина, грыжа межпозвоночного диска, сиринго-миелия, опухоли, спинная сухотка, рассеянный склероз) может прерываться как афферентная, так и эфферентная иннервация полового члена. Нейропатии, например при сахарном диабете, алкоголизме, авитаминозах, сопро-
вождаются поражением нервных окончаний и дефицитом медиаторов. Повреждение нервов пещеристых тел полового члена или полового нерва в результате травмы, радикальной простатэктомии или операций на прямой кишке тоже может вызывать импотенцию.
Эндокринные болезни
Самое частое эндокринное заболевание, выявляемое у больных импотенцией, — сахарный диабет. Причиной импотенции в этом случае служат не столько эндокринные, сколько сосудистые и неврологические нарушения, а также психические расстройства или их сочетание. Снижением полового влечения и исчезновением ночных эрекций может проявляться гипогонадизм, обусловленный опухолью гипоталамуса или гипофиза, приемом эстрогенов или антиандрогенов. То же самое наблюдается после двусторонней орхиэктомии по поводу рака предстательной железы. При зрительной эротической стимуляции возможна нормальная эрекция, то есть способность к эрекции при гипогонадизме сохраняется. При гиперпролактинемии импотенция, вероятно, обусловлена тоже снижением полового влечения. Среди других причин снижения полового влечения и импотенции следует отметить тиреотоксикоз, гипотиреоз, синдром Кушинга, надпочечниковую недостаточность. Что лежит в основе патогенеза импотенции в каждом из этих случаев — эндокринные нарушения или другие факторы, еще предстоит выяснить.
Болезни артерий
В отсутствие эрекции кровоток в пещеристых телах полового члена минимален, но достаточен для нормального метаболизма. Содержание газов в крови пещеристых тел такое же, как в венозной. При эротической стимуляции артерии расширяются, через них быстро притекает большой объем артериальной крови, которая заполняет и расширяет ячейки (фаза набухания). В фазе
Глава 47. Нарушения половой функции у мужчин
 полной эрекции приток и отток крови вновь сокращаются до минимального, необходимого для поддержания эрекции. Давление в пещеристых телах при этом составляет около 100 мм рт. ст.
полной эрекции приток и отток крови вновь сокращаются до минимального, необходимого для поддержания эрекции. Давление в пещеристых телах при этом составляет около 100 мм рт. ст.
В экспериментах на животных показано, что чем вы-раженнее артериальная недостаточность, тем больше времени проходит до наступления фазы полной эрекции. Из-за стеноза или уплотнения артериальной стенки снижается давление в глубокой артерии полового члена. При этом ячейки пещеристых тел заполняются частично и не расширяются настолько, чтобы сдавить большинство вен. Больные с артериальной недостаточностью чаще всего отмечают неполную эрекцию, трудности в ее поддержании или быстрое наступление де-тумесценции. Выявлена прямая зависимость между возрастом и распространенностью ишемической болезни сердца и импотенции. Хотя импотенция артериального происхождения может быть посттравматической или врожденной, чаще всего она возникает при системном поражении артерий. Преимущественная локализация поражения и его проявления у разных больных неодинаковы. Иногда, если приток артериальной крови к пещеристым телам превышает отток венозной, эрекция может сохраняться даже при тяжелом поражении артерий, и наоборот, при минимальном поражении артерий эрекция может отсутствовать из-за относительно интенсивного венозного оттока, дисфункции гладких мышц пещеристых тел или дефицита медиаторов. Таким образом, обследуя больных, нужно учитывать сразу все факторы, влияющие на эрекцию.
Поражение артерий полового члена можно разделить на внутриорганное и внеорганное. К последнему относят окклюзию аорты (синдром Лериша), общей подвздошной или внутренней половой артерии, синдром тазового обкрадывания и травму таза. При внеорганном поражении показаны реконструктивные операции на сосудах. Внутриорганное поражение наблюдается при старении, атеросклерозе и сахарном диабете. Хирургическое лечение при этом малоэффективно.
Патология пещеристых тел
С помощью кавернозографии во время зрительной эротической стимуляции обнаружено, что причиной импотенции может быть отток венозной крови. Как установлено в экспериментах на животных, сдавление вен между расширяющимися ячейками пещеристых тел и белочной оболочкой зависит от расслабления гладких мышц трабекул и растяжимости ячеек. Выделяют 5 типов импотенции из-за патологии пещеристых тел, или импотенции венозного происхождения. При типе 1 патология обусловлена слишком большим диаметром вен, по которым кровь оттекает от пещеристых тел, при типе 2 — перерастяжением вен из-за деформации белочной оболочки (при болезни Пейрони или возрастных изменениях), при типе 3 — нарушением расслабления глад-комышечных клеток пещеристых тел вследствие фиброза или изменений щелевых контактов, при типе 4 —
дефицитом медиаторов (при нейрогенной или психогенной импотенции, а также патологии эндотелия), при типе 5 — аномальным сообщением между пещеристыми и губчатым телами. Последнее может быть врожденным, посттравматическим и ятрогенным (после шунтирующей операции по поводу приапизма).
Из-за неполной окклюзии вен эрекция становится неполной или кратковременной. Она может отсутствовать с раннего возраста или исчезать в 30—40 лет. Поражение ячеек пещеристых тел с последующей импотенцией наблюдается при патологии полового члена: болезни Пейрони, опухолях, системной склеродермии, ушибе или переломе. Импотенция наблюдается более чем у 50% больных приапизмом из-за фиброза пещеристых тел. У больных сахарным диабетом и атеросклерозом при электронной микроскопии биоптатов пещеристых тел, полученных во время фаллопротезирования, часто выявляют атрофию гладких мышц, фиброз и повреждение эндотелия. Кроме того, у больных сахарным диабетом и алкоголизмом, как правило, находят изменения нервных окончаний. При исследовании ткани, полученной при пункционной биопсии пещеристых тел, выявляют увеличение содержания коллагена, уменьшение числа гладкомышечных клеток, истончение эндотелия и уменьшение содержания эластических волокон. Кроме того, отчасти из-за уменьшения числа гладкомышечных клеток во время эрекции в пещеристых телах снижается Ра02 и не блокируется отток венозной крови.
Date: 2016-11-17; view: 454; Нарушение авторских прав