
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Ход работы. Приготовление эталонных растворов меди (II)
|
|
Приготовление эталонных растворов меди (II).
1. Приготовьте стандартный раствор меди (II), содержащий 5,0 мг/мл Cu2+.
2. В мерные колбы на 50,0 мл отберите, соответственно, 1,00; 1,50; 2,00; 2,50 и 3,00 мл раствора, содержащего 5,0 мг/мл Cu2+.
В каждую колбу добавьте по 5 мл раствора аммиака (1:1), доведите раствор до метки дистиллированной водой и тщательно перемешайте.
Подготовка анализируемого раствора меди (II).
1. Из мерной колбы, содержащей раствор 2, отберите пипеткой аликвоту, перенесите в мерную колбу на 50,0 мл, прилейте 5 мл раствора аммиака (1:1) и доведите до метки дистиллированной водой.
2. Аналогично в другой мерной колбе на 50,0 мл приготовьте еще один раствор анализируемого вещества для параллельного определения меди (II).
Измерение оптической плотности растворов.
1. Измерьте оптические плотности эталонных растворов на колориметре на λ = 610 нм в кюветах с толщиной слоя l = 1,0 см, раствором сравнения служит вода. Результаты измерений занесите в табл.2.
2. Измерьте оптические плотности анализируемых растворов Ах на колориметре на λ = 610 нм в кюветах с толщиной слоя l = 1,0 см.
Таблица 2
Данные для построения градуировочного графика для определения содержания Cu2+
(Прибор; l =; l = 1,0 cм; Vр-ра = 50,0 мл)
| № | Добавлено р-ра Cu2+, мл | Содержание mi(Cu2+), мг | A1i | A2i | 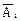
|
| 1,00 | |||||
| 1,50 | |||||
| 2,00 | |||||
| 2,50 | |||||
| 3,00 |
Определение содержания меди(II) методом градуировочного графика.
1. Постройте градуировочный график для определения Cu2+ в растворе в координатах 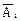 – mi(Cu2+).
– mi(Cu2+).
2. Пользуясь градуировочным графиком, по измеренным значениям оптической плотности Ах найдите содержание Cu2+ в фотометрируемых растворах (mx(Cu2+), мг).
3. Рассчитайте массу меди (II) 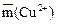 в растворе 2 (в анализируемой смеси).
в растворе 2 (в анализируемой смеси).
Лабораторная работа
Date: 2015-05-22; view: 1409; Нарушение авторских прав