
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Ионообменная хроматография в количественном анализе
|
|
Ионообменная хроматография не является самостоятельным методом количественного анализа. Ее используют как вспомогательный метод, т.е. метод разделения и выделения веществ, предшествующий их количественному определению. Ионообменная хроматография используется для разделения ионов путем выделения одного (или группы ионов) из смеси, концентрирования вещества из сильно разбавленных растворов, удаления ионов, мешающих выполнению анализа. Выделенные компоненты определяют обычными химическими, физико-химическими методами анализа.
Основные задачи, решаемые методом ионообменной хроматографии:
1. Отделение катионов от анионов с помощью катионита или анионита.
2. Разделение ионов одного знака, основанное на различном их сродстве к иониту.
Эмпирически установлено, что чем больше заряд иона, тем он имеет большее сродство к иониту, т.е. сильнее им удерживается и труднее элюируется. Сродство к иониту, как правило, усиливается в рядах:
M+ < M2+ < M3+ < M4+ и
X– < X2– < X3–,
что позволяет разделять ионы разного заряда.
Подбирая состав элюирующего раствора, можно разделить ионы, имеющие одинаковый заряд. Например, элюирование раствором 0,1 моль/л HCl сорбированных на катионите ионов Na+ и K+ позволяет провести их разделение: вначале «вымывается» Na+, затем K+.
Использование в качестве элюентов растворов веществ, образующих с определяемыми ионами комплексы различной устойчивости, позволяет разделять очень близкие по свойствам ионы.
3. Определение суммарного содержания катионов или анионов в растворе и анализ растворов чистых солей.
В результате эквивалентности ионного обмена количество вещества эквивалентов ионов Н+ в фильтрате после пропускания анализируемого раствора через колонку с катионитом в Н-форме равно общему количеству вещества эквивалентов ионов металла, внесенных в колонку, если в анализируемом растворе не было свободных кислот.
Например, при пропускании через катионит в Н-форме раствора соли натрия в результате ионного обмена
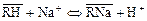
в растворе появится эквивалентное количество Н+-ионов:
n(Na+) = n(H+).
Таким образом можно готовить стандартные растворы хлороводородной кислоты, пропуская раствор точной навески NaCl через катионит в Н-форме.
4. Получение деионизированной воды пропускание воды через катионит и анионит. Такая вода используется вместо дистиллированной.
Date: 2015-05-22; view: 988; Нарушение авторских прав