
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Ход работы. Приготовление эталонных растворов железа (III)
|
|
Приготовление эталонных растворов железа (III).
1. Приготовьте стандартный раствор железа (III), содержащий 0,10 мг/мл Fe3+.
2. В мерные колбы вместимостью 50,0 мл отберите, соответственно, 1,00; 1,50; 2,00; 2,50; 3,00 мл раствора соли железа, содержащего 0,10 мг/мл Fe3+. В каждую колбу добавьте 5 мл 10% раствора сульфосалициловой кислоты, 5 мл раствора аммиака (1:1), доведите до метки водой и тщательно перемешайте.
Подготовка анализируемого раствора железа (III).
1. Отберите пипеткой аликвоту анализируемого раствора из мерной колбы, содержащей раствор трисульфосалицилата железа (III) (раствор 1), и перенесите в мерную колбу на 50,0 мл, доведите объем до метки дистиллированной водой и тщательно перемешайте.
2. Аналогично в другой мерной колбе на 50,0 ил приготовьте еще один раствор анализируемого вещества для параллельного определения содержания железа (III).
Измерение оптической плотности растворов.
1. Измерьте оптическую плотность полученных эталонных растворов на колориметре на λ = 410 нм в кюветах с толщиной слоя l = 1,0 см, используя дистиллированную воду в качестве раствора сравнения. Результаты измерений занесите в табл.1.
2. Измерьте оптическую плотность подготовленных анализируемых растворов Ах в условиях, при которых фотометрировали эталонные растворы.
Таблица 1
Данные для построения градуировочного графика для определения содержания Fe3+
(Прибор; l =; l =; Vр-ра = 50,0 мл)
| № | Добавлено р-ра Fe3+, мл | Содержание mi(Fe3+), мг | A1i | A2i | 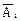
|
| 1,00 | |||||
| 1,50 | |||||
| 2,00 | |||||
| 2,50 | |||||
| 3,00 |
Определение железа (III) методом градуировочного графика.
1. Постройте градуировочный график зависимости Ai от содержания Fe3+ в растворе.
2. Пользуясь градуировочным графиком, по измеренным значениям оптической плотности Ах найдите содержание Fe3+ в фотометрируемых растворах.
Рассчитайте массу железа (III) 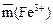 в растворе 1 (анализируемой смеси).
в растворе 1 (анализируемой смеси).
Date: 2015-05-22; view: 2353; Нарушение авторских прав